Д.х.н.,
профессор Байкенов М.И., докторант PhD Гудун К.А., профессор Ма
Фэн Юн*
Карагандинский
государственный университет им. Е.А. Букетова, Казахстан
* Сыньцзяньский университет, КНР
ОПРЕДЕЛЕНИЕ
КИНЕТИЧЕСКИХ ПАРАМЕТРОВ ВОССТАНОВЛЕНИЯ АНТРАЦЕНА И ДИФЕНИЛА В АТМОСФЕРЕ
ВОДОРОДА В ПРИСУТСТВИИ НАНОЧАСТИЦ ЖЕЛЕЗА
Потребность в нефтепродуктах растет с каждым годом. Необходим поиск новых подходов в решении вопросов получения различных видов жидкого топлива, в связи с увеличение стоимости добычи и транспортировки нефти, мероприятий по охране природы. И перспективным направлением в этой области является поиск новых катализаторов или каталитических систем. Основным решением проблемы получения синтетической нефти в странах СНГ и дальнего зарубежья является метод прямой гидрогенизации.
Наравне с разработками теории и технологии гидрогенизации углей и установления принципов управления этим процессом изучается превращение индивидуальных углеводородов, моделирующие органическую массу угля, в среде водорода.
Катализаторы гидрогенизации углей можно классифицировать на гетерогенные, растворимые (гомогенные) системы и расплавы [1]. Согласно Б.Н. Кузнецову предпочтение следует отдавать растворимым системам, так как при их нанесении достигается наиболее равномерное и тонкое распределение активного металла по поверхности угля.
В работах [2 – 5] показано, что более эффективными в процессах
переработки углеводородного сырья являются
катализаторы, вводимые в процесс в виде высокодисперсных частиц, равномерно
распределённых во всём объёме сырья. Для
обеспечения стабильности системы «катализатор – сырьё» размеры частиц катализатора должны приближаться к диаметру
частиц истинных или коллоидных растворов. Подобные каталитические системы
принято назвать псевдогомогенными.
Псевдогомогенные каталитические добавки (ПГКД) в настоящее время используются в
процессах гидрокрекинга тяжёлых нефтяных остатков и фракционировании нефтяного
сырья. В качестве ПГКД в нефтепереработке используют растворимые в нефтяном
сырье нафтенаты молибдена [2], алкилфосфат и сульфонат молибдена [3], эмульсия
водного раствора парамолибдата
аммония [4] и др. Применение псевдогомогенных катализаторов позволяет снизить
температуру и давление процесса, увеличить глубину превращения сырья и выход
целевого продукта.
Уже давно установлено [6], что в процессах гидрогенизации наблюдаются реакции гидрирования, изомеризации, деструкции и алкилирования ароматических углеводородов. Нами была проведена гидрогенизация смеси антрацена и дифенила с добавлением сульфата железа в автоклавных условиях. Целью данной работы было установление влияния ПГКД на гидрогенизацию смеси полиароматических углеводородов; установление кинетики гидрогенизации данной модельной смеси.
Модельная смесь состояла из антрацена и дифенила. Антрацен и дифенил взяли в равных количествах по 0,59 г. В качестве ПГКД использовали 5% водный раствор сульфата железа (II). Гидрогенизацию смеси антрацена и дифенила проводили в реакторе высокого давления (автоклаве) с внутренней мешалкой. Продолжительность гидрогенизации полиароматической смеси в автоклавных условиях варьировалось от 20 до 60 минут при температуре 400 оС и начальном давлении водорода 6 МПа, объем автоклава 0,05 л.
В процессе каталитической гидрогенизации модельной смеси ПГКД сульфат железа (II) генерируется в наноразмерный сульфид железа (рис. 2).
На рисунке 2 показано образование наноразмерных частиц сульфида железа, представленных в виде нанотрубок.
|
|
|
|
а) |
б) |
Рис. 2. Микрофотография наноразмерных частиц сульфида железа, время обработки а) 20минут, б) 40 минут
Анализ жидких продуктов гидрогенизации антрацено–дифениловой смеси выполняли на хромато-масс-спектрометре 7890A Agilent Technologies. Анализ гидрогенизата с помощью ХМС показал, что получаемый гидрогенизат состоит из гидроароматических углеводородов с одним и двумя нафтеновыми кольцами, продуктами деструкции, алкилирования и изомеризации. Как показал анализ, антрацен гидрируется очень быстро в интервале от 20 до 60 минут, дифенил с умеренной скоростью, а образуемый гидроароматический углеводород имеет одно нафтеновое кольцо.
На рисунке 3 показана кинетическая схема гидрогенизации смеси, состоящей из полиароматических углеводородов.
B C k1
![]()
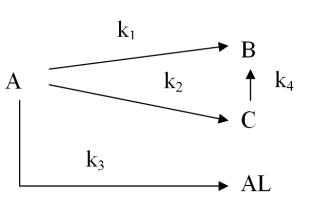
Рис. 3. Кинетическая схема гидрогенизации смеси полиароматических углеводородов в присутствии наноразмерного катализатора
Анализ ХМС гидрогенизатов показал, что до 40 минут в гидрогенизате продукты гидрирования представлены производными гидроароматических углеводородов антрацена (имеющих по 1 и 2 нафтеновыми кольцами), а дифенил до 40 минут не гидрируется, а дает только алкилпроизводные дифенила. Гидрирование дифенила начинается после 40 минут автоклавной обработки смеси. Антрацен гидрируется с большой скоростью, а дифенил с умеренной скоростью. Высокая степень конверсии антрацена, по-видимому, связана с высокой активностью наноразмерных частиц.
Анализ литературы показывает [7], что в присутствии гетерогенных катализаторов (сульфида железа или оксида железа) скорость гидрирования дифенила очень низкая. Нами в присутствии наноразмерного катализатора удалось повысить выход гидропроизводных дифенила до 10-12%, тогда как в присутствии гетерогенных катализаторов, выход гидропроизводных дифенила не превышал 2-5%.
На рисунке 4 показана кинетическая зависимость группового состава гидрогенизата от времени контакта. Анализ кривых показывает, что при увеличении продолжительности выход групповых составов гидрогенизата увеличивается. В условиях автоклавной обработки смеси наблюдается высокая скорость протекания реакции деструкции и гидрирования полиароматических углеводородов.
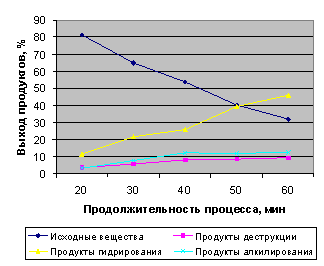
Рис. 4. Зависимость выхода по групповому составу гидрогенизата от продолжительности гидрогенизации смеси полиароматических углеводородов.
На основе кинетической схемы и результатов гидрогенизации смеси
полиароматических углеводородов (рис. 3, 4) нами была составлена кинетическая
модель гидрогенизации смеси антрацена и дифенила, которая представлена в виде
системы дифференциальных уравнений:
![]()
![]()
![]()
![]()
где [A], [B], [C], [AL] – массовые доли группового состава гидрогенизатов в момент времени t; [A] – смесь полиароматических углеводородов; [B] – групповой состав гидрогенизата продуктов деструкции; [С] – групповой состав продуктов гидрирования; [AL] – групповой состав продуктов алкилирования; ki – константа скорости гидрогенизации смеси полиароматических углеводородов, мин-1, k1 – константа скорости реакции деструкции смеси полиароматических углеводородов; k2 – константа скорости реакции гидрирования смеси полиароматических углеводородов; k3 – константа скорости алкилирования смеси полиароматических углеводородов; k4 – константа скорости деструкции продуктов гидрирования.
Расчет системы дифференциальных уравнений проводили с использованием программы «Поиск» [8]. Рассчитанные константы скорости приведены в таблице
Таблица – Рассчитанные константы скорости гидрогенизации смеси полиароматических углеводородов в присутствии наноразмерного катализатора
|
Т, К |
k1, мин-1 |
k2, мин-1 |
k3, мин-1 |
k4, мин-1 |
|
673 |
0,00937 |
0,04107 |
0,01588 |
0,02687 |
В таблице показано, что лимитирующая скорость конверсии смеси полиароматических углеводородов является стадия превращения смеси полиароматических углеводородов в продукты деструкции. На основе рассчитанных констант скоростей получен ряд гидрогенизации смеси полиароматических углеводородов. Скорость конверсии группового состава гидрогенизатов снижается в следующем ряду:
![]()
Таким образом, рассчитаны константы скорости конверсии группового состава гидрогенизатов смеси полиароматических углеводородов в присутствии наноразмерного катализатора (Т = 400 оС). Установлен ряд скорости конверсии группового состава смеси полиароматических углеводородов антрацена и дифенила. Установлено, что имеет место значительное различие в реакционной способности подвергаться гидрогенизации антрацена и дифенила в смеси, что хорошо иллюстрирует неравную реакционную способность органической массы первичной каменноугольной смолы.
Работа проводилась при финансовой поддержке Key Laboratory of Oil & Gas Fine
Chemicals, Ministry of Education & Xinjiang Uyghur Autonomous Region,
Xingjian University
Список литературы
[1] Кузнецов Б.Н. Катализ химических превращений угля и биомассы. – Новосибирск: Наука. – 1990. – 259 с.
[2] Кричко
А.А., Озеренко А.А., Фросин С.Б., Зекель Л.А., Малолетнев А.С. и др.
Псевдогомогенные катализаторы, синтез и особенности формирования // Катализ в промышленности. – 2007. – № 2. – С. 30 – 36.
[3] Кричко
А.А., Озеренко А.А., Малолетнев А.С., Зекель Л.А., Фросин С.Б., Шпирт
М.Я. и др. Применение псевдогомогенных катализаторов для глубокой
переработки нефтяного и коксохимического сырья // Катализ в промышленности. – 2007. – № 3. – С. 23 – 32.
[4] Зекель Л.А. Молибденсодержащие каталитические системы для процессов гидрогенизационной переработки углей // ХТТ. – 2001. – № 5. – С. 49 – 56.
[5] 3екель
Л.А., Малолетнев А.С., Озеренко А.А., Шпирт М.Я. Основы синтеза и
применения псевдогомогенных катализаторов для гидрогенизации углей и нефтяного сырья // ХТТ. – 2007. – №
1. – С. 35 – 42.
[6] Калечиц И.В. Химия гидрогенизационных процессов в переработке топлив. – М: Химия. – 1973. – 336 с.
[7] Калечиц И.В. Моделирование ожижения угля. – М: ИВТАН. – 1999. – 229 с.
[8] Шахтахтинский Т.Н., Бахманов М.Ф. Методы оптимизации процессов химической технологии с программами для ЭВМ. – Баку: Элм. – 1985. – 260 с.

