Физика / 4.
К.т.н.
Родионов И.В.
Саратовский государственный технический
университет
Обоснование
применения способов электризации для создания в оксидных биопокрытиях
имплантатов состояния отрицательно-гомополярного электрета
Имплантология как отрасль медицины в современных условиях
развивается ускоренными темпами благодаря ее возможностям полного восстановления
нарушенных либо утраченных функций органов и систем организма. Это достигается
за счет применения имплантатов – медикотехнических
изделий из небиологического материала, контактирующих с биологической средой в
течение продолжительного времени. Наиболее широко используются костные имплантаты
в стоматологии и ортопедии для замены утраченных либо исправления поврежденных
костных структур организма. Стоматологические имплантаты, предназначенные для
лечения заболеваний и исправления дефектов челюстно-лицевой системы,
представляют искусственные корни зубов или специальные пластины для сращения и
коррекции поврежденной костной ткани челюсти либо костей черепно-лицевой
области. К ортопедическим имплантатам относятся
имплантационные конструкции, используемые для замены функций различных
суставов, коррекции сегментов позвоночника, лечения переломов конечностей и
т.д. Наиболее широкое применение находят имплантаты для лечения переломов
конечностей, которыми в большинстве случаев служат стержневые и спицевые остеофиксаторы,
позволяющие осуществлять направленный остеосинтез
поврежденных частей кости.
Костные имплантаты испытывают биологическое влияние среды, а также действие механических функциональных
нагрузок. Поэтому часто применяются имплантаты комбинированной конструкции,
характеризуемые наличием прочной металлической основы из биоинертных
титана, циркония либо тантала и имеющие покрытие из биокерамического
материала, который может представлять специально сформированный слой металлооксида. Свойства биосовместимости обусловливают
способность оксидного покрытия к интеграции с окружающей биотканью
и обеспечивают наиболее эффективное функционирование имплантата.
Технологические процессы формирования оксидных биопокрытий характеризуются большим разнообразием, при этом
они должны придать покрытию необходимые адгезионные
свойства и качества биоактивности, включающие
определенный фазовый состав, структурную пористость и морфологическую гетерогенность поверхности. В этих условиях происходит
адсорбция аморфных белковых структур на поверхности покрытия, что обеспечивает
его физико-химическую связь с биосредой. Благодаря
данной связи возникает ионизация атомов материала покрытия с последующей
диффузией ионов в белковый слой и в биосреду.
Протекающие биоэлектрохимические реакции вызывают деструкцию
материала, и в образующиеся несплошности прорастают
костные структуры окружающей ткани, происходит остеоинтеграция
с образованием прочной биотехнической системы «имплантат – кость».
Функционирование
биоструктур организма характеризуется протеканием биоэлектрохимических процессов, которые сопровождаются
образованием биопотенциалов, а также появлением биотоков, что приводит к спонтанному
возникновению явлений поляризации биоструктур. За
счет этого формируется их электретное состояние и создаются собственные
электрические поля, влияющие на процессы жизнедеятельности. Поэтому придание
диэлектрическому оксидному покрытию электретного состояния приближает его
качества к свойствам биоткани, улучшает их
взаимодействие и стимулирует протекание интеграции. При этом поддерживаются
процессы вещественного обмена, микроциркуляции биожидкостей, развивается регенерация биоткани
без опасности тромбообразования, воспалительных
осложнений и отторжения имплантата. Кроме того, на поляризованной поверхности покрытия протекают интенсивные
сорбционные явления по отношению к витаминам, протеинам, антибиотикам, что
обеспечивает ускоренное и эффективное приживление имплантата в операционной
ране. Наиболее значимым показателем электретного оксидного покрытия является
высокая тромборезистентность, исключающая в начальный
период остеоинтеграции образование тромбов в микрососудах, расположенных вблизи функциональной
поверхности имплантата. Тромборезистентность достигается
за счет создания в покрытии отрицательно-гомополярного заряженного состояния и
внешнего квазистатического поля, воздействие которого на биоткань
вызывает отталкивание тромбоцитов, имеющих природный отрицательный заряд.
Поэтому при формировании заряда покрытия ему, как правило, придается
отрицательный знак, что обеспечивается путем инжектирования
электронов в структуру биоматериала и их закрепления
в, так называемых, «электронных ловушках».
Электретное
состояние диэлектриков может создаваться с использованием их внутренней, а
также внешней релаксационной поляризации, для чего применяются такие способы,
как термоэлектризация, короноэлектризация,
фотоэлектризация, радиоэлектризация,
механоэлектризация, трибоэлектризация
[1,2]. При этом необходимо учитывать, что биокерамические
оксидные покрытия не обладают дипольной структурой, поэтому их электризация
осуществляется путем внешней поляризации за счет накопления зарядов в
«ловушках» - структурных дефектах и микронесплошностях.
Кроме того, из-за сложности формы и малых размеров костных имплантатов, а также
фотонепрозрачности их материалов и покрытий
применение к ним механо-, трибо-
и фотоэлектризации оказывается затруднительным либо
невозможным, а термоэлектризация создает только
слабые поверхностные заряды с коротким периодом существования квазистатического
поля. Таким образом, для получения объемного гомополярного отрицательного
заряда повышенного значения и увеличенной стабильности целесообразно использовать
способы радиационной поляризации диэлектрических оксидных биопокрытий
путем b-облучения,
а также поляризации в условиях коронного разряда.
Электризация
путем b-облучения. В данных условиях электретное состояние покрытия
возникает за счет воздействия на него потока быстрых электронов, причем способ
реализуется как при действии электрического поля, так и в его отсутствие.
При действии электрического поля
оксидированный имплантат размещается между двумя тонкими электродами, так что
длина свободного пробега электронов превышает толщину покрытия, и электроны b-облучения могут
проникать насквозь (рис. 1). Электрическое поле, воздействующее на покрытие,
имеет напряженность порядка 20 кВ/см, что вызывает
направленное смещение свободных заряженных частиц и их закрепление в
структурных «ловушках». Электронный поток с энергией около 10 МэВ формируется в ускорителе и выходит из его окна, где на
расстоянии 0,1…0,3 мм располагается верхний электрод системы, имеющий вид
сетки. В результате воздействия пронизывающих покрытие электронов на его
поляризованную структуру в течение нескольких минут происходит усиление
направленного смещения заряженных частиц и возрастание величины гомополярного
отрицательного заряда покрытия.
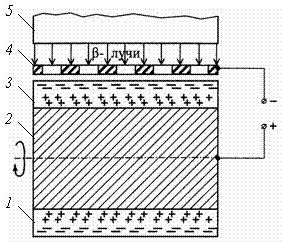
Рис. 1. Радиоэлектризация с воздействием электрического поля: 1, 3 – оксидное покрытие, 2
– металлическая основа имплантата, 4 – сетчатый электрод, 5 – выходное окно ускорителя
Без применения электрического поля радиационная электризация осуществляется при размещении имплантата с покрытием на электроде в вакуумной камере ускорителя, где создается электронный поток с энергией 2,5 МэВ (рис. 2).
Воздействие потока заключается в проникновении
электронов на глубину до 0,4 мм, их закреплении в «ловушках» и формировании
отрицательного заряда во внешнем слое покрытия с образованием положительного
заряда на его внутренней приграничной поверхности. В результате b-облучения оксидное биопокрытие костных имплантатов приобретает гомополярный
отрицательный заряд повышенной стабильности с продолжительностью существования
от нескольких недель до нескольких месяцев. Величина плотности заряда
составляет примерно 10-8 Кл/см2, что близко соответствует плотности
естественного заряда костной ткани. В этих условиях происходит стимулирование
процессов остеогенеза, ускорение остеоинтеграции
электретного имплантата и его приживления в кости. Последующее функционирование
имплантата протекает с предотвращением возможности образования фиброзной прослойки,
опасности расшатывания имплантата, воспаления окружающих тканей и отторжения.
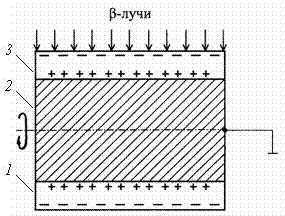
Рис.
2. Радиоэлектризация без воздействия электрического
поля: 1, 3 – оксидное покрытие, 2 – металлическая основа имплантата
Электризация
в условиях коронного разряда. Применение методов поляризации для
изготовления костных имплантатов связано со значительными технологическими
трудностями, в то же время короноэлектризация по
сравнению с вышеуказанными методами является технологически более простой и
эффективной.
Сущность короноэлектризации состоит в создании коронного разряда на
поверхности оксидного покрытия с помощью поляризующих электродов в виде тонких
игл либо струн, расположенных вблизи коронируемой поверхности. Приложенное к
электродам повышенное напряжение создает за счет малой площади их поверхности
большую напряженность электрического поля с высокой его неоднородностью, чем
вызывается ионизация и пробой воздушного промежутка при низких значениях тока.
Возникающий коронный разряд между самими поляризующими электродами и
поверхностью покрытия формирует поток ионов и лавину электронов, направленную к
покрытию и инжектирующую электроны в его поверхностный слой, при соединении
покрытия с массой через металлический имплантат (рис. 3).
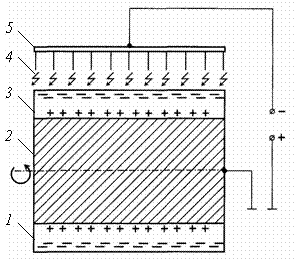
Рис. 3.
Схема процесса короноэлектризации биопокрытия костных имплантатов: 1, 3 – оксидное
покрытие; 2 – металлическая основа
имплантата; 4 – коронные разряды;
5 – коронирующие иглы
В результате коронирования
покрытия образуется гомополярный отрицательный заряд, формирующий стабильное
электретное состояние поверхностного слоя. Наиболее перспективным является
применение коронирования для электризации оксидных биопокрытий небольшой толщины на имплантатах малого габарита,
к которым относятся, например, стоматологические костные конструкции,
ортопедические остеофиксаторы и эндопротезы,
искусственные клапаны сердца.
Рассмотренные способы электризации путем b-облучения и коронирования проходят комплексное
исследование их влияния на качества биоактивности
оксидных покрытий металлоимплантатов. На основе
результатов исследования проводится отработка конструктивно-технологических
параметров для создания технологии получения костных имплантатов с электретными
покрытиями, обладающими высокими качествами биоактивности.
Литература
1. Губкин А.Н. Электреты.
М.: Наука. 1978. 192 с.
2. Гольдаде В.А., Пинчук
А.С. Электретные пластмассы: физика и материаловедение. – Минск: Наука и
техника, 1987. 231 с.