ВЗАИМОДЕЙСТВИЕ
МЕТИЛЦИКЛОПРОПИЛКЕТОНА С ФЕНИЛАЦЕТИЛЕНОМ
Минбаев
Б.О. – Доктор химических наук, профессор
Шуланбай
А.Ж. – Магистрант
Казахский национальный технический
университет имени К.И. Сатпаева
Метилциклопропилкетон мен фенилацетиленнің
әрекеттесу реакциясын зерттей отырып, алынған конденсация
өнімінің құрлысын және физика-химиялық
қасиеті анықталған.
Изучение реакции
взаймодействия метилциклопропилкетона с фенилацетиленом, установление строения
и определение физико – химических свойств продукта конденсации.
Study of the reaction
vzaymodeystviya metiltsiklopropilketona with phenylacetylene, the establishment
of the structure and the definition of physical - chemical properties of the
condensation product.
Фенилацетиленовые производные ароматических углеводородов
представляют большой практический интерес как органические люминофоры,
перспективные рабочие среды для оптических квантовых генераторов, органические
красители, оптические отбеливатели, сцинтилляторы [1]. Заместители с тройными
углерод углеродными связями легко превращаются в другие функциональные группы,
что делает их ценными полупродуктами в органических синтезах [2]. Наиболее
перспективны в этом плане фениллпроизводные ароматических углеводородов,
содержащие в структуре высокосопряженное конденсированное ароматическое ядро.
Ацетиленовые спирты представляют собой класс соединений, весьма
интересный с точки зрения химических и физиологических свойств. Среди таких
спиртов и их производных найдены эффективные пестициды, лекарственные
препараты, бактерициды [3,4,5]. Соединения этого ряда, содержащие разнообразные
заместители, с давних пор привлекают внимание широкого круга исследователей.
Однако немногочисленные работы [6, 7] по получению циклических ацетиленовых
соединений не дают полного представления о химизме и физиологической активности
этого класса соединений. Исследование ацетиленовых соединений с различными,
функциональными группами имеет большое теоретическое и практическое значение и
открывает широкие возможности для синтеза новой группы перспективных
непредельных соединений. Начало изучению реакции ацетиленов с карбонильными
соединениями было положено А.Е. Фаворским в 1899-1900 гг. взаимодействие
различных кетонов с фенилацетиленом в присутствии порошкообразного едкого кали
и показали, что этот способ является общим для синтеза третичных ацетиленовых
спиртов
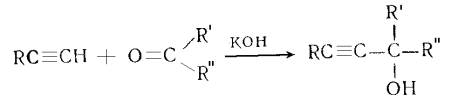
По реакции Фаворского могут быть получены алифатические,
алициклические, ароматические и гетероциклические ацетиленовые и диацетиденовые
спирты и гликоли, ацетиленовые оксикислоты и аминоспирты. Реакция Фаворского лежит
в основе одного из используемых в промышленности метода синтеза изопрена —
сырья для получения синтетических каучуков.
Целью данной работы является изучение состава соединений метилциклопропилкетона и фенилацетилена,
определение возможности получения из них третичных спиртов.
Проведение эксперимента осуществлялось в трехгорлый колбе емкостью 300 мл, снабженную мешалкой, обратным
холодильником, термометром и капельной воронкой (рис.1), помещали 16,2 г гранулированного едкого кали и 240 мл абсалютного бензола. При температуре — 2-0о и
интенсивном перемешивании прибавляли в течении 1 часов смесь, состоящую из 8,4 г метилциклопропилкетона и 5,6 г фенилацетилена, в 60 мл абс. бензола. Реакционную массу при охлаждении ледяной водой
перемешивали в течение 8 и 10 часов при комнатной температуре, затем при
охлаждении до — 8° разлагали
водой (80 мл), эфирный слой отделяли, водный экстрагируем эфиром. Объединенные
эфирные экстракты сушили поташом. Из отфильтрованного экстракта после удаления
бензола, остаток представляет собой розовую жидкость. Полученную
жидкость перегоняем от бензола.
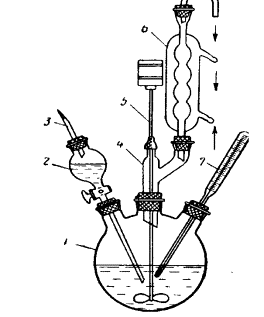
Рисунок 1.
1-реакционная колба, 2-капельная воронка, 3-капилляр, 4-двурогий форштос,
5-мешалка, 6-обратный холодильник, 7-термометр
Конденсацией этого кетона с фенилацетиленом в условиях реакции
Фаворского получен с хорошим выходом третичный ацетиленовый спирт – 1-пропил
3-фенил пропанол-2. Выход продукта составил 70 %. Предполагаемый вариант
реакции синтеза:
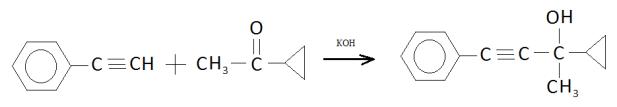
Состав полученный нами продукт исследовался методом инфракрасной
(ИК) спектроскопии. На рисунке 2 представлен
ИК-спектр 1-пропил 3-фенил пропанол-2. В
спектре имеются полосы поглощения с малой интенсивностью при 1640,91; 965,54 и
909 см-1, которые принадлежат производным бензола. Полоса
интенсивности при 1707 см-1 говорит о наличии -ОН групп органических
кислородсодержащих соединений, а полоса поглощения при 1031,84 см-1
принадлежит валентным колебаниям -С-О- групп кислородсодержащих соединений.
Наблюдается полоса поглощения характерная для ароматических структур (1604 см-1)
и наличие полос поглощения насыщенных структур в виде групп -СН, -СН3
в области 1376, 2853 см-1.
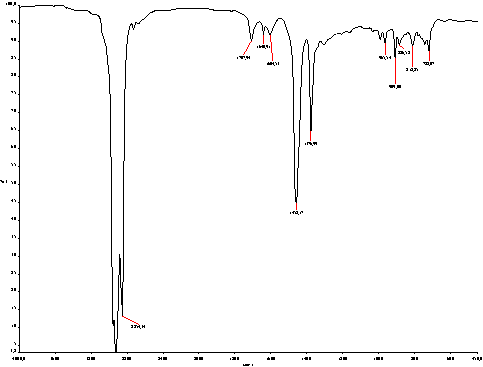
Рисунок 2. ИК-спектр
1-пропил 3-фенил пропанола-2
Исследования реакционной способности ацетиленовых спиртов полоса
поглощения свободной гидроксильной группы асимметрична. При этом в ряду
третичных спиртов асимметрия гидроксильной полосы выражено сильнее. Физико-химические
характеристики исходных и продуктов конденсации представлены в таблице 1.
Электрофильность тройной связи уменьшается, и присоединение нуклеофила
не происходит. При этом электрофильность тройной связи в таких системах будет
зависеть от электронодонорности нуклеофильного остатка, от способности его
компенсировать дефицит электронов. Именно по этой причине оказывается
невозможным присоединение воды к ацетиленовой связи кетонов. Основываясь на
этих рассуждениях, можно было ожидать успешного присоединения следующей
молекулы.
Таблица 1.
Физико-химические характеристики исходных и продуктов конденсации
|
Показатель |
Метилциклопропил кетон |
Фенилацетилен |
1-пропил 3-фенил пропанол-2 |
|
Молекулярный вес |
82 |
102 |
186 |
|
tпл °C |
0,8 |
-44,8 |
18 |
|
tкип °C |
111 |
144 |
171 |
|
d204 |
0,898 |
1,549 |
1,413 |
|
Растворимость в воде, гр/100мл, при 20°C |
18,5 |
Не растворяется |
Не растворяется |
Как видно из табличных данных, продукт органического синтеза
характеризуется высокими значениями температуры кипения – 171°С. По литературным данным можно судить дальнейшие изменения
продукта конденсации. Так как в молекуле имеются тройная связь и спиртная
группа 1-пропил 3-фенил пропанола-2 могут дальше полимеризоваться.
Применение третичные и вторичные ацетиленовые спирты, получающиеся
в реакции Фаворского, в условиях кислотного катализа перегруппировываются в
α,β-ненасыщенные кетоны и альдегиды (перегруппировка Мейера-Шустера):
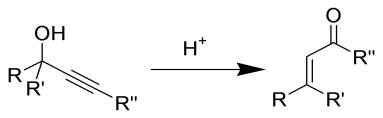
В заключении установлены оптимальные режимы
конденсации кетона и фенилацетилена. Выход продукта конденсации составляет 9 %
меньше теорического выхода продукта. Результаты анализов показали, что синтез
третичного спирта по реакции Фаворского в присутвствии калия конденсация
протекает хорошо, которые в дальнейшем могут использоваться исходным веществом для
получение новых классов органических соединений.
Список
литературы:
1. Мельников Н. Н., Баскаков Ю. А. – Химия гербицидов и регуляторов роста растений.
М., 1962.
2.
Амер. патент 2584420. Chem. Abstracts,
1952, 46, 9605.
3. Назаров И. Н., Иванова Л. И. — Ж. общ. химии, 1956, 26, 78.
4. Азербаев И.Н., Сарбаев Т. Г., Ержанов К.В., Маканов У., Басымбеков М. В.,
Жумартбаев У. Т. – Химия природных соединений и биологически активных веществ в
Казахстане. Алма-Ата, «Наука», 1967, 23.
5. Азербаев И. Н., Сарбаев Т. Г., Ержанов К. Б. — Вестник АН КазССР, 1967,
№3, 42.
6. Азербаев И. Н., Сарбаев Т. Г. Ержанов К. Б. — Изв. АН КазССР, серия хим.,
1967, № 2, 79.
7. Азербаев И. Н., Сарбаев Т. Г., Басымбеков М.Б., Ержанов А.И. — Вестник
АН КазССР, 1967, № 4, 39.
8.
Назаров И. Н., Руденко В. А.— Изв. АН
СССР, отд. хим. наук, 1948, 610.
9. Robert A. Meyers – Encyclopedia of Physical Science and Technology
Organic Chemistry, 2001, 22.