Химия и химические технологии / 5.
К.т.н.
Родионов И.В.
Саратовский государственный технический
университет
Определение
уровня адаптации термооксидированных стальных остеофиксаторов к биосреде по
изменению их коррозионного поведения
Введение
Внешняя
фиксация фрагментов трубчатых костей с использованием металлофиксаторов
аппарата внешнего остеосинтеза является эффективным малоинвазивным методом лечения больных с переломами и
другими костными патологиями как в гуманитарной, так и в ветеринарной медицине
[1-4]. В данных условиях достигается значительное сокращение сроков лечения и
реабилитации пациентов. В то же время при спицевой, а также стержневой фиксации доля возникающих
воспалительных осложнений составляет существенную величину, что связано с
ограниченными биоинтеграционными качествами поверхности
металлов, применяемых для фиксаторов.
Одним из путей решения данной проблемы является применение металлофиксаторов с биокерамическими
покрытиями, способными обеспечить высокий уровень интеграции поверхности с
окружающими биотканями, а также создать условия для
эффективной адаптации остеофиксаторов. Для таких покрытий
используются кальцийфосфатные соединения, биостекло, биоситаллы, углеродные
материалы, при этом методы их нанесения характеризуются повышенной сложностью,
что накладывает существенные ограничения на качества биосовместимости
получаемых покрытий. В число биокерамических материалов
входят оксиды биосовместимых металлов, которые формируются в виде покрытия за
счет химического взаимодействия металла с кислородом. Получение оксидных
покрытий на остеофиксаторах отличается
технологической простотой, образованием их высоких качеств биоинтеграции
и обеспечивается применением различных методов оксидирования фиксаторов, из
которых наиболее эффективными являются термическое и электрохимическое
оксидирование [5, 6].
В числе свойств получаемых покрытий существенное влияние
на их биоинтеграционные качества и уровень адаптации
оказывает коррозионная стойкость при взаимодействии с окружающей биосредой. Поэтому целью данной работы является
исследование изменения коррозионно-электрохимического поведения оксидированных
стержневых остеофиксаторов в биосреде,
а также разработка биотехнических рекомендаций по выбору условий и режима
получения термооксидных покрытий с повышенной
коррозионной стойкостью.
Методика исследования. Опытные остеофиксаторы
представляли винтовые стержни из нержавеющей хромоникелевой стали 12Х18Н9Т, обладающей необходимой биомеханической
совместимостью. Стержни изготовлялись путем токарной обработки и подвергались
пескоструйной обдувке поверхности для удаления загрязняющих слоев и химической
активации. Формирование оксидных биопокрытий
производилось термообработкой в лабораторной электропечи сопротивления с
использованием воздуха и атмосферы перегретого водяного пара.
При
воздушно-термическом оксидировании фиксаторов применялись температуры обработки
400, 500, 600, 7000С с продолжительностью 0,5 ч при каждой
температуре. Паротермическое оксидирование
выполнялось при температуре 5500С и выдержке 2 ч в атмосфере перегретого
водяного пара.
Термооксидированные резьбовые фиксаторы вворачивались в большие берцовые кости
лабораторных животных (кролики породы «черный великан») на 45 суток, после чего
они извлекались из сегментов конечностей и исследовались потенциометрическим
способом на предмет изменения уровня коррозионно-электрохимической стойкости.
Коррозионное
поведение опытных фиксаторов изучалось путем моделирования их взаимодействия с
электролитом, имитирующим жидкую биосреду, при помощи
стандартной лабораторной установки. Оценка коррозионного поведения поверхности
фиксаторов производилась по величине установившегося электродного потенциала Ес,
поскольку он характеризует термодинамическую устойчивость поверхности в данных
условиях электрохимической коррозии.
Опытный
фиксатор в качестве рабочего электрода (Р.Э.) размещался в измерительной
электрохимической ячейке, заполненной электролитом, состав которого моделировал
плазму крови и тканевую жидкость организма. Он представлял физиологический
раствор 0,9% NaCl в дистиллированной воде с величиной рН=7,4. Температуре электролита придавались значения 25,
30, 35, 40, 450С, чем моделировалась область нормальной температуры
организма с выходом за ее пределы для установления температурной зависимости
величины потенциала. Измерение
коррозионного потенциала поверхности опытных остеофиксаторов
выполнялось относительно хлорсеребряного электрода сравнения (Э.С.) после
выдержки в электролите в течение 2 мин для стабилизации величины потенциала.
Указанная методика применялась для измерения потенциалов поверхности
фиксаторов, полученной различной обработкой, характеризующей серии: 1 –
токарная обработка; 2 – пескоструйная обработка; воздушно-термическое оксидирование
при температурах: 3 – 4000С; 4 – 5000С; 5 – 6000С;
6 – 7000С; 7 – паротермическое
оксидирование при температуре 5500С.
Потенциалы измерялись до и после клинических испытаний фиксаторов в
костных сегментах лабораторных животных.
Результаты исследования. Коррозионное поведение поверхности фиксаторов серии 1, изготовленных
с применением токарной обработки, до выполнения клинических испытаний
характеризовалось небольшими отрицательными значениями потенциала. С ростом
температуры электролита потенциалы несколько уменьшались от – 0,095 В до –
0,058 В (рис). Применение пескоструйной обработки фиксаторов серии 2 вызывало
заметное уменьшение величины отрицательных потенциалов, которые изменялись от –
0,085 В до – 0,042 В. Небольшие отрицательные потенциалы поверхности фиксаторов
обеих серий свидетельствуют об их невысокой электрохимической активности и
определенной коррозионной стойкости. Это связано, по-видимому, с наличием
защитных свойств естественной очень тонкой пленки сложного оксида Fe и Cr, образующейся на стальных фиксаторах
при действии воздуха. Пескоструйная обработка создавала лучшую микрошероховатость и окисляемость
поверхности, с ростом температуры электролита могло происходить уплотнение оксидной
пленки, что формировало уменьшение отрицательных потенциалов.
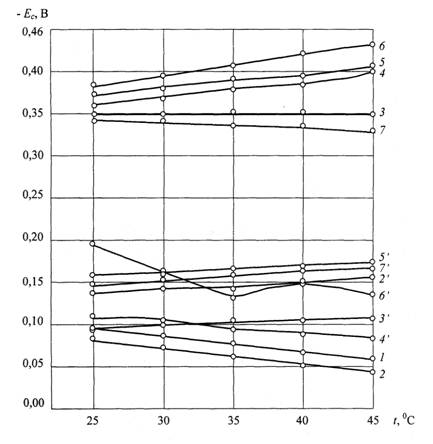
Рис. Влияние вида обработки
поверхности фиксаторов и температуры электролита на изменение коррозионных
потенциалов: 1 – токарная обработка; 2 – пескоструйная обработка;
3, 4, 5, 6 – воздушно-термическое оксидирование при 4000С,
5000С, 6000С, 7000С соответственно; 7 –
паротермическое оксидирование (штрихом обозначены
температурные зависимости потенциалов поверхностей после клинических испытаний
фиксаторов)
Воздушно-термическое
оксидирование фиксаторов приводило к образованию покрытий с потенциалами более
отрицательными в сравнении с фиксаторами до оксидирования (рис). Такой сдвиг
потенциалов объясняется, вероятнее всего, повышенной толщиной оксидных
покрытий, из-за чего происходят рост внутренних напряжений и числа микронесплошностей структуры, а также высоты микронеровностей. В таких условиях обычно возрастает
электрохимическая активность поверхности с увеличением отрицательного
потенциала. По этой же причине, возможно, происходит повышение отрицательных
значений потенциала покрытия с ростом температуры оксидирования фиксаторов
серии 3, 4, 5, 6 от – 0,349 В при температуре 4000С до – 0,435 В при
температуре 7000С. Такое же влияние нагрева электролита на снижение
потенциала поверхности может быть связано с увеличением подвижности ионов в
электролите и активизацией электродных процессов. Покрытие фиксаторов серии 3,
полученное при температуре оксидирования 4000С, обладало наименьшим
отрицательным потенциалом, равным – 0,349 В, который почти не изменялся с нагревом
электролита. Это обусловлено наилучшим сочетанием толщины и плотности данного
вида покрытия, что придает ему повышенную электрохимическую устойчивость.
Паротермическое оксидирование создавало на
поверхности фиксаторов серии 7 покрытие, минимальный отрицательный потенциал
которого составлял – 0,332 В и был меньше потенциала покрытий, полученных воздушно-термической
обработкой. Повышение температуры электролита оказывало небольшое влияние на
изменение потенциала. Возможным объяснением этого служат повышенная структурная
плотность парооксидного покрытия и улучшенная микрошероховатость поверхности.
Коррозионное поведение поверхности фиксаторов после проведения клинического
исследования отличалось значительным смещением коррозионного потенциала в
положительную сторону за исключением неоксидированных
фиксаторов серий 1 и 2.
Прошедшие токарную обработку фиксаторы серии 1 приобрели потенциал, мало зависящий от температуры электролита, средней величиной – 0,160 В. Это на – 0,065 В более отрицательное значение, чем самый отрицательный потенциал фиксатора до клинического исследования. Фиксаторы серии 2 имели среднюю величину потенциала, равную – 0,149 В, что было на – 0,064 В меньше самого отрицательного потенциала до клинического эксперимента. Полученный сдвиг потенциала в отрицательную сторону может быть объяснен возможностью повреждения тонкой естественной пленки оксидов, имеющей катодный характер, при вворачивании фиксаторов с воздействием в течение 45 суток биожидкости на данную пленку.
Воздушно-термическое оксидирование фиксаторов серий 3 и 4
при температурах 400 и 5000С обеспечило получение положительного
сдвига потенциала покрытий в среднем на 0,247 В и 0,284 В соответственно;
покрытие на фиксаторах серии 5, полученное при температуре 6000С
дало средний положительный сдвиг потенциала на 0,228 В. Температура
оксидирования 7000С фиксаторов серии 6 создавала повышенные
внутренние напряжения и малопрочное покрытие с
положительным сдвигом потенциала в среднем на 0,259 В. Это можно объяснить
появлением на поверхности оксидного покрытия пленки белковых структур, имеющей
защитные свойства.
Паротермическое оксидирование фиксаторов серии 7 формировало покрытие, у
которого коррозионный потенциал стал более положительным в среднем на 0,185 В
(рис). Это может быть связано с теми же причинами, которые были приведены выше
при анализе поведения фиксаторов серии 6 с оксидным покрытием, полученным
воздушно-термической обработкой при температуре 7000С.
На основе представленных результатов можно сделать вывод, что технологический режим и условия термического оксидирования стержневых остеофиксаторов из стали 12Х18Н9Т оказывают существенное влияние на электрохимическую активность и адапционную способность оксидных покрытий при лабораторных и клинических исследованиях.
Для проведения чрескостного остеосинтеза рекомендуется применять фиксаторы из стали 12Х18Н9Т с оксидными покрытиями, полученными воздушно-термическим оксидированием при температурах 400 и 5000С, обладающие наибольшей коррозионной стойкостью в биосредах, высокими качествами биоинтеграции и возможностью эффективной адаптации к костным, мягким, а также жидким структурам организма.
Литература
1. Илизаров Г.А. Значение факторов напряжения растяжения в генезе тканей и формообразовательных процессов при чрескостном остеосинтезе // Чрескостный остеосинтез в ортопедии и травматологии: сб. научн. тр. – Курган, 1984. Вып. №9. С. 4-41.
2. Аболина А.Е., Абрамов М.Л., Морозов В.П. Чрескостный компрессионно-дистракционный остеосинтез при лечении переломов плеча, бедра, голени и их последствий // Метод Илизарова – достижения и перспективы. – Курган, 1993. С. 40-41.
3. Анников В.В., Бейдик О.В. Внешняя стержневая фиксация переломов трубчатых костей собак и кошек: Уч. пособие. – Саратов, 2006. 30 с.
4. Бейдик О.В., Бутовский К.Г., Островский Н.В., Лясников В.Н. Моделирование наружного чрескостного остеосинтеза. – Саратов: Изд-во СГМУ, 2002. – 198 с.
5. Родионов И.В., Бутовский К.Г., Анников В.В., Хапрова Т.С. Поверхностно-структурные характеристики термооксидных биопокрытий остеофиксаторов из стали 12Х18Н9Т / Сб. докладов 2-го Междунар. научно-технического симпозиума «Наноструктурные функциональные покрытия и материалы для промышленности» Харьковской нанотехнологической ассамблеи – 2007. Т.1. Наноструктурные материалы. Украина, Харьков, 2007. С. 139-145.
6. Родионов И.В., Бутовский К.Г., Серянов Ю.В. Формирование оксидных биопокрытий на титановых чрескостных
фиксаторах в электролите для совмещенного анодного обезжиривания и
оксидирования / Материалы Всеросс. научно-практич. конф. «Новые
технологии создания и применения биокерамики в
восстановительной медицине». Томск: Изд-во ТПУ, 2007.
С. 97-103.