Экология/2. Экологические и метеорологические
проблемы больших городов и промышленных зон
Мырзахметова Б. Б., Калменова А. К., д.т.н. Бестереков У.
Южно-Казахстанский государственный
университет им. М.Ауезова, Казахстан
Переработка фосфогипса на серную
кислоту и известь
Несмотря на
большое число предложенных и разработанных технологических процессов, степень
утилизации фосфогипса в мировой практике, все еще остается низкой [1].
Известные на сегодня
методы использования фосфогипа можно разделить на две группы [2,3]:
- Методы
не требующие предварительной обработки фосфогипса перед использованием (за
исключением подсушки). Эксплуатационные и капитальные затраты на
осуществление этих методов незначительны. К этой группе относятся использование
фосфогипса в качестве добавок при производстве портландцемента и гипсование солонцов
взамен природного гипса в сельском хозяйстве.
- Методы термического разложения фосфогипса. При этом осуществляется термическое
разложение фосфогипса на основные составляющие компоненты. Эти процессы требуют
сравнительно сложного аппаратурного оформления и, следовательно, сопровождаются
значительными эксплуатационными затратами.
Несомненно, первая группа
методов привлекательна простотой реализации и меньшей капиталоемкостью. Однако
эти методы при всей их экономичности могут решить проблему утилизации
фосфогипса лишь частично. Кроме того современные экологические требования не допускают непосредственное использование
фосфогипса в вышеуказанных целях.
В этой связи, на наш взгляд,
наиболее приемлемым, несмотря на более высокую стоимость, представляется вторая
группа методов. Одним из таких способов является термическое разложение
фосфогипса с получением извести и сернистого газа. Здесь, в отличии от
известных способов, в процессах переработки фосфогипса в целевые продукты используется
сильный окислитель – озон. Химизм имеющих место при этом процессов может быть
представлено нижеследующим образом:
CaSO4.2H2O = CaSO4
+2H2O (1)
CaSO4=
CaO +SO2 –Q (2)
Расчеты показывают, что выделяющейся
при разложений фосфогипса по реакций воды достаточно для образования серной
кислоты по реакции:
SO2+O3 +Н2О = H2SO4+O2 (3)
Результаты расчетов термодинамической
вероятности протекания реакций (3), приведены в таблице 1.
Таблица 1 – Изменение энергии Гиббса
с температурой.
|
Т,К |
298 |
400 |
500 |
600 |
700 |
800 |
900 |
1000 |
|
∆G, кДж/моль*К |
-233,71 |
-231,23 |
-228,94 |
-226,73 |
-224,58 |
-220,44 |
-219,98 |
-218,40 |
Проведены экспериментальные
исследования в лабораторных условиях по нижеследующей методике:
Предварительно взвешенный
фосфогипс помещают в лодочку 2. Затем лодочку 2 помещают в трубчатую обжиговую
печь 1 во внутрь кварцевой трубки, имеющей входные и отводные концы. Отводной
конец кварцевой трубки плотно закрывается термостойкой пробкой с отверстием,
куда вставляется стеклянная трубка, подключенная к водяному холодильнику 4, к
которому имеется также линия подвода озона газообразного, получаемого в
озонаторе 3. В трубчатой печи 1 фосфогипс подвергается термическому разложению
при Т=1200оС. Образующиеся при этом газообразные продукты в виде SO2 и паров воды, совместно с
газообразным озоном отсасываются водяным насосом 5, устанавливаемым после
холодильника 4. После холодильника 4 конденсат серной кислоты отделяется от
отходящих газов в каплеулавителе и собирается в сборнике кислоты 6. По мере
завершения опытов обожженный фосфогипс анализируется на содержание СаО, а
исходное сырье – на выход SO2 и СаО. В каждом конкретном случае также устанавливается выход
серной кислоты и ее концентрация. Схема экспериментальной установки приведена
на рисунке 1.
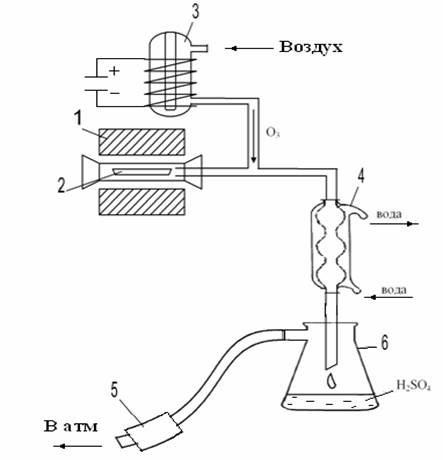
1 – трубчатая печь; 2 – лодочка с
фосфогипсом; 3 – озонатор;
4 – холодильник; 5 – водоструйный
насос; 6 – сборник серной кислоты.
Рисунок 1 – Схема экспериментальной установки получения
серной кислоты и извести из фосфогипса
На рисунках 2 и 3 показано
влияние температуры, продолжительности обжига на степень разложения фосфогипса
(выход активного СаО).
Рисунки 4 и 5
иллюстрируют влияние температуры,
продолжительности обжига на степень выделение
SO2.
Из графика видно, что при повышении температуры обжига до 1100 оС
выход SO2
достигает 75%.
![]()

Рисунок 2 – Влияние продолжительности обжига на степень разложения фосфогипса
![]()
![]()
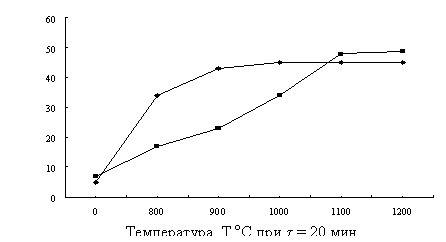
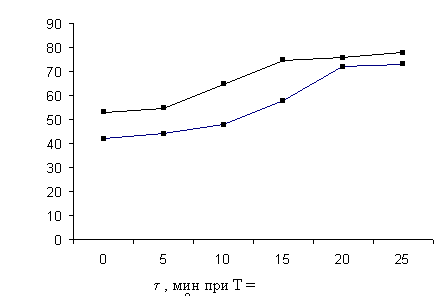 Рисунок 3 – Влияние температуры обжига на степень разложения фосфогипса
Рисунок 3 – Влияние температуры обжига на степень разложения фосфогипса
Рисунок 4 – Влияние продолжительности
обжига на степень выделения SO2
![]()
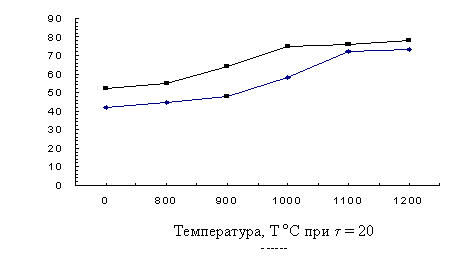
Рисунок 5 – Влияние температуры
обжига на степень выделения SO2
Результаты анализа серной
кислоты приведены в нижеследующей таблице 2.
Таблица 2 – Результаты анализа серной
кислоты
|
Навеска фосфогипса, г |
Выход SO2, г |
Выход Н2SO4, г |
Концентрация Н2SO4, % |
|
2,05 |
0,510 |
0,790 |
84,62 |
|
22,18 |
0,548 |
0,755 |
83,36 |
|
2,25 |
0,565 |
0,771 |
83,13 |
На основе проведенных
исследовании можно сделать следующие обобщения и вывод:
1.
Разработана
новая технология переработки фосфогипса, позволяющая получить в качестве
конечных целевых продуктов известь и серную кислоту.
2.
Данная
технология способствует высокоэффективному решению серьезнейшей экологической
проблемы и имеет важное прикладное значение.
Литература:
1. Мырзахметова Б.Б,
Калменова А.К, Бестереков У.Б. Анализ состояния современного уровня технологии
переработки фосфогипса в целевые продукты// Труды ЮКГУ-2007, том10
2. Наркевич И.П,
Печковский В,В. Утилизация и ликвидация отходов в технологии неоганических
веществ.- М.: Химия, 1984.-240с.
3. Фосфогипс и его
использование / Иваницкий В.В., Классен П. В, Новиков А. А и др.-М.: Химия,
1990.