Фундаментальные проблемы создания новых
материалов и технологий.
Кічура Д. Б., Яхура Ю. Б., Каспришин Н. М.
Національний
університет ²Львівська
політехніка²,
вул. С.Бандери,
12, м. Львів, 79013 Україна Е-mail: chaykivskyy@polynet.lviv.ua
Екологічні аспекти Утилізації побічних продуктів спиртового виробництва з
метою синтезу моноестерів на основі фталевого ангідриду
Сьогодні вітчизняна спиртова
промисловість за рік може випускати більше 60 млн. дал спирту. Ставиться
завдання покращити якісні показники спирту, знизити їх собівартість та
підвищити ефективність переробки побічних продуктів. Пошук нових функціональних
мономерів з підвищеною міцністю, термостійкістю та сумісністю є надзвичайно
актуальним. Перспективним
шляхом утилізації сивушної олії (СО), яка містить спирти С2 – С5 є одержання моно- та
диестерів. В склад СО входить ряд спиртів нормальної та ізобудови, таких як: етиловий
(ЕС), пропіловий (ПС), ізо-бутиловий (і-БТ) та ізопентиловий (і-ПС). Актуальність і практичне значення
експериментальних досліджень пов’язане з впливом вихідної сировини на процес
синтезу естерів, їх структуру, а також фізико-механічні та хімічні
характеристики композитів, які можна отримати на їх основі.
Метою роботи було визначення впливу будови індивідуального
спирту на синтез моноестерів на основі фталевого ангідриду (ФА) шляхом конденсації з відповідним
спиртом. Застосовували індивідуальні спирти, що входять у склад СО, які
попередньо висушували прожареним сульфатом міді та очищали дистиляцією, згідно
відомих методик. Взаємодію спиртів проводили з ФА, який широко використовується
як мономер у поліконденсаційних процесах, має високу реакційну здатність.
Синтезовані моноестери можуть використовуватися як вихідна сировина для
отримання нових поліконденсаційних смол, а також самостійно як твердники.
Співвідношення вихідних реагентів ФА : спирт =1 : 1…3 (мол.) інтервал температур 333…373
К. Основними фізико-хімічними показниками, що характеризували відповідний
моноестер є кислотне число, число омилення, молекулярна маса.
Кислотне число є важливою хімічною характеристикою, що вказує
на вміст у сполуці карбоксильних груп. Оскільки температура кипіння етанолу 351
К, то досліджуваний інтервал темеператур знаходився в межах 333…353 К. Як видно
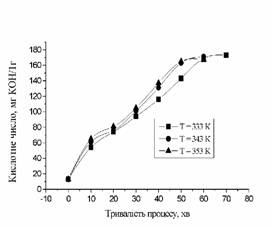
з рис.1 в початковий момент часу, коли реакційна суміш нагрілась до температури
реакції кислотне число становить 13 мг КОН/г. Так для температури 333 К має
місце прямопропорційне підвищення кислотного числа з плином самого процесу. За
перші 10 хв часу в температурному інтервалі 333…353 К кислотне число зростає
найбільше в середньому на 40…52 мг КОН/г. Через 10 хв проведення процесу
кислотне число збільшується в середньому на 15…20 мг КОН/г. Після 30 хв при 333
К кислотність збільшується на 20…29 мг КОН/г. Підсумовуючи експериментальні
дослідження зображені на рис. 1 – 4 видно, що при температурі процесу 353К процес триває в
середньому 70 … 80 хв, для
343 і 353 К на 10 хв довше.
|
Рис. 1. Залежність кислотного
числа моноетанолфталату від температури та тривалості процесу |
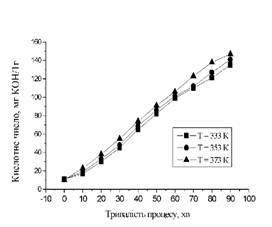
Рис. 2. Вплив тривалості процесу
та температури на кислотне число монопропанолфталату |
З експериментальних досліджень видно, що підвищення
температури реакції призводить до збільшення кислотного числа, що говорить про
накопичення в реакційній масі моноестеру. Використовують надлишок ангідриду,
оскільки при використанні співвідношення ФА : спирт = 1 : 1 (мол.) конверсія ФА
не перевищує 45 %. Загалом ж підвищення температури процесу, призводить до
зменшення його тривалості.
Для пропанолу отримуємо прямопропорційний впилив тривалості
процесу та його температури на кислотне число моноестеру. При температурі 333 К
до 70 хв проведення конденсації кислотне число зростає в середньому на 6…19 мг
КОН/г, подальша тривалість процесу хоча сприяє підвищенню кислотного числа, але
підвищення кислотності зменшується і складає в середньому 15…17 мг КОН/г.
Підвищення температури до 373 К не призводить до значних змін у значеннях кислотних
чисел, як видно з рис. 2. Єдине, що максимальна ступінь перетворення ФА має місце при
температурі 373 К, процес завершується на 90 хв. Вміст карбоксильних груп
коливається в межах від 1 до 12,9 % мас.
|
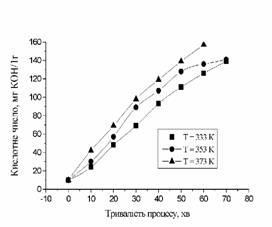
Рис. 3. Залежність кислотного
числа моноызобутанолфталату від температури та тривалості процесу |
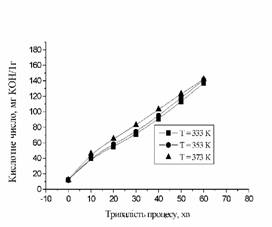
Рис. 4. Вплив тривалості процесу
та температури на кислотне число моноізопентанолфталату |
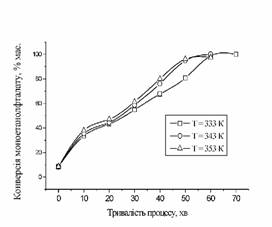
Підсумовуючи проведення експериментальні конверсію визначали
для етанолу та ізоамілового спиртів, оскільки їх є найбільше у СО. Для ЕС при
температурі 333, 343 К спостерігається підвищення конверсії ФА за перші 10 хв
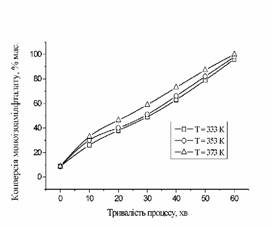
на 25…30 %, а далі конверсія зростає в середньому на 15 %, (див. рис. 5). Для і-ПС конверсія найбільше зростає у перші 10
хв проведення процесу (див.
рис. 6), наступні 20…40 хв
спостерігається прямопропорційна залежність зростання конверсії, далі з 50 хв підвищення конверсії гальмується.
|
Рис. 5. Залежність конверсії моноетанолфталату від тривалості
процесу |
Рис. 6. Вплив тривалості та температури на конверсію
моноізопентанолфталату |
Як видно з проведених експериментальних досліджень значення
функціональних чисел зменшуються зі збільшення молекулярної маси відповідного
моноестеру. Вміст карбоксильних груп зменшується з підвищення молекулярної маси з 13,8
до 11,3 % мас., спадає
також кислотне число – 171 … 142 мг КОН/г та число омилення – 289 … 237 мг КОН / г. Отже, ФА можна застосовувати для одержання моно- та диестерів на основі спиртів СО. Синтезовані моноестери є твердими речовинами з характерним запахом. Ці естери
можуть бути сировиною для парфумерної промисловості та виробництва миючих
засобів, оскільки вони мають освіжаючі та дезинфікуючі властивості. А також як мономери чи
пластифікатори в органічних синтезах та хімії високомолекулярних
сполук.