К.т.н.
Колесников А.С., д.т.н., Капсалямов Б.А., Аринова Д. Б., Колесникова О.Г.,
Ралдыгин К.А.
РГКП «ЮКГУ им. М. Ауезова», Шымкент, Казахстан
Реакционная
способность восстановителей по отношению к ZnO
При
переработке Zn-
содержащих материалов вельцеванием образуется до 0,89 т клинкера на т сырья. В
клинкере от вельцевания различных материалов содержание Fe составляет от 20 до 32 % и углерода 15-20%. О
возможности присутствия Fe3C в клинкере вельцевания говорится в работе [1]. В
клинкере вельцевания (несмотря на то, что Fe3C устойчив при Т>1000К) в виду малой скорости распада, он может быть
единственным продуктом восстановления оксидов и находиться довольно долго в
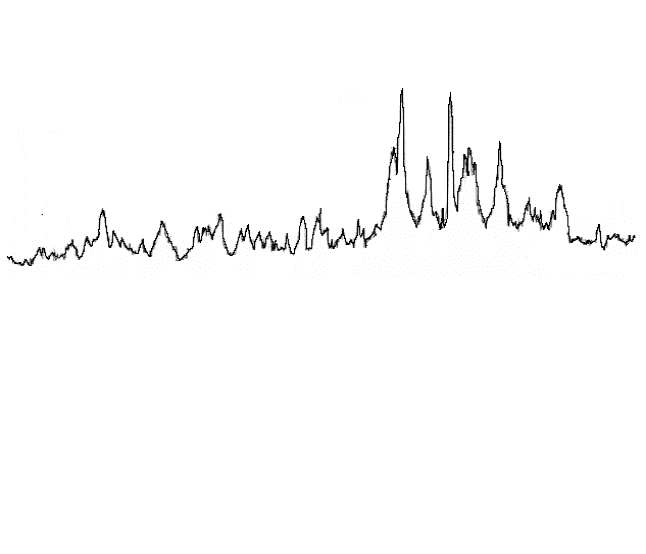
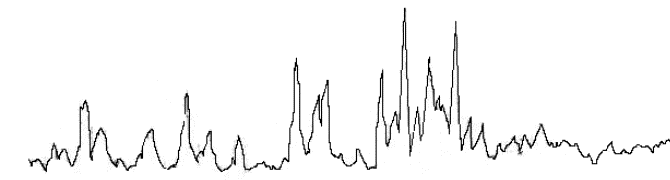
неразложившемся состоянии при Т<1000К. На рисунке 1 приведена
рентгенограмма клинкера из старых отвалов
и свежеобразовавшегося, из которого следует, что железо в клинкере
присутствует в виде элементного, Fe3C, FeО и Fe2О3.
При коллективной переработке клинкеров
вельцевания
восстановительно-возгоночным методом, с восстановлением Zn и переводом его в возгоны важно определить
реакционную способность Fe3C по отношению к ZnО. С этой целью было проведено термодинамическое
моделирование восстановления ZnО с
использованием программного комплекса «Астра-4» [4] в системах ZnО-С, ZnО-СО, ZnО-Н2,
ZnО-СН4, ZnО-Fe, ZnО-SiC, ZnО-Fe3Si и ZnО-Fe3C. Алгоритм многоцелевого программного комплекса
«Астра-4» основан на универсальном термодинамическом методе определения
характеристик равновесия поликомпонентных систем на основе фундаментального
принципа максимума энтропии. Эффективность использования комплекса «Астра-4», включающего в свою базу
данных 5547 соединений, 79 элементов, для восстановительных процессов была
показана в работах [2]. На рисунке 2 приведена информация о восстановлении Zn в рассмотренных системах в температурном интервале
интервале 900-1800К и давлении 0,1 мПа, из которого следует, что при
температуре 900К наибольшей реакционной способностью обладает SiC, затем Fe3Si.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Остальные восстановители заметно уступают
в начальной реакционной способности SiC и Fe3C. Однако и они
по температуре 1% степени восстановления образуют следующий ряд: СH4 > H2> CO> Fe3C( Fe)> Fe3C( FeО)> Fe т.е
при температуре 900К реакционная способность восстановителей изменяется в
следующей последовательности: SiC(<900К)>Fe3Si(<900К)>СH4(976К)>H2(981К)> >CO(1064К)> Fe3C(1201К Fe)>Fe3C(1202К FeО) > Fe(1452К)
6 7 2 1 3 8 4 5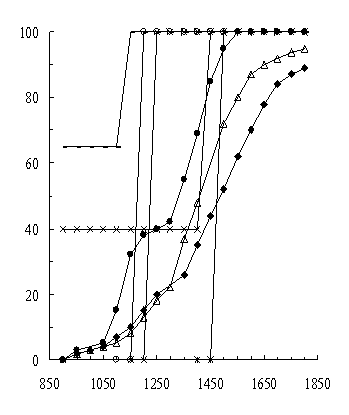
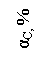
![]()

Проведенная работа по восстановлению Zn из ZnО позволяет
сделать следующие выводы: изменение начальной реакционной способности
восстановителей по отношению к ZnО изменяется в
следующей последовательности: SiC>Fe3Si>СH4>H2>CO>Fe3C>Fe; по величине минимальной температуры полного
восстановления Zn реакционная способность
восстановителей изменяется следующим образом: SiC>С> Fe3C(Fe)>Fe3C( FeО)>Fe3Si>Fe>СH4>H2>CO; карбид железа при температуре 1250К способен
полностью восстановить Zn с
образованием элементного железа, по восстановительной способности он уступает
только SiC и С.
Литература:
1 Абдеев М.А.,
Колесников А.В., Ушаков Н.Н.
Вельцевание цинк-свинец содержащих
материалов. – М.: «Металлургия», 1985, -120 с.
2 Капсалямов Б.А., Шевко В.М., Колесников А.С. Кинетика восстановления и перехода кремния в
ферросилиций из клинкеров вельцевания.// КИМС, 2007, № 2, С.36-40.