Экология/
2. Экологические и метеорологические проблемы больших городов и промышленных
зон
Д.т.н., проф. Свергузова
С.В., аспирант Ипанов Д. Ю.
Белгородский
государственный технологический университет
им. В.Г.
Шухова, Россия
К вопросу о возможности
использования пыли электросталеплавильного производства для очистки
фосфатсодержащих вод
Водные экосистемы, в которых живые компоненты
представлены водорослями, простейшими и т.д., как правило, быстро реагируют на
загрязненность [1].
Фосфаты, поступающие в водные объекты со
сточными водами, представляют серьезную угрозу для водных экосистем, поскольку
избыточное содержание фосфатов в воде вызывает усиленную эвтрофикацию вод. Одним
из худших последствий эвтрофикации является вызванное этим феноменом изменение содержания
кислорода в воде. Гидробионты испытывают серьезные трудности при жизни в таких
водных объектах, поскольку ночами весь или почти весь кислород воды растения
используют на дыхание, ничего не оставляя рыбам и другим представителям водной
фауны [2]. Поэтому разработка эффективных и недорогих способов очистки сточных
вод от фосфатов является актуальной задачей.
Нами для очистки фосфатсодержащих вод предложено
использовать отход сталеплавильного производства – пыль электродуговых
сталеплавильных печей (ЭДСП) Оскольского электрометаллургического комбината
Белгородской области (Россия).
Исходя из данных химического анализа состава
пыли ЭДСП, в ней содержится до 14 % СаО, находящегося в пыли в свободном виде и
в виде силикатов кальция типа CaSiO3 и Ca2SiO4.
Кроме того, в пыли содержатся в незначительных количествах оксиды Mg, Mn(II), Al,
Fe(II), Fe (III), Cu, Sn, Zn, Pb. При добавлении к пыли раствора H2SO4
(0,1 н) происходит растворение соединений металлов по схемам:
CaO + H2O → Ca(OH)2
MeSiO3 + H2SO4
→ MeSO4 + H2SiO3 ↓
Me2SiO4 + 2H2SO4
→ 2MeSO4 + H2SiO4 ↓
MeO + H2SO4 →
MeSO4 + H2O
Me2O3 + 3H2SO4 → Me2(SO4)3 + 3H2O
В результате, образуется суспензия, содержащая
металлы в ионном виде.
При обработке данной суспензией модельных
металл- и фосфатсодержащих растворов возможно образование малорастворимых
соединений в результате обменных реакций:
Ca2+ + PO43- → Ca3(PO4)2 ↓ Fe3+ + PO43- → FePO4↓
Mg2+ + PO43- → Mg3(PO4)2 ↓ Ni2+ + 2OH- → Ni(OH)2
↓
Mn2+ + PO43- → Mn3(PO4)2 ↓ Cu2+ + 2OH- → Cu(OH)2
↓
Al3+ + PO43-
→ AlPO4 ↓ 2Ni2+ + 2OH- →
(NiOH)2CO3 ↓
Fe3+ + PO43-
→ Fe3(PO4)2↓ 2Cu2+ + 2OH-
+ CO3 → (CuOH)2CO3 ↓
О возможности образования перечисленных осадков
можно судить по величинам их произведений растворимости (ПР) (табл.) [3].
Таблица
Произведения растворимости
|
Вещество |
ПР |
Вещество |
ПР |
|
Ca3(PO4)2 |
2,0∙10-29 |
FePO4 |
1,3∙10-22 |
|
Mg3(PO4)2 |
1,3∙10-13 |
Ni(OH)2 |
2,0∙10-15 |
|
AlPO4 |
5,75∙10-19 |
Cu(OH)2 |
2,2∙10-20 |
Образовавшийся осадок легко удалить из раствора
отстаиванием или фильтрованием.
Кроме
протекания перечисленных реакций возможна также очистка за счет
сорбционных процессов. Обоснованием такого предположения является большая
удельная поверхность пыли (64,6 м2/г) и наличие на поверхности
частиц пыли множества шероховатостей, неровностей, сколов, что свидетельствует
об энергетической неоднородности поверхности и возможных адсорбционных
свойствах пыли. Поэтому нами была исследована возможность сорбционной очистки с
помощью пыли ЭДСП.
В связи с тем, что при добавлении пыли в
модельные или реальные сточные воды происходит ее частичное растворение, часть
ионов Са2+ переход в
раствор, что делает вероятным образование малорастворимого соединения Са3(РО4)2.
Это может искажать результаты исследований процесса адсорбции ионов РО43-
на поверхности пыли. Поэтому для данной серии исследований пыль ЭДСП
обрабатывали 1,0 н HCl в течение часа, затем оставшуюся часть
пыли отмывали до нейтральной реакции. С отмытой пылью ЭДСП проводили исследования процесса адсорбции
ионов РО43-.
Определение изотерм адсорбции и десорбции в
статических условиях для фосфат-ионов (рис.) на пыли, отмытой 1 н кислотой,
показало, что процесс адсорбции ионов РО43- поверхностью
пыли протекает в незначительной степени, сорбционная емкость составляет 1,93
мг/г.
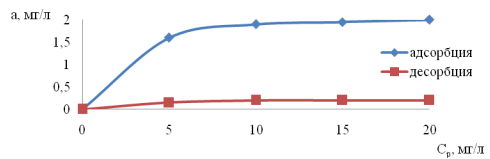
Рис. Изотермы адсорбции и десорбции ионов РО43- на поверхности пыли ЭДСП
Поскольку на изотерме адсорбции отсутствуют
перегибы, можно предположить, что на поверхности происходит формирование
моноадсорбционного слоя. Кривая десорбции расположена вблизи от оси ОХ, поэтому
можно предположить, что в данном случае имеет место как физическая, так и
химическая адсорбция.
В результате экспериментов по очистке модельных
фосфатсодержащих растворов с исходной концентрацией ионов РО43-
30 и 50 мг/л пылью ЭДСП эффективность очистки составляла 95,8 % и 98,7 %
соответственно при добавке пыли 1,5 г на 100 мл модельного раствора.
Таким образом, в работе доказана возможность
использования пыли ЭДСП для очистки фосфатсодержащих вод.
Литература
1. Водная экосистема [Электронный
ресурс]- Режим удаленного доступа: http://ru-ecology.info.
2. Почему фосфаты и нитраты
являются загрязняющими воду веществами [Электронный ресурс] - Режим удаленного
доступа: http://www.geoglobus.ru.
3. Лурье Ю.Ю. Справочник по
аналитической химии / Ю.Ю. Лурье. – М.: Химия, 1971. – 456 с.