УДК 663.764
Міськів
О.В., Нагорна С.Ю.
Дніпродзержинський
державний технічний університет, м. Дніпродзержинськ, Україна
ДОСЛІДЖЕННЯ ВПЛИВУ НА ВИХІД І КРУПНІСТЬ
сульфату амонію ТЕМПЕРАТУРИ, НАПРУЖЕНОСТІ МАГНІТНОГО ПОЛЯ, КИСЛОТНОСТІ ТА ЧАСУ
ОМАГНІЧУВАННЯ маточного розчину
Одним з
найважливіших хімічних продуктів, який отримують на коксохімічних заводах у
великій кількості, є сульфат амонію. Він широко застосовується в сільському
господарстві в якості азотного добрива. Так як добриво добре розчинюється у воді,
то легко поглинається вологою грунту. Живильною речовиною у сульфаті амонію є
азот, який засвоюється з грунту корінням рослин. Сульфат амонію є фізіологічно
кислим добривом, особливо ефективний на ґрунтах, насичених лугами (чорноземи,
сіроземи, каштанові ґрунти), а також на вапнякових підзолистих ґрунтах.
Сульфат
амонію отримують в основному з аміаку коксового газу в апараті, який
називається сатуратором. В сатураторах коксовий газ барботує через маточний
розчин, що містить вільну сульфатну кислоту [1].
Для
характеристики сульфату амонію як добрива велике значення має розмір його
кристалів. Тому питанню про отримання крупнокристалічного добрива приділяють
багато уваги. В деяких випадках для збільшення величини кристалів сульфату
амонію в маточний розчин сатуратору періодично подають коагулюючу добавку –
поліакриламід або маточний розчин піддають дії магнітного поля.
Нами вивчені
можливості дії на процес кристалізації солі таких чинників як температура та кислотність, а також напруженість
магнітного поля та часу омагнічування маточного розчину для досягнення кінцевої
мети – отримання крупнокристалічного сульфату амонію. Виготовлена лабораторна
установка моделююча промислову схему отримання сульфату амонію за сатураторним
способом (див. рис.1).
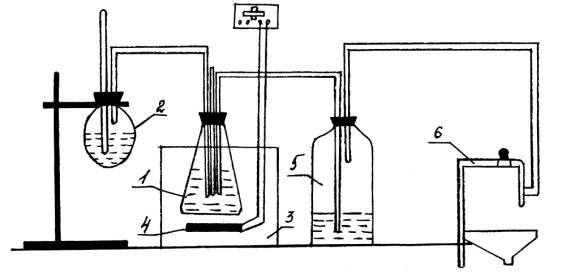
1 – нейтралізатор; 2 –
колба з розчином аміаку; 3 – термостат; 4 – нагрівач; 5 – поглинача залишкового
аміаку; 6 – патрубок вакуумної системи
Рисунок 1 – Схема
лабораторної установки для отримання сульфату амонію
Нейтралізацію насиченого маточного розчину, підкисленого сульфатною
кислотою, проводили сумішшю аміаку і повітря, яку отримували в процесі просмоктування
повітря за допомогою вакуумної системи через 25%-вий розчин аміаку. Нейтралізатор
1 встановлювали у термостат 3, у якому за допомогою нагрівача підтримували задану
температуру. Перед завантаженням суміші в нейтралізатор її піддавали магнітній обробці
при різних напруженості магнітного поля та часу омагнічування на апараті УЕМ-1Т
(універсальний електромагніт).
У ході проведення дослідів виконали ряд визначень, а
саме, кислотність маточного розчину, концентрацію розчинів сульфатної кислоти
(фільтрату) й аміаку до і після експерименту за відомими методиками, прийнятими
при поточному контролі якості хімічних продуктів коксування [2].
В процесі досліджень провели шість серій дослідів,
які відрізняються один від одного різними
чинниками.
Результати дослідів наведені у таблицях 1.
Таблиця 1 – Залежність гранулометричного складу сульфату
амонію від часу обробки маточного розчину в магнітному полі
|
Найменування показників |
Час омагнічування, хв. |
|||||
|
не ом. |
5 |
10 |
15 |
20 |
25 |
|
|
1. Температура проведення досліду, °C |
52 |
50 |
48 |
46 |
46 |
44 |
|
2. Кислотність маточного розчину, % |
4,9 |
4,8 |
4,8 |
4,7 |
4,7 |
4.6 |
|
3. Маса отриманої солі, г |
14,9 |
19,7 |
35,7 |
32,9 |
32,8 |
24,8 |
|
4. Гранулометричний склад, %, класи, мм > 1 мм 0,2 – 1,0 мм 0,16 – 0,2 мм 0,1 – 0,16 мм < 0,1 мм |
11,5 6,7 19,6 23,9 38,3 |
19,8 9,6 17,9 21,4 31,3 |
26,8 15,1 22,1 16,4 19,6 |
25,2 14,8 21,3 16 22,7 |
24,8 13,9 20,1 15,7 25,5 |
21,3 13,1 19,9 15,6 30,1 |
Аналіз даних,
представлених в таблиці 1 і на рисунках 2, 3, 4 та 5, дає підстави
стверджувати, що досліждувані умови, а саме: інтенсивність магнітної обробки, час
омагнічування маточного розчину, кислотність маточного розчину та температурний
режим впливають на процес отримання сульфату амонію, зокрема, його
кристалізацію.
Розглядаючи
характер зміни розподілу вузьких класів крупності сульфату амонію отриманого з
необробленого та обробленого в магнітному полі різної напруженості маточного
розчину, також можна зробити певний висновок.
Сульфат
амонію, отриманий з неомагніченого маточного розчину, представлений в основному
класами крупності 0,16-0,1 мм і менше, при цьому в ньому міститься
відносно велика кількість тонкодисперсних класів менше 0,1 мм,
що є небажаним, оскільки збільшує злежуваність продукту і утрудняє внесення
його в ґрунт.
При цьому магнітна
обробка маточного розчину у всіх досліджуваних випадках сприяє збільшенню
вмісту найкрупніших класів і зменшенню тонкодисперсних. Найкрупніші кристали
сульфату амонію отримані
при обробці магнітним полем напруженістю 8∙104 – 16∙104
А/м та часу дії 10 – 20 хв. відповідно (рисунки 2 та 3).
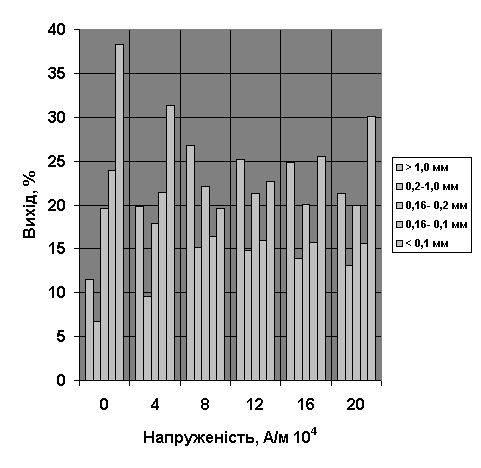
Рисунок 2 – Залежність
фракційного виходу кристалів сульфату амонію від напруженості магнітного поля
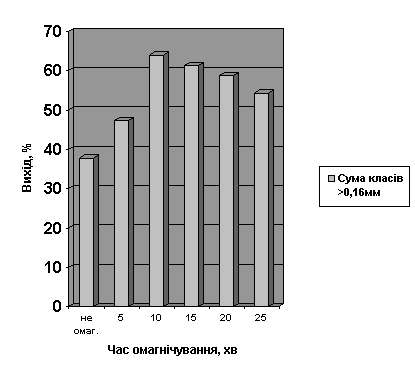
Рисунок 3 – Залежність
виходу крупних фракцій кристалів сульфату амонію більше 0,16 мм в залежності від часу омагнічування
Звертає увагу
на себе також той факт, що при зниженні температури утворення сульфату амонію
збільшується маса отриманої солі. Зіставляючи абсолютні величини цих показників
в сульфаті амонію, отриманого за традиційною технологією (без омагнічування
маточного розчину) і при омагнічуванні (діапазон зміни тривалості 5 – 25 хв. при напруженості від 4∙104 до 20∙104
А/м відповідно) видно, що в першому
випадку температура випадіння кристалів в осад склала 52 ºC і при цьому утворилося 14,9 г солі, а у другому – температура знижувалась з 50 ºC до 44 ºC, а маса утвореного сульфату амонію збільшувалась з 19,7 до 35,7
г. Потрібно відмітити, що найбільшу
масу сульфату амонію (35,7 г),
отримано за температури
48 °C, кислотності маточного
розчину 4,8 % і напруженості
магнітного поля 8∙104 А/м. Схожі
результати, але з дещо меншою масою солі – 32,9 і 32,8 г – було отримано при обробці маточного
розчину 12∙104 і 16∙104 А/м відповідно. Кислотність при цьому склала 4,7 %, а температура підтримувалась в
межах 46 ºC. Вказаний ефект є
позитивним, так як температура – це один з вагомих факторів, який впливає на
якість та вихід сульфату амонію.
Кислотність
під час проведення дослідів підтримувалась в межах 4-5%.
Таким чином,
для отримання бажаної крупності кристалів сульфату амонію в досліджуваному
діапазоні зміни напруженості обробка маточного розчину в магнітному полі
повинна проводитися в межах напруженості 8∙104 – 16∙104
А/м. Цей висновок співпадає з
діапазоном зміни температури, часом обробки розчину і масовим виходом добрива.
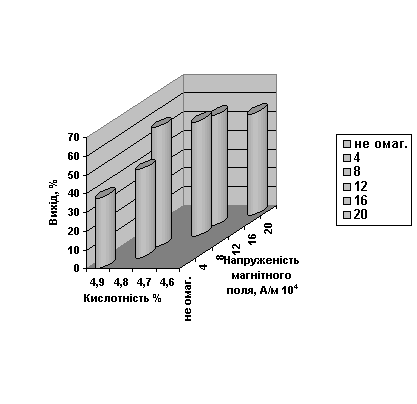
Рисунок 4 – Залежність крупності
кристалів сульфату амонію від кислотності маточного розчину
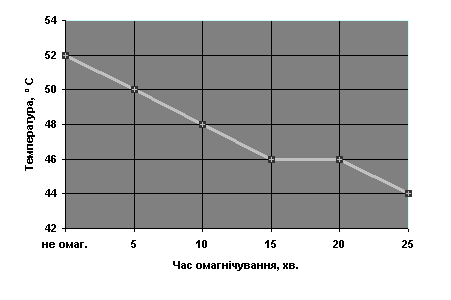
Рисунок 5 – Кінетика зниження
температури в реакторі при збільшенні часу омагнічування
Список літератури:
1.Лейбович Р.Е., Яковлева Е.Н., Филатов А.Б. Технология
коксохимтческого прозводства. Изд. 3-е, перераб. и доп. М.: «Металлургия»,
1974. – 360с.
2.Розрахунки в
технології азотних та фосфорних добрив / Уклад. М. Д. Волошин, Зеленська Л. О.,
Астрелін І. М. – Дніпропетровськ: Системні технології, 2003. – 314с.