Химия и химическая технология / Органическая химия
Сычева Е.С.,
Асылханов Ж.С., Сактаганов А.Е.,
Курманкулов
Н.Б., Ержанов К.Б.
АО «Институт
химических наук им. А.Б. Бектурова», Казахстан
Синтез и химические модификации
1,5-ди(проп-2-инилокси)нафталина
Создание новых высокоэффективных
синтетических биологически активных веществ для медицины и сельского хозяйства
является актуальной задачей для Казахстана в связи с необходимостью внедрения и
развития высокотехнологичных наукоемких производств в этих областях. Широкие
возможности решения этой проблемы даёт развитие химии ацетиленовых соединений.
Несмотря на огромные достижения в этой области, химия ацетиленовых соединений
привлекает исследователей разнообразием возможностей использования их в
разработке новых полифункциональных производных, перспективных в качестве
биологически активных веществ.
Ароматические моно- и дипропаргиловые
эфиры находят применение в сельском хозяйстве в качестве высокоэффективных гербицидов против злаковых сорняков [1-3] и фунгицидов в борьбе с болезнями и вредителями [4-7]. В
медицинской практике этот класс соединений используется в качестве
антигликемических средств [8, 9], а некоторые Csp-аминометилированные пропаргиловые эфиры проявляют
противоопухолевую активность [10].
Для синтеза новых соединений в
ряду диацетиленовых ароматических производных в качестве исходного синтона взят
1,5-дигидроксинафталин. Синтез 1,5-ди(проп-2-инилокси)нафталина (1) осуществили взаимодействием
1,5-дигидроксиоксинафталина с бромистым пропаргилом в различных средах. В
ацетоне выход целевого продукта составил 58 %, а в ДМСО/KOH – 63 %. Наибольший выход 1,5-ди(проп-2-инилокси)нафталина (1) был достигнут в системе ДМФА/K2CO3 (70 %).
Наличие в ИК спектре дипропинилоксинафталина (1) характеристических полос
поглощения в области валентных колебаний ≡С-Н
концевой ацетиленовой связи в виде узкого интенсивного пика при 3275 см-1,
тройной С≡С-связи – в виде слабоинтенсивного пика при 2130 см-1
может служить первичным доказательством его строения.
Однозначный ответ о структуре
синтезированного соединения (1) дают данные спектров ЯМР 1Н и 13С.
В ЯМР 1Н спектре в СDCl3 присутствуют следующие характерные сигналы: ацетиленового протона в виде триплета при 2,54 м.д. (J НН 2,06 Гц), протонов оксиметиленовой группы при 4,87
м.д. в виде дублета (J
НН 2,06 Гц) и протонов нафталинового кольца H2H6 при 6,97 м.д. в виде дублета с константой
спин-спинового взаимодействия (J
НН 7,56 Гц), H3H7 при 7,38
м.д. в виде триплета (J
НН 8,24 Гц), H4H8 при 7,90
м.д. в виде дублета (J
НН 8,47 Гц). Особенностью спектра ПМР
1,5-дипропаргилового нафталина (1) является некоторое упрощение сигналов
протонов нафталинового кольца за счет их совпадения. Это объясняется наличием
оси симметрии 2-го (n=2) порядка обсуждаемой молекулы.
Спектр ЯМР 13С также имеет характерные значения химических сдвигов:
атомы ацетиленовых углеводородов дают резонансные сигналы при 75,69 и 78,69
м.д. и располагаются рядом с триплетом от дейтерированного хлороформа, сигналы
оксиметиленовые атомы углерода проявляються при 56,26 м.д., а сигналы
ароматических углеродных атомов расположены в самой слабопольной части спектра
при 153,20 м.д. (С1С5), 106,44 м.д. (С2С6),
125,22 м.д. (С3С7), 115,34 м.д. (С4С8),
126,86 м.д. (С9С10).
С целью
определения реакционной способности ацетиленового водорода в дипропинилоксинафталине (1) в реакции Манниха
и получения новых ди(аминобутинилокси)нафталинов (2a,b) с потенциальной биологической активностью
изучено взаимодействие дипропинилоксинафталина (1) с параформом и вторичными аминами (пиперидином, морфолином) в среде сухого
диоксана при температуре 60 оС. В результате реакции выделены
1,5-бис(4-пиперидилбут-2-инилокси)нафталин (2а) (82%) и
1,5-бис(4-морфолинобут-2-инилокси)нафталин (2b)
(50%).
Для получения
новых диацетиленовых ароматических спиртов проведены реакции дипропинилоксинафталина (1) с циклогексаноном и N-метилпиперидоном
в условиях реакции Фаворского. Синтезы диацетиленовых гликолей (3a,b) проводили
в среде сухого эфира в присутствии 4-х кратного избытка KOH при
комнатной температуре. Получены
1,5-ди(3-(1-гидроксициклогекс-1-ил)проп-2-инилокси)нафталин (3а) и
1,5-ди(3-(1-метил-4-гидроксипиперидин-4-ил)проп-2-инилокси)нафталин (3b) с выходами
50% и 80% соответственно.
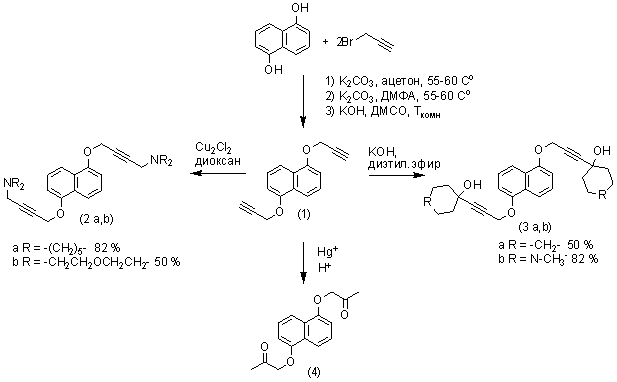
В продолжение работ по изучению реакционной
способности тройной углерод-углеродной связи диацетиленового производного
нафтола осуществлена гидратация дипропинилоксинафталина
(1) в уксусной и в серной кислотах. В обоих
случаях протекает гидратация тройной связи с образованием кетоэфира (4). В системе HgO/CH3COOH выход целевого продукта составил 42%, а в среде 7%-ой
серной кислоты в присутствии ионов ртути (II) и метанола – 19%.
Появление в ИК спектре характеристической полосы поглощения карбонильной группы при 1719 см-1, в спектре ЯМР 1Н – резонансных сигналов оксиметиленовых протонов – при 5,75 м.д., метильной группы – при 1,27 м.д., а также в спектре ЯМР 13С сигнал при 206,06 м.д. (С=О) доказывает образование 1,5-ди(2-кетопропилокси)нафталина (4). При этом в спектрах отсутствуют сигналы тройной углерод-углеродной связи.
В настоящее время синтезированные соединения в виде водорастворимых дигидрохлоридов проходят испытания на антибактериальную и рострегулирующую активность.
Литература:
1. Пат.6462222 B1 США. Aminoindan
derivatives. / Опубл. 08.10.02.
2. Пат. 4985065 США. Tetrazolinone
herbicides. / Опубл. 15.01.91.
3. Пат. 4913724 США. Herbicidal
tetrazolinones. / Опубл. 03.04.90.
4. Пат. 6011064 США. Microbicidal
compositions. / Опубл. 04.01.2000.
5. Пат. 6329424 В1 США. Microbicidal compositions. / Опубл. 11.12.01.
6. Пат. 6441028 В2 США. Microbicidal compositions. / Опубл. 27.08.02.
7. Пат. 4218467 США.
8-Methoxy-3-phenyl-5-methylpropargylaminomethyl-2H-1-benzopyran-2-one and
pharmaceutical compositions containing it. / Опубл.
19.08.80.
8. Пат.
5605918 US. Anti-hyperglycemic agents – substituted thiazolidine-2,4-diones. / Опубл. 25.02.1997.
9. Пат. 5574051 US.
Certain-(3-aryl-prop-20ynyl)-5-(arylsulfonyl) thiazolydine-2,4-dione
derivatives-hyperglycemic./ Опубл.
12.11.1996.
10. Поплавская И.А. // Тезисы докл. IV Всесоюзн. Конф. По химии ацетилена и его производных.
– Баку, 1979. – Т.2. – С.188.