Химия и химические технологии / 5.
К.т.н.
Родионов И.В.
Саратовский государственный технический
университет
Разработка технологических условий анодного оксидирования внутрикостных дентальных имплантатов для создания оксидных покрытий с биоинтеграционной способностью
Введение
Успешное развитие ортопедической имплантологии связано
с использованием современных биоматериалов, имеющих
небиологическое происхождение и не вызывающих иммунных реакций организма. К
таким материалам относятся биоинертные металлы и
сплавы – Ta, Ti, Zr, Ni, TiNi, Co-Cr, Co-Cr-Ni, Co-Cr-Mo,
нержавеющая сталь 12Х18Н10Т; органические и
неорганические биоактивные полимеры – трикальцийфосфат, гидроксиапатит, фторгидроксиапатит,
стеклоуглерод, биостекла и биоситаллы, а также оксиды биоинертных
металлов [1]. С использованием данных материалов изготовляют многие внутрикостные,
в том числе дентальные имплантаты, т.е. искусственные корни зубов,
соответствующие требованиям биологической и механической совместимости с окружающими
биотканями и действующими нагрузками. Биоинертные металлы используют, как правило, для
изготовления несущей основы имплантата, служащей для размещения зубного
протеза. Органические и неорганические полимеры применяют для нанесения на
металлическую основу функциональных покрытий, обеспечивающих прочную
биомеханическую связь с костными структурами.
Наибольшее применение в производстве
дентальных имплантатов получил технический титан ВТ1-00,
обладающий требуемым уровнем биологических и механических свойств при
взаимодействии с биосредой. При этом на поверхности
титана формируют специальное биопокрытие с
определенными морфологическими качествами и фазово-структурным состоянием,
придающими имплантату высокий уровень биосовместимости. В качестве материалов таких
покрытий могут использоваться как биоактивные
полимеры, наносимые на поверхность имплантата различными методами, так и
собственный оксидный слой титана, создаваемый на поверхности с помощью анодного
оксидирования [2, 3].
Титанооксидные соединения характеризуются благоприятным сочетанием физико-механических свойств, регулируемых за счет режима оксидирования. Изменение параметров режима может придать оксидному покрытию биоинтеграционные качества, характеризующие его способность к прочной взаимосвязи с окружающими костными структурами. В то же время результаты ранее проведенных исследований не содержат сведений о свойствах анодно-оксидных покрытий, способных создать эффективную биоинтеграцию имплантатов. Поэтому целью данной работы является разработка технологических условий анодного оксидирования титановых дентальных имплантатов, придающих покрытию высокие показатели биосовместимости и биоинтеграционную способность.
Методика исследования
Объектами эксперимента являлись пластинчатые образцы
из титана ВТ1-00, имеющие площадь рабочей поверхности
200 мм2 и толщину 1 мм. Перед анодированием поверхность образцов подвергалась
предварительной пескоструйной обработке корундовым порошком в течение 8 минут
при давлении воздушно-абразивной струи 0,65 МПа. Этим
создавалась исходная микрошероховатость поверхности и
обеспечивались необходимые условия для получения морфологически гетерогенного
оксидного покрытия. В качестве электролита анодирования
использовался водный раствор, содержащий серную кислоту и добавку сульфата
меди, концентрацией компонентов 200 г/л Н2SO4 + 50 г/л CuSO4 · 5Н2О.
Добавлением сульфата меди обеспечивался ускоренный рост оксидного покрытия в
толщину и придавались антисептические биомедицинские свойства его поверхности
за счет включения частиц оксида CuО в состав титанооксидного слоя. Процесс сернокислотного анодирования пескоструйно обработанных
образцов осуществлялся в электрохимической термостатируемой
ячейке с полым кольцевым титановым противоэлектродом,
обеспечивающим получение равномерного анодно-оксидного покрытия. Эксперименты
проводились в гальваностатических условиях реализуемых с помощью источника постоянного
тока Б5-47 при различных значениях анодной плотности тока, продолжительности
обработки и температуры электролита.
Рентгенофазовый анализ покрытия проводился на
установке ДРОН-3М в FeКα
– излучении при сканировании брэгговского угла
со скоростью 2 град/мин. Идентификация фаз на дифрактограммах
производилась по картотеке ASTM.
Коррозионные потенциалы Ес оксидного покрытия
измерялись в стандартной двухэлектродной термостатируемой ячейке с модельным электролитом,
относительно насыщенного хлорсеребряного электрода сравнения при температуре
36,60С, соответствующей нормальной температуре тела человека.
Коррозионный электролит представлял изотонический раствор 0,9%
NaCl в дистиллированной воде с величиной pH=7,4, моделирующий плазму крови и тканевую жидкость
организма, а также условия функционирования имплантатов в биосреде.
Морфологические характеристики анодно-оксидных
покрытий образцов исследовались методами профилометрии и бесконтактного
определения размерных параметров выступающих частиц и имеющихся углублений, включая
поры. Для измерения параметров шероховатости использовался профилограф-профилометр
«Калибр-171011», для обработки элементов морфологии применялись специальная
компьютерная программа PlotCalc и анализатор изображений микроструктур АГПМ-6М с микроскопом «Биолам».
По результатам программных измерений автоматически строились график
распределения размеров частиц и пор, график изменения частоты размеров,
вычислялись статистические характеристики распределения элементов профиля.
Результаты исследования и их анализ
Рентгенофазовый анализ полученных анодно-оксидных
покрытий показал, что анодирование титана приводит к
образованию смешанных оксидов общего состава TiO2
(анатаз, брукит, рутил) с
примесями TiO, Ti2O3 и СuО. Данные металлооксиды обладают высокой биоинертностью
к средам организма и обусловливают
биологическую совместимость анодированных титановых имплантатов. Кроме того,
наличие в титанооксидном покрытии частиц оксида СuО обеспечивает антисептическое действие на окружающую биосреду с предотвращением развития в ней патогенных
микроорганизмов и появления воспалительных реакций тканей [4].
В результате металлографических
исследований структуры анодированных образцов и оптических измерений толщины h
анодно-оксидных покрытий было установлено, что необходимая для нормального
биомеханического взаимодействия толщина, составляет 30-40 мкм и формируется при
значениях анодной плотности тока i=40-50 мА/см2 и продолжительности
электролиза t=0,3 ч (рис.1).
![]()
![]()
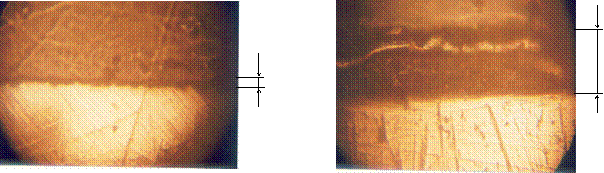
i
= 15 мА/см2,
t = 500С, τ = 0,9 ч i
= 50 мА/см2,
t = 500С, τ = 0,3 ч
а
б
Рис. 1. Микрошлифы титановых образцов, анодированных в электролите 200 г/л Н2SO4 + 50 г/л CuSO4 · 5Н2О
при различных режимах (х190):
а - h = 10 мкм; б – h = 40 мкм
Измерение коррозионных потенциалов Ес полученных оксидных
покрытий характеризовалось средним значением Ес=0,15 В, что
указывает на высокую коррозионную стойкость анодированных имплантатов в
физиологических средах организма (кровь, лимфа, тканевая жидкость).
Исследование параметров шероховатости анодно-оксидного
покрытия показало, что значения его микронеровностей,
составляющие в среднем Ra=1,35
мкм, Rz=3,45
мкм, Rmax=6,2
мкм и Sm=10
мкм, обусловливают высоко развитый рельеф поверхности, способный обеспечить
прочную физико-механическую взаимосвязь покрытия с костными структурами при их прорастании
в имеющиеся микронеровности (рис. 2).
Рис. 2. Рельеф
поверхности оксидного покрытия, полученного анодированием
титана при i = 50 мА/см2, t = 500С, τ = 0,3 ч
(х200)
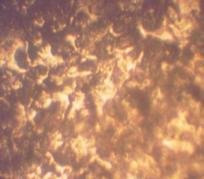
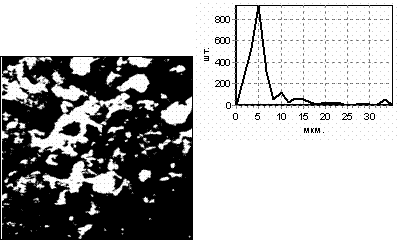
Программная обработка элементов морфологии покрытия, преобразованных в монохроматическое изображение (белые поля – частицы, черные поля – поры), позволила численно определить статистическое распределение и величину поверхностно-структурных параметров, установить характер их влияния на взаимодействие с биотканями (рис. 3, табл.1).
Частицы
Монохроматическое изображение
поверхности покрытия (х300)
|
Средний
радиус rч: 9,7 мкм Модальный
радиус rм: 5,0 мкм Размах варьирования Rч: 30 мкм Среднеквадр. отклон. Sч: 5,9 мкм Дисперсия
σч: 10,5 мкм Коэффициент вариации Vч: 60,4% |
||
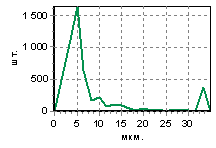
ПорыГрафик
распределения
|
Средний
радиус rп: 9,8 мкм Модальный
радиус rм: 5,0 мкм Размах варьирования Rп: 30 мкм Среднеквадр. отклон. Sп: 6,1 мкм Дисперсия
σп: 11,1 мкм Коэффициент вариации Vп: 56,3% Средняя пористость П: 30,7% |
Рис. 3. Программная обработка поверхности покрытия,
полученного анодированием пескоструйно
обработанного титана в сернокислом электролите при i=50 мА/см2, t=500С, τ=0,3 ч
Таблица 1
Среднестатистические результаты программной обработки параметров
морфологии оксидного покрытия, полученного анодированием
титана в электролите 200 г/л Н2SO4 + 50 г/л CuSO4
· 5Н2О при i=50 мА/см2, t=500С, τ=0,3 ч
|
№ участка покрытия |
Характеристики частиц |
Характеристики пор |
|||||||||||
|
rч, мкм |
rм, мкм |
Rч, мкм |
Sч, мкм |
σч, мкм |
Vч, % |
rп, мкм |
rм, мкм |
Rп, мкм |
Sп, мкм |
σп, мкм |
Vп, % |
П, % |
|
|
1 |
9,7 |
5,0 |
30 |
5,9 |
10,5 |
60,4 |
9,8 |
5,0 |
30 |
6,1 |
11,1 |
56,3 |
30,7 |
|
2 |
9,9 |
5,7 |
30 |
5,7 |
10,0 |
60,8 |
9,6 |
5,0 |
30 |
6,3 |
11,0 |
56,6 |
30,8 |
|
3 |
8,3 |
6,4 |
30 |
5,9 |
9,8 |
58,8 |
8,4 |
4,6 |
30 |
5,7 |
10,5 |
52,0 |
30,7 |
|
сред.
знач. |
9,3 |
5,7 |
30,0 |
5,8 |
10,1 |
60,0 |
9,26 |
4,86 |
30,0 |
6,0 |
10,8 |
55,0 |
30,7 |
Из полученных результатов следует, что значения морфологических характеристик оксидного покрытия, соответствуют условиям эффективной биоинтеграции анодированных имплантатов и их успешного применения в хирургической стоматологии.
Полученные результаты позволяют считать, что выбранные технологические условия оксидирования обеспечивают получение покрытий имплантатов с необходимым уровнем физико-химических и механических свойств, фазово-структурным состоянием, а также морфологической гетерогенностью, создающих качества биосовместимости и благоприятные условия для протекания процесса биоинтеграции (табл.2).
Таблица 2
Технологические условия анодирования
и параметры
оксидных покрытий титановых
дентальных имплантатов
|
Электролит, г/л |
Режим электролиза |
Параметры покрытия |
||||||||||
|
i, мА/см2 |
t, 0С |
τ, ч |
фазовый состав |
h, мкм |
σадг, МПа |
Нкв, ГПа |
П, % |
Ес, В |
Шероховатость, мкм |
|||
|
Rа |
Rmax |
Sm |
||||||||||
|
(200) H2SO4 + (50) CuSO4· 5Н2О |
30-50 |
40-50 |
0,3-0,9 |
TiO, TiO2,
Ti2O3, CuO |
30-50 |
29 |
10 |
30-35 |
0,15 |
1,35 |
6,20 |
10 |
Выводы
Проведены экспериментальные исследования
функциональных свойств оксидных биосовместимых покрытий титановых дентальных
имплантатов, полученных методом сернокислотного анодирования.
С помощью рентгенофазового анализа установлено, что
данные покрытия состоят из нестехиометрического TiO2 c примесью частиц CuО, обусловленной добавкой в сернокислый электролит сульфата
меди.
Определено коррозионное поведение анодно-оксидных
покрытий в модельной физиологической среде, соответствующей химическому составу
плазмы крови. Показано, что средняя положительная величина потенциала коррозии Ес покрытия, равная 0,15 В, обеспечивает
высокий уровень коррозионной стойкости анодированных имплантатов в биожидкостях.
Установлено, что рельеф покрытия характеризуется
высокой степенью шероховатости и морфологической гетерогенности,
создающих благоприятные условия для прорастания костных клеточных структур, биоинтеграции, прочного закрепления и эффективного функционирования дентальных
имплантатов.
Литература
1. Бутовский К.Г., Протасова Н.В. Материалы, используемые в производстве дентальных имплантатов // Современные проблемы имплантологии: Сборник научных статей по материалам 6-й Международной конференции. Саратов, 2002. С. 21-29.
2. Родионов И.В., Бутовский К.Г.
Функциональные свойства анодно-оксидных биосовместимых покрытий титановых
дентальных имплантатов / Материалы междунар. науч. конф. «Химия, химическая
технология и биотехнология на рубеже тысячелетий». Томск. Изд-во ТПУ, 2006, Т.2. С. 424-426.
3. Родионов И.В., Серянов Ю.В. Применение технологии анодного оксидирования при создании биосовместимых покрытий на дентальных имплантатах // Вестник Саратовского государственного технического университета, №2 (12), 2006. С. 77-87.
4. Родионов И.В. Исследование биоинтеграционных и антисептических свойств анодированных титановых имплантатов / Сборник науч. статей Всеросс. конф. «Актуальные проблемы электрохимической технологии». Саратов: Изд-во Сарат. гос. техн. ун-та, 2008. С. 196-200.