Технические науки. Металлургия
Карагандинский государственный технический университет,
Республика Казахстан
Проф., д.т.н. Исагулов А.З., доцент, к.т.н. Турсунбаева
А.К.,
Акимбаева Д.Г., проф., д.т.н.Портнов В.С., Акеева А.Т.
Выщелачивание золотосодержащих
руд циансодержащим реагентом
Кучное выщелачивание с
применением цианирования экономично и пригодно при переработке самородных
силикатных и карбонатных золотосодержащих руд [1, 2]. К таким рудам, прежде всего, относится золотосодержащая
руда окисленной зоны Васильковского месторождения (г.Кокшетау,
Казахстан).
Проведенные
исследования на рудах Васильковского месторождения показали, что наиболее
эффективным растворителем золота считаются цианистые растворы щелочных
металлов.
В Казахстане циансодержащие
соединения получают путем утилизации отходов фосфорной промышленности.
Циансодержащее соединение, полученное из твердой фазы котрельного
«молока», в составе которого присутствуют фосфаты, гексацианоферраты
(II, III) и цианид натрия, может применяться
в качестве растворителя золота. Его использование в гидрометаллургии
благородных металлов обусловлено свойством растворять золото в присутствии
кислорода при комнатной температуре [3]:
![]() . (1)
. (1)
Гексацианоферраты (II и III) натрия, присутствующие в полученном
продукте, также способны растворять золото по следующей реакции [4]:
![]() . (2)
. (2)
Исходя из
вышеизложенного, существует принципиальная возможность применения этого
циансодержащего реагента для выщелачивания золота из руд.
Следует
отметить, что каждый тип руды имеет свои особенности, обусловленные
определенным химическим и фазовым составом. Основными параметрами, влияющими
на извлечение целевого металла в раствор при кучном выщелачивании, являются
концентрация растворителя, плотность орошения и пауза между орошениями [5].
Предварительно экспериментальным путем, перколяционным
выщелачиванием руды, определены оптимальные параметры процесса выщелачивания
руд с использованием нового циансодержащего реагента.
Перколяционное выщелачивание является моделью кучного выщелачивания в лабораторных
условиях.
В
процессе исследований после каждого орошения образующийся золотосодержащий
продуктивный раствор анализировали на содержание золота, остаточного цианида и
определяли значения pH среды.
При использовании цианида натрия концентрация CN- в растворе составляет 0,4 г/дм3. Поэтому
изучение влияния плотности орошения на выщелачивание золота из руды при
применении циансодержащего реагента проводили при односуточной паузе орошения и
постоянной концентрации цианида в подаваемом растворе 0,4 г/дм3.
Плотность орошения (Р, дм3/т руды) изменяли от 5 до 20 дм3/т
руды.
Проведенные
расчеты [6] показали, что с повышением плотности орошения скорость растворения
золота, общее извлечение (eAu, %) и удельный расход цианида (QNaCN, г/г Au) при одинаковом числе орошений увеличивается (рисунок 1),
концентрация же золота в растворе после выщелачивания, наоборот, снижается.
Рисунок 1 – Зависимость извлечения золота (1) и удельного расхода цианида (2) за одно орошение от
плотности орошения
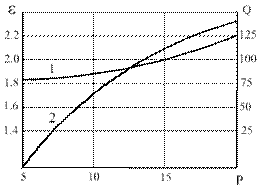
Так, при
плотности орошения 20 дм3/т руды извлечение металла составляет 2,3
%, это примерно в 2 раза больше, чем при плотности орошения 5 дм3/т
руды, а концентрация золота в полученном растворе в 2 раза ниже. Выщелачивание при высоких плотностях орошения и,
следовательно, при низких концентрациях золота и примесей, снижает диффузионное
сопротивление на границе раздела фаз Т - Ж, способствуя увеличению растворения
не только золота, но и элементов пустой породы. Высокое среднее извлечение
золота за одно орошение
Изучение
влияния концентрации цианида на перколяционное
выщелачивание руды проводили растворами циансодержащего соединения, содержащими
от 0,2 до 0,6 г/дм3 цианида, при плотности орошения 10 дм3/т
и паузе орошения 1 сутки. Установлено, что скорость растворения золота, степень
извлечения металла за одно орошение, концентрация металла в растворе и
удельный расход цианида с повышением концентрации используемого раствора
цианида натрия (СNaCN, г/г Au) увеличиваются (рисунок , а).
Однако при концентрации цианида 0,6 г/дм3 его удельный расход на
извлечение
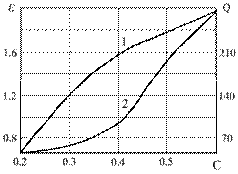
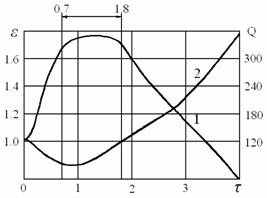
а) б) Рисунок 2 – Зависимость
извлечения золота (1) и удельного расхода цианида (2) за одно орошение от
концентрации цианида натрия (а) и продолжительности паузы между орошениями
(б)
Влияние
пауз орошения (t,сут) на
извлечение золота изучали с помощью раствора, приготовленного на основе цианидсодержащего соединения, содержащего 0,4 г/дм цианида, при плотности орошения 10 дм3/т руды при этом паузу орошения изменяли от 4 до 0
суток. Установлено, максимальному извлечению золота 1,8 % соответствует пауза
между орошениями 0,7-1,8 суток (рисунок 2, б). В соответствии с технологией
извлечения золота в промышленных условиях оптимальной паузой орошения следует
считать 1 сутки. Увеличение паузы орошения приводит к чрезмерному расходу
реагента, который в свою очередь на выход металла не влияет.
Таким
образом, по результатам исследований установлено, что максимальное извлечение
золота новым реагентом цианирования при минимальном расходе цианида из
окисленной золотосодержащей руды достигается при односуточной паузе между
орошениями, плотности орошения 10 дм3/т руды и концентрации цианида
в растворе циансодержащего соединения 0,4 г/дм3.
Литература:
1. Пыжов С. С. И др. Кучное выщелачивание
золотосодержащих руд за рубежом // Цвет. металлы. – 1984. – № 11. – С. 25-28.
2.
Parkhurst
D. The heap leach-carbon adsorbtion method for
processing gold ores //
3. Андреев
И.И. К вопросу о растворении золота в цианистых растворах // Известие
Санкт-Петербургского политехнического института. – 1998. – Т.9, - С. 447-485.
4. Костромина
Н.А. Химия координационных соединений. – М.: Высшая школа, 1990. 431 с.
5. Зеликман А.Н. и др. Теория гидрометаллургических процессов.
– М.: Металлургия, 1983. – 424 с.
6. Зеленов В.И. Методика исследования золото- и
серебросодержащих руд. – М.: Недра, 1989. – 302 с.