Кириллов В.Ю.1,
д.х.н., проф. Еркасов Р.Ш.2
1Кокшетауский государственный университет им. Ш.Ш. Уалиханова, Казахстан
2Павлодарский государственный
университет им. С. Торайгырова, Казахстан
Определение
коэффициентов распределения
α-аминофосфонатов методами компьютерной химии
Аминофосфонаты представляют несомненный интерес как биологически активные
вещества, комплексообразователи, экстрагенты, ионофоры и т. д. Для
практического использования этих соединений важное значение имеют данные об их
константах распределения между водой и органическими растворителями.
В настоящей работе с использованием методов компьютерной химии определены
константы распределения ряда α-аминофосфорильных соединений, которые были
синтезированы по «иминному» варианту реакции Пудовика
– присоединение гидрофосфорильных соединений к ароматическим азометинам в
отсутствие растворителя с использованием в качестве катализаторов бензола,
толуола, п-толуолсульфокислоты:
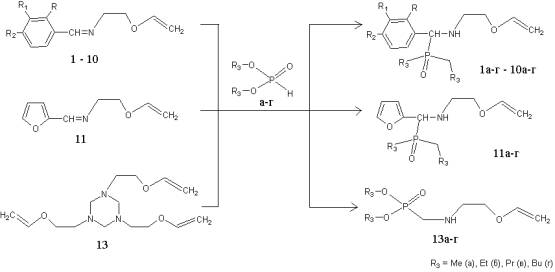
R=R1=R2=H (1), R=R1=H, R2=F (2), R=R1=H R2=O-CH3 (3), R=R2=O-CH3 (4), R=H, R1=R2=O-CH3 (5), R=R2=H, R1=O-CH3 (6), R=R1=H, R2=NO2 (7), R=R2=H, R1=NO2 (8), R1= R2=H, R=OH (9), R=R1=H, R2=N(CH3)2 (10)
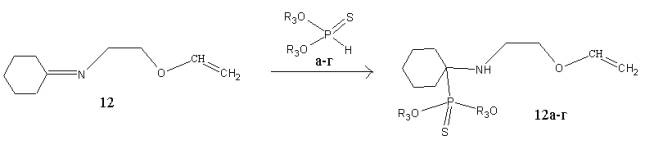
Гидрофобность
вещества (его липофильность) оценивается на основании расчета логарифма
коэффициента распределения вещества в двухфазной системе н-октанол–вода logP. Отрицательное значение logP означает, что
соединение имеет более высокую близость к водной фазе (более гидрофильно);
когда logP = 0, то соединение
одинаково распределено между липидной и водной фазами; положительное значение
logP означает более высокую
концентрацию соединения в липидной фазе (более липофильно).
Этот
параметр характеризует транспорт вещества через мембраны, его взаимодействие с
биологическими рецепторами и ферментами, токсичность и биологическую активность.
Коэффициент
распределения необходим для оценки распределения лекарственных препаратов по
организму. Гидрофобные препараты с высоким коэффициентом распределения
предпочтительно распределены в гидрофобных местах, например, в билипидном слое
клеток, в то время как гидрофильные препараты (низкий коэффициент
распределения) предпочтительно найдены в гидрофильных местах, например, в
сыворотке крови.
В
контексте агрохимии гидрофобные инсектициды и гербициды имеют тенденцию быть
более активными. С другой стороны, гидрофобные агрохимикаты имеют более длинный
период полураспада и поэтому проявляют увеличенный риск неблагоприятного
экологического воздействия. Согласно правилу трех
Бриггса, соединение в качестве инсектицида, гербицида и фунгицида биоактивно
при logP < 3.
Коэффициент
распределения может быть определен экспериментально. Самыми наиболее
распространенными методами являются метод Shake Flask и метод ВЭЖХ.
Коэффициент
распределения (logP) исследуемых соединений был
определен с помощью программ ACD/LogP v.12.0 (Advanced
Chemistry Development Inc., Toronto, Canada) [1-2] и Instant JChem v.2.2.1 (ChemAxon, Hungary) [3-5].
Для оценки корректности
интерпретации коэффициента распределения (logP) исследуемых соединений, нами
было проведено сопоставление известных экспериментальных данных достаточно
хорошо изученных α-аминофосфонатов с результатами компьютерных расчетов. В таблице 1
приведены тестовые расчеты коэффициента
распределения α-аминофосфорильных соединений.
Таблица 1 – Тестовые расчеты коэффициента распределения
(logP) ряда α-аминофосфорильных соединений (R1O)2P(O)-X-NHR2
|
Формула
вещества |
logP |
|
||||||
|
эксп. [6] |
данные комп. расчета (ACD/LogP) |
погреш- ность, % |
данные комп. расчета (Instant Jchem) |
погреш- ность, % |
||||
|
X |
R1 |
R2 |
||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
|
|
|
4,26 |
4,95±0,35 |
13,94 |
4,94 |
13,77 |
|
|
|
|
|
6,49 |
6,42±0,34 |
1,08 |
6,57 |
1,22 |
|
|
|
|
|
7,62 |
9,00±0,49 |
15,33 |
7,20 |
5,51 |
|
|
|
|
|
10,37 |
11,93±0,50 |
13,08 |
9,52 |
8,20 |
|
|
|
|
|
11,36 |
12,78±0,49 |
11,11 |
10,56 |
7,04 |
|
|
|
|
|
3,55 |
5,98±0,34 |
40,64 |
6,21 |
42,83 |
|
|
|
|
|
7,54 |
9,09±0,47 |
17,05 |
7,45 |
1,19 |
|
|
|
|
|
11,60 |
12,46±0,38 |
6,90 |
9,85 |
15,09 |
|
|
|
|
|
6,66 |
8,80±0,35 |
24,32 |
8,60 |
22,56 |
|
|
|
|
|
4,06 |
6,55±0,34 |
38,02 |
6,61 |
38,58 |
|
|
|
|
|
12,63 |
13,52±0,38 |
6,58 |
10,64 |
15,76 |
|
|
|
|
7,18 |
9,37±0,35 |
23,37 |
9,00 |
20,22 |
|
|
|
|
|
5,99 |
8,60±0,37 |
30,35 |
7,97 |
24,84 |
|
|
|
|
|
10,18 |
11,10±0,37 |
8,29 |
9,54 |
6,29 |
|
|
|
|
|
7,58 |
8,25±0,36 |
8,12 |
7,37 |
2,77 |
|
|
|
|
|
7,06 |
7,91±0,36 |
10,75 |
7,37 |
4,21 |
|
|
|
|
|
9,14 |
9,85±0,36 |
7,21 |
8,73 |
4,49 |
|
|
|
|
|
9,14 |
10,40±0,35 |
12,12 |
8,94 |
2,19 |
|
Как
видно из таблицы 1 результаты расчета коэффициента распределения имеют
некоторое расхождение с литературными данными. Это может быть обусловлено
заданными условиями расчета (рН и температура), что в условиях эксперимента
зависит от множества факторов и может изменяться в течение времени.
Коэффициент
распределения вещества в двухфазной системе н-октанол–вода
(logP) (таблица 2) виниловых эфиров оснований Шиффа увеличивается в ряду
соединений 11 < 4 < 8 < 7 <
9 < 1 < 6 < 5 < 3 < 10 < 2 < 12.
Увеличение длины
углеводородных цепочек в молекулах О,О'-диалкил α-аминоалкилфосфонатов приводит к возрастанию коэффициентов распределения за
счет увеличения гидрофобности молекулы в целом; с уменьшением числа углеродных
атомов в алкильных группах, естественно, наблюдается обратный эффект.
Наименьшую липофильность
имеет соединение 13а (logP=-0,59±0,45),
наибольшую – 12г (logP=5,88±0,44 (5,20)).
Наибольшие значения
коэффициентов распределения характерны для О,О'-диалкил
α-аминоалкилтиофосфонатов, что, по нашему мнению, связано с меньшей
способностью тиофосфорильной группы по сравнению с фосфорильной образовывать
водородные связи с молекулами воды, что приводит к более сильному смещению
двухфазного равновесия в сторону органической фазы (таблица 2).
Таблица 2 – Коэффициент распределения (logP) молекул виниловых эфиров оснований Шиффа, О,О'-диалкил α-аминоалкилфосфонатов и О,О'-диалкил α-аминоалкилтиофосфонатов
|
Соеди-нение |
logP |
Соеди-нение |
logP |
Соеди-нение |
logP |
|||
|
ACDLab |
Instant Jchem |
ACDLab |
Instant Jchem |
ACDLab |
Instant Jchem |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
1 |
2,09±0,42 |
2,57 |
2 |
2,30±0,50 |
2,71 |
3 |
2,21±0,44 |
2,31 |
|
1а |
1,64±0,49 |
2,15 |
2а |
1,69±0,56 |
2,29 |
3а |
1,55±0,50 |
1,90 |
|
1б |
2,70±0,49 |
2,84 |
2б |
2,75±0,56 |
2,98 |
3б |
2,62±0,50 |
2,59 |
|
1в |
3,76±0,49 |
3,78 |
2в |
3,82±0,56 |
3,92 |
3в |
3,68±0,50 |
3,52 |
|
1г |
4,83±0,49 |
4,57 |
2г |
4,88±0,56 |
4,71 |
3г |
4,74±0,50 |
4,32 |
|
4 |
1,82±0,46 |
2,06 |
5 |
2,20±0,46 |
2,06 |
6 |
2,17±0,44 |
2,31 |
|
4а |
1,35±0,51 |
1,65 |
5а |
1,38±0,51 |
1,65 |
6а |
1,55±0,50 |
1,90 |
|
4б |
2,41±0,51 |
2,33 |
5б |
2,44±0,51 |
2,33 |
6б |
2,62±0,50 |
2,59 |
|
4в |
3,48±0,51 |
3,27 |
5в |
3,50±0,51 |
3,27 |
6в |
3,68±0,50 |
3,52 |
4г |
4,54±0,51 |
4,06 |
5г |
4,56±0,51 |
4,06 |
6г |
4,74±0,50 |
4,32 |
|
7 |
2,01±0,43 |
2,52 |
8 |
2,00±0,44 |
2,52 |
9 |
2,05±0,45 |
2,28 |
|
7а |
1,37±0,50 |
2,11 |
8а |
1,37±0,50 |
2,11 |
9а |
0,90±0,49 |
1,87 |
|
7б |
2,43±0,50 |
2,79 |
8б |
2,43±0,50 |
2,79 |
9б |
1,97±0,49 |
2,55 |
|
7в |
3,49±0,50 |
3,73 |
8в |
3,49±0,50 |
3,73 |
9в |
3,03±0,49 |
3,49 |
|
7г |
4,56±0,50 |
4,52 |
8г |
4,56±0,50 |
4,52 |
9г |
4,09±0,49 |
4,28 |
|
10 |
2,26±0,44 |
2,83 |
11 |
1,25±0,82 |
1,52 |
12 |
3,44±0,50 |
2,37 |
|
10а |
1,75±0,51 |
2,42 |
11а |
0,80±0,50 |
1,10 |
12а |
2,69±0,44 |
2,79 |
|
10б |
2,81±0,51 |
3,10 |
11б |
1,86±0,50 |
1,79 |
12б |
3,75±0,44 |
3,47 |
|
10в |
3,87±0,51 |
4,04 |
11в |
2,93±0,50 |
2,72 |
12в |
4,82±0,44 |
4,41 |
|
10г |
4,94±0,51 |
4,83 |
11г |
3,99±0,50 |
3,52 |
12г |
5,88±0,44 |
5,20 |
|
13а |
-0,59±0,45 |
0,43 |
13б |
0,47±0,45 |
1,11 |
13в |
1,53±0,45 |
2,05 |
|
|
|
|
|
|
|
13г |
2,60±0,45 |
2,84 |
Таким образом, несмотря на некоторые расхождения значений коэффициента
распределения в системе н-октанол –
вода (logP), полученных методами компьютерной химии, с
экспериментальными данными, что может зависеть от множества факторов проведения
эксперимента, использование методов компьютерной химии является приемлемым для
вычисления такой важной физико-химической характеристики соединения, как
коэффициент распределения (logP).
Литература:
1. ACD/LogP DB.
www.acdlabs.com/logp/ Advanced Chemistry Development, Inc.,
Toronto, ON, Canada. - 15 January, 2007.
2. Takacsne N.K.//
Acta Pharm. Hung. - 1998. - Vol. 68, № 1. - Р. 39-48.
4. Csizmadia F., Tsantili-Kakoulidou A., Panderi I. and
Darvas F. //J.Pharm.Sci. - 1997. - № 86 (7). - Р. 865-871.
5. Bouchard G., Carrupt P. A., Testa B., Gobry V. and Girault
H. H. //Pharm.Res. - 2001. - № 18 (5). - Р. 702-708.
6. Фицева Н.А. Синтез α-аминофосфонатов и их
способность к молекулярному распознаванию ди- и α-гидроксикарбоновых
кислот: автореф. … канд. хим. наук:02.00.03. –
Казань, 2004. – 21 с.