к.фарм.н.
Куліш С.М., Тетерятник А.О.
Запорізький державний медичний університет
Алкілування
5-(піридин-2-іл)-4R-1,2,4-тріазол-3-тіонів α-галоген-кетонами та їх відновлені системи
Алкілуванню
1,2,4-тріазол-3-тіонів α-галогенкетонами присвячено декілька робіт вітчизняних і іноземних авторів.
Встановлено, що рекція 1,2,4-тріазол-3-тіонів з α-галоген-кетонами
проходить виключно по атому сірки з утворенням
2-(1,2,4-тріазол-3-ілтіо)-1-арилетанонів.
При проведені нами
алкілування 5-(піридин-2-іл)-2H-1,2,4-тріазол-3-тіону
та 4-феніл-5-(піридин-2-іл)-1,2,4-тріазол-3-тіону α-галогенкетонами в середовищі етанолу з додаванням еквімолекулярної
кількості натрій гідроксиду відбувається також з утворенням відповідних
2-[5-(піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетанонів
рис. 1.
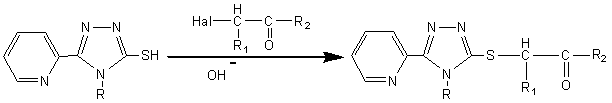
R= H, Ph; R1=Н, Ph; R2=C6H5, C6H4NO2-п, C6H4Сl-п, C6H4ОСН3-п
Рис. 1. Схема
синтезу 2-[5-(піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетанонів
із 5-(піридин-2-іл)-4R-1,2,4-тріазол-3-тіонів.
Отримані
2-[5-(піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетанони
–
білі або жовті кристалічні речовини
практично нерозчинні у воді, розчинні в спиртах та диметилформаміді. Для
аналізу сполуки перекристалізовані із суміші ДМФА:вода, 2:1, метанолу, суміші
етанова кислота:вода, 2:1; суміші етанол:н-пропанол, 1:1, ізобутанолу, або н-пропанолу.
Індивідуальність
сполук підтверджена за допомогою тонкошарової хроматографії, в різних системах
розчинників
ІЧ-спектри сполук характеризуються смугами коливань NH-груп в межах 3500 –
3300 см–1 , піридинового циклу в межах
1510 – 1480 см-1, C=N-груп
в межах 1650 – 1605
см–1, та СО- груп в межах 1725 – 1700 см-1 , О2N-груп
в межах 1550 – 1520 см–1
і 1360 – 1340 см–1,
також наявні смуги коливаня в межах 1465 – 1440 см–1,
що характерно для ароматичного кільця.
ПМР-спектр 2-(5-(піридин-2-іл)-2H-1,2,4-тріазол-3-ілтіо)-1-фенілетанону характеризується наявністю сигналів протонів метиленової групи, зв’язаної
з атомом сірки (4.21 м.ч.), протонів піридинового циклу (7.36, 7.85, 8.38, 8.59
м.ч.), ароматичних протонів фенільного радикалу (7.45, 7.50, 7.58, 7.94 м.ч.).
Продовжуючи пошук
біологічно активних речовин теоретичний і практичний інтерес представляло
синтезувати ряд 2-(1,2,4-тріазол-3-ілтіо)-1-арилетанолів. При цьому
може бути використано селективний метод відновлення карбонільної
групи, описаний в монографії, дисертації.
Відновлення відповідних 2-(5-R-1,2,4-тріазол-2-ілтіо)-1-арилетанонів
ми
проводили
натрій
боргідридом з додаванням еквімолекулярної кількості натрій
гідроксиду. Реакцію проводили протягом 24 год при кімнатній
температурі. Реакційну суміш підкисляли ацетатною кислотою,
осади сполук відфільтровували.
2-[5-(Піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетанони,
які містять залишок п-нітрофенацилброміду
відновлювались за методикою, суть якої полягає в тому, що як розчинник
застосовували диметилформамід, а розчин лугу та боргідриду натрію додавали з
такою швидкістю, щоб рН середовища не перевищував 9, а температура реакційної
суміші не піднімалася вище 250С. Після додавання всього борогідриду натрію
реакційну суміш залишають на 24 год при кімнатній температурі, потім
підкисляють ацетатною кислотою, осад сполук відфільтровують.
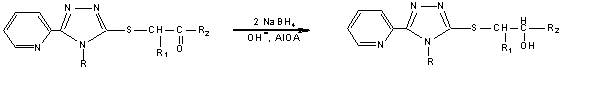
R= H, феніл ; R1=Н,
феніл; R2= C6H5, C6H4NO2-4;
C6H4Сl-4, C6H4ОСН3-4
Рис. 2 Схема
відновлення 2-[5-(піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетанонів натрій
боргідридом
Синтезовані
2-[5-(піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетаноли білі або жовті
кристалічні речовини практично не розчині у воді, але розчинні в розчинах лугів
і органічних розчинниках. Сполуки очищені із суміші метанол: вода, 1:1, сполуки
– із суміші етанова кислота:вода, 2:1, із суміші етанова
кислота:вода:диметилформамід, 1:1:1, із ізобутанолу.
Індивідуальність
одержаних сполук 2.42-2.50 підтверджена методом тонкошарової хроматографії в
різних системах розчинників.
ІЧ-спектри сполук
характеризуються наявністю смуг коливань C=N-груп в межах 1650 – 1610 см–1,
NH-груп в межах 3400 – 3200 см–1, О2N-груп в межах 1550 – 1510 см-1
і 1350-1320 см–1, смуги коливань піридинового циклу 1500 – 1480 см-1 та смуги
коливань СS-груп в межах 600 – 520 см–1. На відміну від
2-[5-(піридин-2-іл)-4R-1,2,4-тріазол-3-ілтіо]-1-арилетанонів виявлені смуги в
межах 3590 – 3490 см–1, які відповідають валентним коливанням ОН-груп, а смуги
коливання СО-груп в межах 1725 – 1700 см-1 відсутні.
ПМР-спектр
2-(5-(піридин-2-іл)-2H-1,2,4-тріазол-3-ілтіо)-1-фенілетано-лу (2.42), (рис.
2.14) характеризується сигналами протонів карбоксильної групи (4.95 м.ч),
метиленової групи, зв’язаної з атомом сірки (3.54 м.ч.) та протонів
піридинового циклу (7.36, 7.85, 8.38, 8.59 м.ч.).
Список використаної літератури:
1.
Авраменко Н. А. Синтез, свойства и
биологическая активность галогенидов 1-алкил(ацилалкил)-4-амино(алкиламино,
илиденамино)-1,2,4-тріазолия : дис. канд. фармац. наук. / Авраменко Н. А. – Львов, 1987. – 134 с.
2.
Кныш Е. Г. Синтез, физико-химические и
биологические свойства N- и S‑замещенных 1,2,4-триазола : дис. … д-ра
фармац. наук / Кныш Е. Г. – Х., 1987.– 350 с.
3.
Панасенко О. І. Синтез, перетворення,
фізико-хімічні та біологічні властивості аміно- і тіопохідних 1,2,4-тріазолу :
дис. … д-ра фармац. наук / Панасенко О. І. – К., 2005. – 396 с.
4.
Парченко В. В. Синтез и биологическая
активность S-замещенных 5-(2-фурил)-2,4-дигидро-1,2,4-триазол-3-тиона /
Парченко В. В., Панасенко А. И., Кныш Е. Г. // Актуальні питания фармац. та
мед. науки та практики : зб. наук. ст. – Запоріжжя, 2004. – Вип. ХІII. – С.
241–244.
5.
Поиск биологически активных веществ в
ряду производных 3-ацил-алкилтио-1,2,4триазолов и их бициклических систем / В.
В. Парченко, А. И. Панасенко, Е. Г.
Кныш, А. Н. Лесничая // Запорож. мед. журн. – 2005. – № 2. – С. 126–129.
6.
Chen Wen-Bin. Синтез и биологическая
активность новых тріазольных соединений, содержащих cepy / Chen Wen-Bin, Jin
Gut-Yu. // Gaodeng xuexiao huozun xuebao = Chem. J. Chin. Univ. – 2001. – Vol.
22, № 7. – P. 1147–1151.
7.
Synthesis of new 5-substituted
1,2,4-triazole-3-thione derivatives / Foks H., Czarnocka-Janowicz A., Rudnicka
W., Trzeciak H. // Phosph., Sulfur and Silicon and Relat. Elem. – 2000. – Vol.
164. – P. 67–81.
8.
Vardhan V. Aditya. Condensation of
3-methyl/ethyl-5-mercapto-s-triazole with 3-acetylcoumarin and its derivatives
/ Vardhan V. Aditya, Kumar V. Ravi, Rao V. Rajeswar // Indian J. Chem. B. –
1999. – Vol. 38, № 1. – P. 18–23.