Племенков В.В., Мазова О.В., Покровская И.С., Апыхтин
Н.Н.
Российский государственный университет им. Иммануила
Канта
Россия, г.
Калининград 236040, ул. Университетская, 2 , кафедра химии
Некоторые особенности
химического состава эфирных масел соцветий тысячелистника обыкновенного
(Achillea millefollium L.)
Растения семейства сложноцветных (сompositae) – наиболее
высокоорганизованные представители высших растений – широко представлены в
растительном царстве большим разнообразием видов и отличаются высокой
устойчивостью к воздействию внешних факторов. Последний факт позволяет
предположить наличие в таких растениях развитой системы биосинтеза веществ
вторичного метаболизма с разноплановыми защитными функциями, функциями
выживания. Именно поэтому многие представители семейства сompositae входят в
реестр лекарственных растений [1]. Они интересны тем, что в их составе
обнаружены химические вещества различных классов, обладающих бактерицидным,
противовоспалительным, кровоостанавливающим действием, обладающих свойством
активизировать фагоцитарные функции организма.
Среди официальных лекарственных растений семейства сложноцветных следует
выделить некоторые виды тысячелистника (Achillea millefollium L.)- повсеместно распространенные сорные
растения.
Тысячелистник обыкновенный (Achillea millefollium L.) [1] – многолетнее травянистое растение,
стебель до 50 см высотой. В медицине
используют траву тысячелистника [2] как настои и жидкие экстракты, в качестве
кровоостанавливающих, гемостатических средств растительного происхождения.
Биологически активный комплекс тысячелистника обыкновенного представлен
известными веществами - фенольными
соединениями, полисахаридами, витаминами, эфирными маслами. Трава также
содержит малоизученные основания, гликоалкалоид ахиллеин, органические кислоты,
смолы и др. В составе эфирного масла тысячелистника обыкновенного найдены азулены, сложные эфиры, камфора, туйол,
цинеол, кариофиллен – всего насчитывается 50 компонентов [3]. Из литературных источников известно о
химической изменчивости тысячелистника обыкновенного, в том числе его эфирного
масла [4].
Учитывая отсутствие данных по составу эфирных масел тысячелистника
обыкновенного, произрастающего в анклаве Калининградской области с его
характерным прибалтийским климатом, нами проведено сравнительное исследование
состава эфирных масел, выделенных из соцветий видов семейства сompositae,
собранных в период цветения с эфирными
маслами, полученными от сбора тысячелистника в Татарии и на Алтае.
Представленные регионы существенно отличаются по климату от Калининградской
области, но расположены на одной широте, следовательно в одинаковом световом
режиме.
Выбор методики гидродистилляции или перегонки с водяным паром
обусловлен доступностью и высокой
эффективностью выделения летучих веществ [5]. А в случае тысячелистника
возможностью визуально контролировать выделение азулена (хамазулена) – одного
из основных компонентов эфирного масла, обладающего биологической активностью,
Хамазулен образуется из проазуленов (сесквитерпеновых γ-лактонов ) в
нативном растении.
Для исследования было подготовлено растительное сырье [6] – соцветия
тысячелистника обыкновенного. Морфологических различий у растений, с которых
срезали соцветия, не было выявлено. Сбор производился в период с начала
цветения и окончания с июня по сентябрь 2007 г. Образцы растений были собраны в
трех местах:
1.
Валообразная
береговая дюна. Пионерск.
Калининградская область.
2.
Пригородная
зона отдыха. Илеть. Марийская республика.
3.
Пригородная
зона отдыха. Барнаул. Алтай.
Все образцы сушили и хранили в одинаковых условиях в соответствии с
правилами сбора и сушки лекарственных растений[6].
Эфирное масло получали методом перегонки с паром, используя классическую
методику в сочетании с вводом низкокипящего органического растворителя
(петролейного эфира) в перегонную колбу
по окончании отгонки [5].Это позволяет избежать значительных потерь
продуктов отгонки за счет сорбции на стенках прибора. Однако, вместо паровика
нами использовалась капельная воронка, заполненная дистиллированной водой,
поступающей в нагреваемую перегонную колбу по мере испарения влаги.
Для получения эфирных масел в рабочую колбу вместимостью 500 мл помещали
40г соцветий, заливали дистиллированной водой (около 200 мл) и подсоединяли
капельную воронку, заполненную водой. Отгоняли дистиллят в течение 3 часов с
момента появления первых его капель. Скорость отгонки составляла 2-3 капли в
секунду. По окончании процесса через капельную воронку вливали 20 мл
петролейного эфира в рабочую колбу. Пар пропускали до полного перехода
растворителя в приемник. Полученный дистиллят экстрагировали, эфирную вытяжку
сушили безводным сульфатом натрия, отгоняли
растворитель и получали темно-синее масло .
Химический состав полученных концентратов эфирных масел изучали методом хромато-масс-спектрометрии (GC-MS). Пробы анализировали на масс-спектрометре с двойной
фокусировкой «Thermo Finning» модели«DFS», работающем в режиме электронной ионизации, в сочетании с
газовым хроматографом той же фирмы
модели «Trace GC Ultra». В качестве газа носителя использовали
гелий. Определение осуществляли с использованием колонки«Trace-5MS» длиной 30м, внутренним диаметром 0,25 мм
и толщиной слоя неподвижной фазы 0,1мкм. Скорость потока через колонку
составляла 0,8 мл/мин. Вводили со сбросом, который составлял 50/1. Температура
инжектора, переходной линии и ионного источника оставляли 275ºC, 280
ºC, 235 ºC соответственно.
Условия программирования температуры были следующими: начальная
температура колонки 40 ºC (1 мин.), нагрев со скоростью 10 ºC /мин.
До температуры 300 ºC (5 мин.). Образцы анализировали в режиме селективной
регистрации ионов с m/z 215.1674, 238.1470, 294.2096. Энергия электронов
составляла 70 эВ. Исследования проводили, используя электрическое сканирование. В ходе анализа непрерывно вводили
калибровочное вещество, перфтортрибутиламин. Ион m/z 213.98975 использовали в
качестве реперного. Разрешение составляло 11200, напряжение на электронном
умножителе 1615 В.
Идентификация компонентного состава по хроматограммам была проведена с
использованием библиотеки масс-спектров: 1) NISТ¢05
; 2) Wіlеу 7th Εdition.
Всего хроматограмма показывает наличие в эфирных маслах всех образцов не
менее 60 компонентов, из которых идентифицировано 52-55 соединений. Типичная
хроматограмма эфирного масла
образца Achillea millefollium L. №1 приведена на рисунке. На
хроматограмме отчетливо видно, что пики мжно разделить по интенсивности на 3
группы: 1) пики мажорных веществ, содержание
которых более 10%; 2) пики веществ средней интенсивности (от 10 до 1%);
3) пики минорных веществ (от 1 до 0,1%). Вещества, содержащиеся в количестве
менее 1% можно считать следовыми.
Результаты по химическому составу эфирного масла растений показывают,
что компонентные составы второй и третьей групп близки по средним значениям.
Так, хамазулена 24,6% и 26,3%; гермакрена 19,8% и 14,1%; β-пинена 9,9 % и 8,3%; эвкалиптола 7,5% и 7,4%,; борнил
ацетата 2,2; кариофиллена 17,7% и 5,9%.
Полученные нами результаты по Калининградской области заметно отличаются от
приведенных выше: хамазулена 37,5%; кариофиллена 19,7%; гермакрена 13,6% и
борнил ацетата 2,2%. В 1 группе
присутствуют зингиберен (2,3%); виридофлорол (3,04%); цис-фарнезол
(2,1%) в то время как во 2 и 3 группах
эти вещества не найдены.
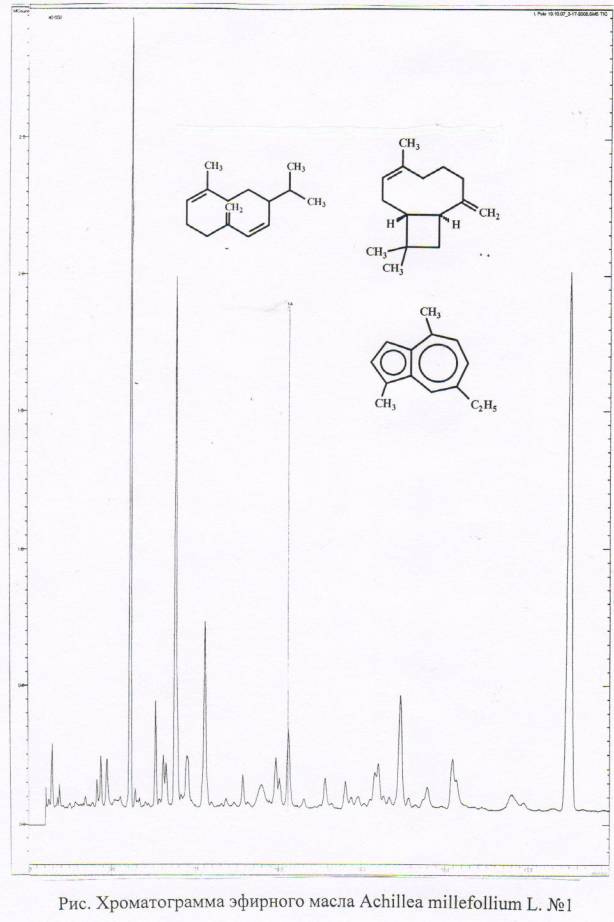
Таблица. Компонентный состав эфирного масла соцветий
тысячелистника
обыкновенного ( Achillea millefollium L.)
|
Содержание компонента в эфирном масле, в
% |
Achillea №1 |
Achillea № 2 |
Achillea №3 |
|
Кариофиллен |
19,7 |
17,7 |
5,9 |
|
Кариофиллен оксидон |
2,6 |
14,7 |
14,7 |
|
Гермакрен |
13,6 |
19,8 |
14,1 |
|
Эвкалиптол |
6,9 |
7,5 |
7,4 |
|
β-Пинен |
9,1 |
9,9 |
8,3 |
|
Хамазулен |
37,5 |
24,6 |
26,3 |
|
Гумулен |
1,9 |
Не обн. |
7,3 |
|
Зингиберен |
2,3 |
Не обн. |
Не обн. |
|
δ-Кадинен |
2,4 |
5,60 |
6,2 |
|
Неролидол |
5,6 |
Не обн. |
14,2 |
|
Борнил ацетат |
2,2 |
10,7 |
10,7 |
|
Виридофлорол |
3,0 |
Не обн. |
Не обн. |
|
цис-Фарнезол |
2,1 |
Не обн. |
Не обн. |
Сопоставление всех данных показывает, что три соединения
сесквитерпенового ряда – кариофиллен, гермокрен и хамазулен – могут быть
принятыми в качестве таксонов для растений вида Achillea millefollium L., так как во всех случаях они являются
мажорными веществами. Кроме того, можно отметить, что относительное содержание
гермокрена и кариофиллена меняется в зависимости от климатической зоны – в
условиях континентального климата из двух компонент гермокрен и кариофиллен
доминирующим является гермокрен, в условиях морского климата - кариофиллен.
Литература
1.
Атлас ареалов и ресурсов
лекарственных растений СССР, М., 1980, С.316
2.
Машковский М.Д.
Лекарственные средства. М., «Новая волна», 2000, С.473
3.
Дембицкий А.Д., Юрина
Р.А., Кротова Г.И. Особенности терпеноидного состава эфирных масел некоторых
видов тысячелистника Казахстана и Средней Азии // Основные направления научных
исследований по интенсификации эфирномасличного производства// Всесоюзн.
научно-техн. Совещание. Тез.докл. и сообщ. 4-го симпоз. По эфирномасличным
растениям и маслам (Симферополь, 1-4 октября 1985г.) Симферополь, Ч.3, 1985, С.62
4.
Устюжанин А.А.,
Коновалов Д.А., Шретер А.И. и др. Содержание хамазулена в Achillea millefollium L.s.1. в европейской части СССР// Рас. Ресурсы, 1987, Т.23, вып.3, С.424-429
5.
Палей Р.В.,
Племенков В.В., Аритемова Н.П., Чугунов Ю.В., Фазлыева М.Г. Химический состав
эфирного масла Achillea millefollium L., полученного методо гидродистилляции. Раст. Ресурсы, вып.4,
1996, С.37-44
6.
Правила
сбора и сушки лекарственных растений: Сборник инструкций, 1985 г.