Медицинские науки/ 7.Клиническая медицина
О. В. Кривошей, Г. Г. Берест, А. І. Авраменко, С. І. Коваленко
Запорізький державний
медичний університет
Результати дослідження
протитуберкульозної активності похідних [1,2,4]триазино[2,3-с]хіназоліну
Ключові слова: протитуберкульозна активність, похідні [1,2,4]триазино[4,3-c]хіназоліну.
Туберкульоз
є сьогодні гострою та актуальною медико-соціальною проблемою не тільки в
Україні, але і у всьому світі. За прогнозами Всесвітньої організації охорони
здоров'я, протягом наступного десятиліття на нашій планеті буде близько 90 млн.
нових випадків туберкульозу, причому більшість з них у віковій групі від 20 до
49 років, тобто в найбільш продуктивний період життя. Епідемія туберкульозу в
Україні невпинно прогресує і набуває загрозливих масштабів [1]. Внаслідок
політичних і економічних труднощів, децентралізації медичних установ і
скорочення бюджету охорони здоров'я існуюча система боротьби з туберкульозом перестала
справлятися в належній мірі із зростаючим числом хворих. На додаток до цього
високий рівень захворюваності туберкульозом серед асоціальних груп населення
(колишні ув’язнені, мігранти, безпритульні) погіршує і без того складну
ситуацію. До перерахованих проблем приєдналися такі моменти патоморфозу
туберкульозу, як резистентність та ВІЛ-інфекції. Все це призвело до того, що
проведення боротьби з туберкульозом старими методами стало неможливим. Отже,
вирішення соціальних проблем і, безперечно, пошук і створення
резистентностійких протитуберкульозних засобів є актуальною проблемою
сьогодення.
Для
оцінки протитуберкульозної активності нами відібрані сполуки (1.1-1.3), які синтезовані на кафедрі
органічної і біоорганічної хімії Запорізького державного медичного університету
[2] та у тесті на антибактерільну дію показали високу активність по відношенню
до Mycobacterium luteum.
Досліджувані сполуки є похідними [1,2,4]триазино[2,3-с]хіназоліну і мають наступну будову (рис. 1).
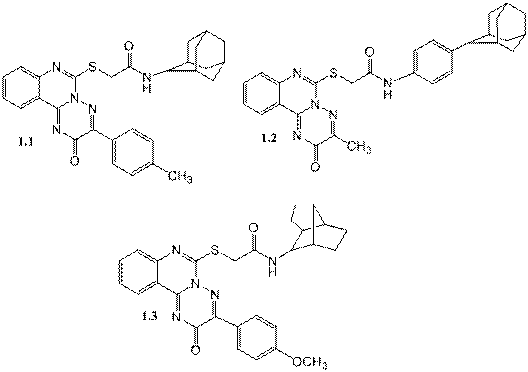
Рис. 1. Будова N-циклоалкіл-(циклоалкарил)-2-[(3-R-2-оксо-2H-[1,2,4]триазино[2,3-с]хіназолін-6-іл)тіо]ацетамідів (1.1-1.3)
Протитуберкульозну
активність синтезованих сполук вивчали у середовищі Левенштейна-Йєнсена, що
використовується при визначенні стійкості до антибіотиків, за методом Канетті іn vitro
[3]. В якості культури, обраної для тестування, використовували лабораторний
штам Mycobacterium tuberculosis Н37RV, чутливий до антибактеріальних препаратів групи гідразидів
ізонікотинової кислоти. Робочі концентрації досліджуваних речовин отримували
шляхом розведення 0,1 г наважки в 10 мл спирту етилового у мірній колбі на 100 мл.
Після цього готували 4 розчини: розчин А (0,1 г
наважки у 10 мл спирту доводили у мірній колбі до 100 мл водою стерильною,
концентрація сполуки 1×10-3 г/мл); розчин Б (1,0 мл розчину А доводили
у мірній колбі до 10 мл водою стерильною, концентрація сполуки 1×10-4
г/мл); розчин В (1,0 мл розчину Б доводили у мірній колбі до 10 мл водою
стерильною, концентрація сполуки 1×10-5 г/мл); розчин Г (2,0
мл розчину В доводили у мірній колбі до 100 мл водою стерильною, концентрація
сполуки 0,2×10-6 г/мл). Середовище Левенштейна-Йєнсена з отриманою
концентрацією досліджуваних речовин розливали по 5,0 мл у стерильні
пробірки та згортали у скошеному вигляді за 85 °С
протягом 30 хв в приладі для згортання сироватки крові. На готове
середовище засівали суспензію лабораторного штаму Myc. tuberculosis
Н37RV,
відкаліброваного за стандартом мутності 1МсF (300×106
мікротіл/мл) та розведену до 10-4 стерильним фізіологічним розчином
натрію хлориду. Паралельно було зроблено два контрольні посіви на середовище
Левенштейна-Йєнсена без додавання досліджуваних речовин. Посіви інкубовано в
термостаті за 37°С. Чутливість визначали вимірюванням
мінімальної інгібуючої концентрації (МІК) - найменшої концентрації
досліджуваних сполук, яка повністю пригнічує видимий ріст мікроорганізмів.
Висновки.
Проведені дослідження показали, що МІК для досліджених сполук складає 0,2×10-6
г/мл. Таким чином, N-циклоалкіл-(циклоалкарил)-2-[(3-R-2-оксо-2H-[1,2,4]триазино[2,3-с]хіназолін-6-іл)тіо]ацетаміди (1.1-1.3) в інтервалі наведених
концентрацій проявляють високу протитуберкульозну активність і потребують більш
поглиблених досліджень.
Література:
1.
Эпидемиологическая ситуация по туберкулезу
в Украине. - Режим доступу: http://tb.org.ua/statistics/problema-tuberkuleza-v-ukraine.html
2.
Берест Г. Г. 3-R-6-тіо-6,7-дигідро-2H-[1,2,4]триазино[2,3-c]хіназолін-2-они: синтез,
функціоналізація, фізико-хімічні та біологічні властивості : автореф. дис. на
здобуття наук. ступеня канд. фармац. наук : спец. 15.00.02 Львів. нац. мед.
ун-т ім. Д. Галицького / Г. Г. Берест. - Львів, 2012. - 24 с.
3.
Стандарти бактеріологічної діагностики
туберкульозу в лабораторіях протитуберкульозних закладів України: навчальний
посібник для фахівців бактеріологічних лабораторій закладів протитуберкульозної
служби України / О. А. Журило, А. І. Барбова, Т. Г. Глушкевич, Л. В. Третякова.
– Київ, 2012. – 188 с. – Режим доступу: http://www.ifp.kiev.ua/ftp1/metoddoc/posibnyk_1_2012.pdf
Відомості про авторів
E-mail: krivoshejjoksana@rambler.ru
Берест Галина Григорівна - к. фарм. н., доцент
кафедри фармакогнозії, фармацевтичної хімії і технології ліків, Запорізький
державний медичний університет
Авраменко Антоніна Іванівна - к. фарм. н., доцент
кафедри фізколоїдної хімії, Запорізький державний медичний університет
Коваленко Сергій Іванович – д. фарм. н.,
професор, завідувач каф. органічної і біоорганічної хімії, Запорізький
державний медичний університет
E-mail: Kovalenkosergiy@gmail.com