Медицина/8.Морфология
к.м.н. Косторная И.В., к.м.н. Ермакова О.М.
Ставропольский государственный медицинский
университет, доценты кафедры патологической анатомии и судебной медицины
Морфологическое исследование соматической патологии на фоне
хронической опиатной интоксикации
Потребление низкокачественного
«афганского» героина наркоманами на территории Ставропольского края за
последние 10 лет привело к формированию героинсвязанной патологии. Это явление
послужило толчком к существенному росту числа случаев смерти наркоманов как при
остром отравлении героином (объект судебно-медицинских исследований); так и при
хронической наркотической интоксикации, которая являлась фоном для
множественной висцеральной патологии у наркоманов. Как правило, в стационар при
хронической наркотической интоксикации больной поступает с проявлениями
соматической патологии.
По данным Управления по наркотикам и
преступности ООН (УНП ООН, 2009 г.) героин применяли около 16 млн человек. В
2007г незаконный оборот опиатов достиг 476,5т в морфиновом эквиваленте, из
которых 365т произведено в Афганистане. Для медицинских и научных целей во всем
мире в этом же году потребовалось 27,3 т морфина. В 2007 г. Афганистан произвел
87% мировой опийной продукции.
Понимание патоморфо- и танатогенеза при
наркомании затруднено из-за многообразия эффектов от вводимых в организм
веществ и препаратов, которые используют наркоманы, а также поражения многих
органов и систем на различных уровнях и в различных комбинациях, возникающего
при длительном их потреблении. Это – безусловно, затрудняет верификацию
наркомании и ставит патологоанатома в сложную диагностическую ситуацию.
Нами были исследованы 242 протокола
патологоанатомического вскрытия с последующей гистологической обработкой лиц,
погибших от соматической патологии в стационарах городских и краевой больниц
(характер соматической патологии представлен циррозом, сепсисом, деструктивной
пневмонией, язвенная болезнь и т. д).
Произведен количественный анализ гистологических структур,
доступный практикующему врачу – патологоанатому. Анализ данных осуществлен с
использованием пакета статистических программ STATISTICA6.0.
Сравнительная характеристика возраста
больных героиновой наркоманией в зависимости от длительности интоксикации и
пола представлена в таблице № 1.
|
Группа |
Пол |
n |
Возраст, лет |
|||
|
M±SE |
Медиана |
Min |
Max |
|||
|
|
жен. |
73 |
25.1±0.6 |
24 |
18 |
39 |
|
муж. |
169 |
23.5±0.3 |
24 |
15 |
38 |
|
P м/ж = 0.285
Достоверность различий средних величин
между мужчинами и женщинами оценивалась по U – критерию Манна – Уитни.
Из таблицы №1 следует, что хронической
наркоманией страдают уже лица возраста: у женщин 18 лет, а у мужчин 15 лет.
Контингент разделен на 3 группы:
1а – 66 больных; 1б – 143 чел., 1в – 33
чел., страдающих хронической героиновой (инъекционной наркоманией). Всего – 242
чел.
Иллюстрации
выполнены в редакторе Adobe Photoshop 8.0.
И.П. Анохина (1988) подчеркивает общность
клинической симптоматики при злоупотреблении психоактивными веществами, которая
обусловлена их однотипным действием на катехоламиновый обмен. Прием опиатов
приводит к значительному выбросу катехоламинов в кровь из надпочечников. Такой
резкий выброс нередко сопровождается положительными эмоциональными реакциями.
Постоянный прием наркотиков ведет к истощению запасов нейромедиаторов,
формированию «порочного круга», чем в значительной мере обусловлено проявление
синдрома психической зависимости [9,12].
Хроническая
интоксикация приводит к усилению синтеза катехоламинов и, соответственно, к
подавлению активности ферментов их метаболизма. Формируется ускоренный
кругооборот катехоламинов. При прекращении приема героина вследствие
вышеописанных механизмов происходит накопление дофамина в крови и биологических
жидкостях. Именно с этим связаны такие проявления синдрома физической
зависимости, как высокая тревожность, возбуждение, вегетативные нарушения и т.
д. Известно, что уровень дофамина в крови четко коррелирует с тяжестью
абстинентного синдрома [5, 6,11].
При секционном исследовании,
проведенном согласно общепринятым методикам, выявлены следующие признаки,
имеющие отношение к хроническому отравлению наркотическими веществами, в
частности героином.
Кожные
покровы в 3-х исследуемых группах отличались бледностью (78%), имелись типичные
следы инъекционных повреждений т. н. «дорожки», т.е. линейные плотноватые
рубцы.
В 1а и в
«б» подгруппах, где стаж употребления героина до 3-х лет и от 3 до 7 лет, из
соматических заболеваний преобладала патология печени, токсический гепатит
высокой степени активности с паренхиматозной желтухой и хроническим ДВС –
синдромом.
В 1в
подгруппе (героиновая зависимость более 7 лет) – преобладают такие состояния
как сепсис и на втором месте цирроз печени.
При внутреннем исследовании
трупов преобладали жидкая кровь в полостях сердца и в просветах сосудов (86%).
Оставшиеся, 14% приходятся на смерть от осложнений септического процесса,
связанного с тромбоэндокардитом трехстворчатого клапана (т. н. «эндокардит
наркоманов»), либо абсцедирующей пневмонией.
В нашем исследовании мы отобразили наиболее часто
встречаемую гистологическую картину.
В ткани головного мозга имелись признаки отека и
набухания его вещества, а также отек оболочек мозга. Это может быть объяснено
сочетанием расстройств микроциркуляции, свойственных отравлению опиатами, с
сердечно-дыхательной недостаточностью, связанной с поражением дыхательного
центра, нарастающим отеком легких и поражениями сердца[8]. Гистологически,
помимо отека дренажной глии, проявляющегося микроскопически периваскулярным и
перицеллюлярным отеком (Рис.1 .), выявлены разнообразные нарушения
микроциркуляции в виде стаза эритроцитов в капиллярах, общего венозного
полнокровия, пареза резистентного звена микроциркуляции, сладжа эритроцитов,
иногда образования фибриново-эритроцитарных тромбов и множественные мелкие
диапедезные кровоизлияния в субкортикальных отделах и в стволе, наблюдавшиеся в
53% случаев.
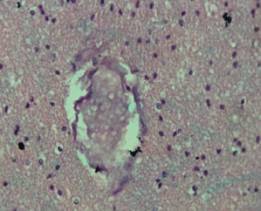
Рис.1.
Б-ной В., 22г. Стаж героиновой наркомании 3г. Парез и полнокровие микроциркуляторного
русла, эритроцитарно-фибриновые тромбы в капиллярах субкортикальных отделов
головного мозга при ДВС-синдроме.
Окраска
гематоксилин-эозин. х 100
Мы не ставили перед собой
цель исследовать головной мозг, т. к. достаточное количество работ подробно
описывает поражение ЦНС при хронической опиатной интоксикации, в частности в
работе К.Ш. Логуа, 1978г, на гистохимическом и электронно-микроскопическом
уровнях. В практике врача-патологоанатома подобное исследование практически невозможно.
Мы старались выявить органы-мишени при хронической наркотической интоксикации.
В
легких при микроскопическом исследовании, где стаж наркомании до 5 лет
деструктивных изменений характерных для длительной героиновой интоксикации не
обнаружено. Гистологическая картина соответствовала осложнениям основного
заболевания т. к. сепсис, тромбоэмболия. Но, наркоманы 1в группы, где стаж
героиновой интоксикации более 7 лет – обнаружены некоторые особенности редукции
артериоло-капиллярного русла, по типу посткапиллярной легочной гипертензии
(Рис.2).
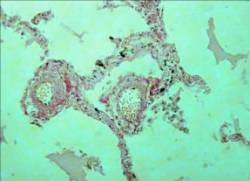
Рис. 2. Б-ной тот
же. Гипертрофия циркулярной мышечной оболочки мелких ветвей легочной артерии.
Окраска гематоксилин – эозин. х 200
Данная
патология, нам встречалась в 85% случаев в 1а и 1б подгруппах, связана с вено-артериальной
реакцией (редукцией оттока крови) – сокращение стенок артериол и мелких
артерий[13], в ответ на нарушение венозного оттока, являющейся проявлений
кардиомиопатии при хронической наркотической интоксикации.
При исследовании сердца и сосудов установлено
следующее. Дилатация камер
сердца, наблюдавшаяся в 32,4%
наблюдений, может быть связана как с фибрилляцией желудочков сердца, так и с
поражением сердечной мышцы кардиомиопатией токсического генеза. Первое
предположение подтверждается наличием
в 33% этих наблюдений гистологически подтвержденных очагов кардиосклероза, что
свидетельствует о значимости некоронарогенных механизмов возникновения фиброза
сердечной мышцы, а фиброз — предрасполагающий к развитию фибрилляции фактор.
Иные маркеры фибрилляции желудочков сердца в виде фрагментации контрактурно
поврежденных кардиомиоцитов, пареза микроциркуляции и очаговых острых
кровоизлияний встретились в 20,7% наблюдений (Рис. 3.) при том, что дистрофические изменения
кардиомиоцитов встретились в 59,2% случаев. При типичной окраске гематоксилином
и эозином отмечено неравномерное восприятие красителя, что свидетельствует о метаболических
повреждениях миокарда ишемического или иного генеза. Это заставляет предположить
наличие специфической наркогенной
кардиомиопатии, однако достоверные маркеры ее не были обнаружены нами.
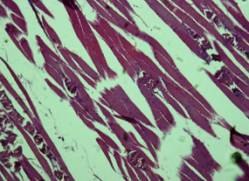
Рис. 3. Б-ной Е.,
21г. Стаж наркомании 4г. Парез микроциркуляторного русла, фрагментация
миокардиоцитов.
Окраска
гематоксилин – эозин. х 200.
Печень при макроскопическом исследовании была увеличена,
причем в 57,4% случаев наблюдался вес более 2000г. (гепатомегалия).
Макроскопические данные более всего соответствовали т. н. «большой красной
печени» (А.И. Струков, В.В. Серов, 1998г.). Из 242 умерших, страдавших
хронической героиновой наркоманией – у 161(66,2%) чел., подтверждено клинически,
инфицированность гепатотропной вирусной инфекцией - вирусный гепатит С /HCV-инфекция/. Но следует отметить, что
причиной смерти ни в одном случае, не являлась печеночная недостаточность. В
танатогенезе преобладали: сепсис, абсцедирующая пневмония, тромбоэндокардит
трехстворчатого клапана и травматизм. В группе сравнения исследовались умершие,
в основном при травматизме, где в анамнезе не зарегистрировано употребление
наркотика.
Гистологически практически
во всех случаях обнаружена картина хронического гепатита. Тип воспалительного
процесса трактовался как портальный гепатит, т. к. портальные тракты были
инфильтрированы макрофагами и лимфоцитами (в некоторых случаях с формированием
лимфатических фолликулов - в 35,7% наблюдений), местами в инфильтрате
присутствовали сегментоядерные лейкоциты (11,8%) и эозинофилы (49,3%). В части
наблюдений отмечено наличие распространения инфильтрации за пограничную
пластинку однако, крупные некрозы типа мостовидных обнаружены в 6,7%, где стаж
наркомании более 7 лет. Повсеместно преобладала над гидропической дистрофией
гепатоцитов – диссеминированная крупнокапельная жировая дистрофия в 37,2%
наблюдений (Рис.4.).
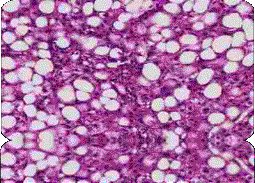
Рис.4. Б-ная Р.,
19 лет. Диссеминированная жировая дистрофия гепатоцитов при героиновой наркомании,
стаж употребления 4г. Окраска гематоксилин-эозин. х 400
Таким
образом, для печени при хронической наркотической интоксикации характерно
наличие в 100% наблюдений картины портального гепатита с участками разрушения
пограничной пластинки, капилляризацией синусоидов и различными видами фиброза,
а так же ранняя перестройка гистоархитектоники печени по типу монолобулярного
цирроза.
Весьма
распространены различные формы нефропатий. По данным некоторых авторов [4], 36 % героиновых
наркоманов страдают почечной патологией. Ультраструктурные изменения в ткани
почек находят у всех больных наркоманией. Они проявляются фокальными
утолщениями базальной мембраны эпителия почечных канальцев и отложением в ней
гомогенного гранулярного электронно-плотного материала. Клинически описаны 2
формы нефротического синдрома. 1-я характеризуется массивной протеинурией при
нормальной концентрации мочевины в крови. При 2-й форме происходит быстрое
ухудшение функции почек с неизбежной протеинурией.
В наших наблюдениях
поражение почек может быть вторичным по отношению к миоглобинурии (Рис.5).
Последнее состояние является следствием острого рабдомиолиза, развивающегося при употреблении
героина, в наших исследованиях он встречался у 29 больных (20,3%).
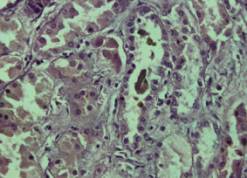
Рис. 5. Б-ная 26л.
Стаж героиновой наркомании 7 лет. Пигментный нефроз при миоглобинурии. Окраска
гематоксилин и эозин. х 160.
Имеются сообщения о появлении острого рабдомиолиза (Рис.6.)
при внутривенных инъекциях героина, когда уровни миоглобина в сыворотке крови
возрастают в 100 раз, а активность креатин-фосфокиназы превышает нормальные
значения в 700 раз [10].
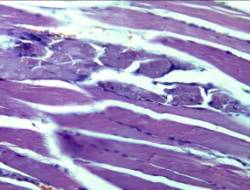
Рис.6. Б-ная та же. Очаговый рабдомиолиз икроножной мышцы.
Окраска гематоксилин и эозин. х 200
Обнаруженные изменения соответствуют фазе истощения
генерализованного адаптационного синдрома.
В наблюдениях сепсиса, прогрессирующего
фиброзно-кавернозного туберкулеза отмечались характерные морфологические
явления, которые не отличались специфичностью.
Таким
образом, наши данные позволяют выделить следующие варианты танатогенеза при
ХНИ:
1.
Танатогенез
по типу сердечной скоропостижной смерти, характеризующийся фибрилляцией
желудочков сердца, асистолией, что имеет свои морфологические маркеры.
2.
Танатогенез
по типу смерти от плюригландулярной дисфункции. Характеризуется морфологией
ДВС-синдрома в малом круге кровообращения и собственно картиной
геморрагического отека легких, а так же возможна, острая надпочечниковая
недостаточность, анафилактический шок и пр.) со своими морфологическими
маркерами.
3.Редкие виды танатогенеза (Однако, мы
должны признать, что на нашем материале зачастую имелось сочетание этих видов
танатогенеза и, таким образом, правомочно говорить об общей морфологической
картине хронического отравления при героиновой интоксикации.
Библиографический список:
1.
Барчуков
В.П., Калачев Б.Ф. Некоторые аспекты незаконного распространения наркотиков в
России. Вопр. наркол. – 1993. - №1. – С 56 -61.
2.
Боровиков
В.Т. STATISTICA. Искусство анализа данных на компьютере:
для профессионалов. 2-е изд. СПб: Питер, 2003. – 688с.
3.
Богомолов
Д.В. Судебно-медицинская диагностика наркотической интоксикации по
морфологическим данным: Дис. … д-ра мед. наук. – М., 2000.
4.
Веселовская
Н.В., Коваленко А.Е. Наркотики. М.: «Триада-Х», 2000. – 206 с.
5.
Кошкина
Е.А., Корчагина Г.А., Шамота А.З. Заболеваемость и болезненность алкоголизмом и
наркоманиями в Российской Федерации: Пособие для врачей психиатров-наркологов.
– М.: 2000. – 276 с.
6.
Логинов А.С.
Поражение печени наркотиками // Новые направления в гепатологии: Тез. междунар.
фальк симпозиума №92. – СПб., 1996. – С.41.
7.
Надточий
А.А., Юрченко О.И., Осташевская Н.Г. Некоторые вопросы патоморфологии при
опийной наркомании. // Сб.: 3-й всесоюзный съезд судебных медиков. М., 1988, с.
259-261.
9.Пиголкин Ю.И., Богомолов Д.В., Должанский О.В.,
Оздамирова Ю.М. Перспективы морфометрического анализа соматических поражений
при хронической наркотической интоксикации. В сб. Актуальные аспекты судебной
медицины. – 1999.- Вып. 5.- Ижевск. – «Экспертиза».- с. 171-173.
10. Abou-Khalil
B., Young A.B., Pennу J.B.
Evidence for the presynaptik localization of opiate binding sites on strial
efferent fibers.-Brain Res.-2004.- V.323.-Nr. 1. – p.21-29.
11. Bruton J., Charpak S. Heterogeneitу of cell
firing properties and opioid sensitivitу in the
thalamic reticular nucleus. Neuroscience.-1998.-May.-78(2). Pp.303-307.
12. Knapp P.E., Hauser K.F. mu-Opioid
receptor activation enhances DNA sуnthesis in immature oligodendrocуtes. Brain. Res. – 2006.-16.-743.-P. 1-2.
13. Nair M.R., Schwartz S.A., Polasani R.,
Hou J., Sweet A., Chadha K.C. Immunoregulatory effects of morphine on human
lymphocytes. Clinical & Diagnostic Laboratory Immunology., 2007.-4(2).-pp. 127-32.