Технические науки/1. Металлургия
К.х.н. Лобачева О.Л., к.х.н.
Джевага Н.В., к.х.н. Литвинова Т.Е.
Национальный
минерально-сырьевой университет «Горный»
Флотационное извлечение Eu(III) из нитратных сред
Применение РЗЭ в различных областях науки и техники является
показателем научно-технического развития тех или иных отраслей, способствует экономии
минерального сырья, улучшению экологической обстановки, обеспечению
национальной безопасности.
В
процессе ионной флотации катионов металлов [2], степень извлечения резко
возрастает в области pH гидратообразования. Предполагается, что ионная флотация
цветных металлов протекает с образованием их основных солей с анионными
поверхностно-активными веществами (ПАВ) [3]. Для установления механизма процесса
и прогнозирования оптимальных условий извлечения и разделения катионов металлов
методом ионной флотации необходимо знать рН образования гидроксокомплексов
металлов и рН гидратообразования, которые могут быть рассчитаны на основе
энергий Гиббса образования гидроксокомплексов и гидроксидов металлов.
Измерения
удельной электропроводности проводили с помощью кондуктометра марки «Анион
4100». С помощью иономера «Анион 7010» параллельно измеряли pH раствора. По
результатам строили кривую титрования, представленную на рисунке 1. Результаты
титрования с целью подтверждения их достоверности были дважды воспроизведены.
На
кривых кондуктометрического титрования выделяются следующие участки. Линейное
понижение удельной электропроводности обусловлено вследствие нейтрализации
азотной кислоты щелочью. На зависимости удельной электропроводности от объема
добавленной щелочи наблюдается резкий излом с переходом к почти горизонтальному
участку, что свидетельствует о связывании добавляемых гидроксид-ионов в
малодиссоциированное соединение.
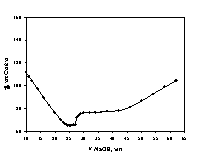
Рис.
1. Зависимость удельной электропроводности раствора Eu(NO3)3 от объема
раствора NaOH в ходе кондуктометрического и потенциометрического
титрования.
По количеству
миллиэквивалентов щелочи и изломов на кривых титрования определили образование моногидроксокомплексов
Eu(OH)2+ . Далее на кривых
титрования наблюдается почти линейный рост удельной электропроводности,
обусловленный избытком щелочи. Ионную флотацию катионов РЗЭ изучали из водного
раствора нитрата Ме(III) с концентрацией 0,001 моль·кг−1
с помощью додецилсульфата натрия (NaDS). Флотация проводилась
на лабораторной установке механического типа 137 В-ФЛ, с объемом камеры 1,0 дм3.
В водной фазе после флотации определяли концентрацию Me(III)
фотометрическим методом с арсеназо III [4] и DS- (С12H25OSO3-) путем
потенциометрического титрования 0,002 моль·дм−3 раствором
хлорида цетилтриметиламмония с ионоселективным электродом [5,6]. Экспериментальные
данные зависимости коэффициента распределения: 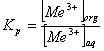 Eu(III)
из нитратных сред от рН раствора представлены на рисунке 2.
Eu(III)
из нитратных сред от рН раствора представлены на рисунке 2. 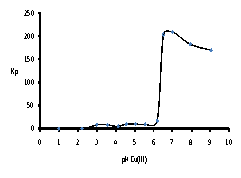
Рис.
2. Зависимость коэффициента распределения Кр ионов Eu3+ от рН раствора.
Значение
рН, при котором начинается резкое увеличение коэффициента распределения, равно
6,3 и соответствует данным кондуктометрического титрования рН образования
гидроксокомплекса Eu(III) 6,30±0,14. На этом
основании можно предположить, что Eu(III)
флотируется преимущественно в форме основного додецилсульфата гидроксоиттербия Eu(OH)(C12H25OSO3)2. При этом
достигается коэффициент распределения более 200. Максимальное извлечение происходит в области
рН образования гидроксидов, но в ходе эксперимента выпадение осадков не
наблюдали, что можно объяснить образованием в водной фазе устойчивых комплексов
гидроксокатионов с додецилсульфатом.
Термодинамические характеристики гидроксосоединений Eu(III)[6]
|
Соединение |
pHгидратообразования |
Соединение |
рНкомплексообразования |
|
Eu(OH)3 |
6,52 |
Eu(OH)2+ |
4,80 |
Литература:
1.
В.В.
Комольцев, Ф.Д. Ларичкин, А.А. Александров Конъюнктура рынка редкоземельных
металлов. / Цветная металлургия. 2004. №11. С.8-12.
2.
Grieves R.B., Charewicz W.R. Ion and
colloid flotation of Ni, Co and Pt // Separation Science. 1975. Vol.10. N 1. P.77-92.
3.
Gassett B.B., Otis J.S., Peter F.A.
The Influence of various parameters on foam separation / J.Water Pollution
Control Fed. 1965. V. 37. N 4. p. 460.
4.
С.Б. Савин Арсеназо III. / М.: Атомиздат. 1966.
265 с.
5.
С.В.Тимофеев,
В.А.Матерова, Л.К Архангельский. Электродное
поведение анионселективных мембран / Вестник ЛГУ. Серия физика, химия. 1978. №
16. Вып. 3. С. 139-141.
6.
Д.Э.
Чиркст, О.Л. Лобачева, И.В. Берлинский Извлечение и разделение ионов Се3+
и Y3+ методом ионной флотации. / Ж. Прикл. Хим. 2009. Т. 82. № 8.
С. 1273 - 1276.