Технічні науки / Металургія
Грицай В.П., Иванов В.И.,
Лукошников И.Е., Болюк С.В., Моисейко Ю.В.
Запорожская государственная инженерная академия
НЕКОТОРЫЕ
АСПЕКТЫ КОНВЕКЦИИ ПРИ ЭЛЕКТРОЛИЗЕ РАСПЛАВЛЕННЫХ СОЛЕЙ
На
механизм процесса перемещения ионов при электролизе расплавленных солей в электрохимической
ячейке значительное влияние оказывают возмущения, обусловленные образованием слоя
металла на катоде.
Процесс
катодного получения металла можно представить следующим образом. В расплаве
электролита присутствуют катионы двух- и трехвалентного основного металла, а
также анионы хлора. При отсутствии подвода разности потенциалов к
электрохимической ячейке система «электроды-электролит» находится в обратимом
термодинамическом равновесии, при ее наличии происходит активная миграция ионов
основного металла к катоду с последующим восстановлением на его поверхности. Повышение
температуры в электрохимической ячейке сопровождается термогравитационной
конвекцией, которая, в зависимости от конкретных условий, приводит к ускорению
или замедлению процесса электролиза. По мере восстановления ионов основного
металла существенно понижается его концентрация в расплавленном электролите
вблизи катода, а также плотность расплава, что способствует возникновению в нем
конвективных потоков.
В
условиях конвективного перемещения расплава предполагается осесимметричный
характер распределения в электрохимической ячейке переменных процесса: скорости, температуры и концентрации.
Движение электролита полагают установившимся и ламинарным, а расплав –
несжимаемым. Принимают, что теплофизические характеристики расплава не зависят
от температуры.
В
соответствии с принятыми допущениями математическое описание процесса сводили к
краевой задаче теории пограничного слоя и представляли в виде системы интегро-дифференциальных
уравнений гидродинамики, переноса теплоты и массы в безразмерном виде:
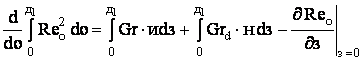 ; (1)
; (1)
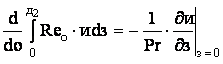 ; (2)
; (2)
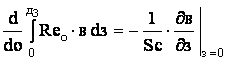 (3)
(3)
с соответствующими
начальными и граничными условиями.
Здесь Re, Gr, Grd, Pr, Sc - числа Рейнольдса, Грасгофа, Грасгофа
диффузионного, Прандтля и Шмидта; ![]()
![]() - безразмерные
температура и концентрация; d1, d2, d3 - толщина
гидродинамического, теплового и концентрационного пограничных слоев ; x, h - безразмерные координаты.
- безразмерные
температура и концентрация; d1, d2, d3 - толщина
гидродинамического, теплового и концентрационного пограничных слоев ; x, h - безразмерные координаты.
Решение краевой задачи и введение
обозначений ![]() ,
, ![]() ,
, ![]() позволяет получить систему обыкновенных
дифференциальных уравнений относительно толщины пограничных слоев:
позволяет получить систему обыкновенных
дифференциальных уравнений относительно толщины пограничных слоев:
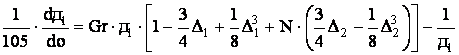 , (4)
, (4)
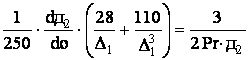 , (5)
, (5)
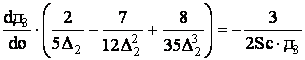 . (6)
. (6)
Для
упрощения задачи ограничивались случаем, когда D1 = 1. При совместном рассмотрении
уравнений (4) и (5) можно записать
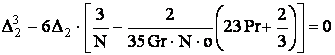 . (7)
. (7)
Решение
уравнения (7) имеет вид
![]() ,
(8)
,
(8)
где
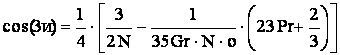 .
.
После
интегрирования уравнения (6) с учетом равенства (8), а также несложных
преобразований, получили зависимость толщины концентрационного пограничного
слоя от чисел, характеризующих физические переменные процесса:
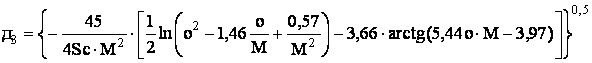 , (9)
, (9)
где М
= f(Gr,Pr,N).
Последующий
вычислительный эксперимент с использованием уравнения (9) в широком диапазоне
изменения числа Шмидта позволил установить отсутствие концентрационного
пограничного слоя в интервале изменения величины параметра xМ от 0 до 0,68. Полная
автомодельность данного параметра имеет место при его значениях более 1,2.
Результаты
исследования изменения соотношения гидродинамического и концентрационного
пограничных слоев по длине образующей катода свидетельствуют о быстром
завершении формирования данных слоев, и в дальнейшем это соотношение остается
постоянной величиной, которая определяется только значениями чисел Gr, Pr, Sc и N. При этом
установлено, что при увеличении значений числа N отношение указанных
пограничных слоев стремится к единице и при N = 2,5
наблюдается равенство толщины гидродинамического, теплового и концентрационного
пограничных слоев. Следовательно, необходимым условием достижения равенства
толщины пограничных слоев является организация движения ионов в расплаве, при
котором скорость их перемещения становится равной или в 2,5 раза превышает
скорость перемещения расплава электролита, т.е. Grd ³ Gr.
Реализация
такого уровня скоростей перемещения ионов в расплаве достигается повышением
плотности тока. Его величину можно рассчитать по формуле:
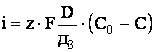 , (10)
, (10)
где ![]() - валентность
ионов основного металла;
- валентность
ионов основного металла; ![]() - число
Фарадея;
- число
Фарадея; ![]() - коэффициент
диффузии ионов; Со, С -
концентрация ионов основного металла и расплаве и на поверхности катода
соответственно.
- коэффициент
диффузии ионов; Со, С -
концентрация ионов основного металла и расплаве и на поверхности катода
соответственно.
В
случае, когда d1 = d2 = d3, соотношение (10)
можно преобразовать в выражение
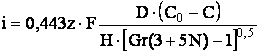 . (11)
. (11)
Рассмотрение
выражения ![]() позволяет определить пределы
максимального выхода основного металла по току, т.е.
позволяет определить пределы
максимального выхода основного металла по току, т.е.
![]() , (12)
, (12)
откуда
![]() .
(13)
.
(13)
Таким
образом, при наличии электрического поля в электрохимической ячейке, а также
значений чисел Грасгофа, определяемых соотношением (13), имеет место совместная
термогравитационная и концентрационная конвекции. При этом противоположное
направление перемещения расплава электролита и диффузии ионов основного
металла, создаваемое действием обоих видов конвекции (N < 0),
способствует возрастанию плотности тока электролиза, а совпадение направлений их
перемещения (N > 0) - снижению ее величины.