КИНЕТИКА СЕРНОКИСЛОТНОГО ИЗВЛЕЧЕНИЯ БЕРИЛЛИЯ ИЗ
МЕХАНОАКТИВИРОВАННОГО БЕРИЛЛА
Оналбаева Ж.С., Самойлов В.И.
«Восточно-Казахстанский государственный
технический университет
им. Д. Серикбаева», (г. Усть-Каменогорск,
Казахстан)
В гидрометаллургии бериллия затраты на активацию берилла перед его вскрытием
серной кислотой оцениваются ~22 % от суммарных затрат на переработку сырья
до технического гидроксида бериллия; активирующая подготовка берилла включает
его энергоемкую плавку с дорогостоящими флюсами, водную грануляцию плава с
последующим измельчением плава-гранулята [1]. Поэтому актуальной является
задача удешевления процесса активирующей подготовки берилла путем применения
менее затратной механоактивации данного силиката.
Известен [1] способ прямого сернокислотного вскрытия берилла полностью
исключающий затраты на активирующую подготовку данного силиката. Недостатками
способа прямого вскрытия берилла является высокий расход серной кислоты в процессе растворения берилла в
реакторе (многократно превышающий стехиометрическое значение) и большая
продолжительность процесса (40 ч). Получаемый при таком сернокислотном
растворении берилла раствор содержит сотые доли граммов бериллия в литре, что
очень мало для промышленной реализации этой технологии (требуемая концентрация
бериллия в растворе должна составлять несколько граммов в литре). Для
нейтрализации серной кислоты при промышленном использовании данного способа
вскрытия берилла потребуется огромное количество дорогостоящего раствора
аммиака. Кроме того, трудно представляется дальнейшая переработка раствора
сульфата бериллия, загрязненного большим количеством кремния.
Для устранения указанных недостатков был предложен промышленный способ
вскрытия берилла в трубчатой вращающейся печи сульфатизации [2], основанный
на применении механоактивированного берилла.
Концентрат механоактивировали в течение 30 мин в лабораторной
планетарной мельнице (рис.1) АИР-0,015М (разработка института «Гидроцветмет»,
Новосибирск) в следующих условиях: диаметр стальных мелющих шаров 5 мм,
массовое соотношение шары : концентрат – 50 : 1, три помольных барабана,
центростремительное ускорение по оси барабана 350 м/с2, объёмная
шаровая загрузка барабанов – 60 %.
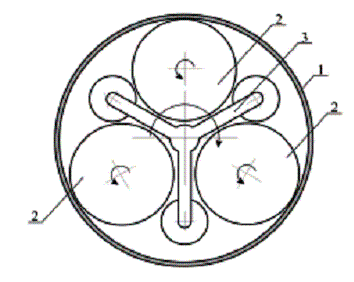
1 – корпус мельницы; 2 –
барабан с шарами; 3 – водило с тремя роликами
Рисунок 1 – Схема работы планетарной мельницы (вид сверху)
Рентгеноструктурный
анализ концентрата показал (рис. 2), что его измельчение в планетарной мельнице
даёт полное разрушение кристаллических решёток минералов, входящих в состав бериллового
концентрата.
Вместе с тем кинетика
предложенного в диссертации [1] способа до настоящего времени не изучена. Для
восполнения указанного пробела нами исследованы кинетические зависимости,
которым подчиняется данный процесс. В частности,
определена степень извлечения бериллия из берилла в водорастворимый
сульфат бериллия при различных температурах и продолжительностях
выщелачивания минерала.
Исследования
выполнены с использованием берилла крупностью -10 мкм с содержанием оксида
бериллия 11 % масс. Навески минерала массой 500 мг (55 мг по оксиду бериллия) обрабатывали 0,8 мл 69
% серной кислоты и образовавшуюся реакционную массу выдерживали в течение 9 ч при температуре
240÷300 °С, перемешивая её каждые 1÷2 ч.
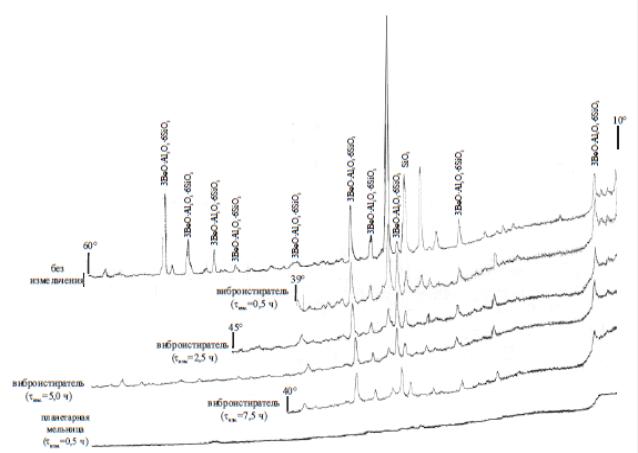
Рисунок 2 – Результаты рентгеноструктурного
анализа бериллового концентрата в диапазоне углов отражения от 10 до
60°, механоактивированного в течение различного времени (τизм.)
Затем сульфатизированный берилл
выщелачивали водой 20 мин
при Т:Ж=1:5 по исходному бериллу,
95 ºС. Пульпу выщелачивания фильтровывали, остаток от выщелачивания
подвергали двукратной
фильтр-репульпационной отмывке от сульфата бериллия (Т:Ж, температура и
продолжительность каждой из отмывок составляли 1:7 по исходному бериллу, 95 ºС и 15 мин). Отмытый остаток от
выщелачивания высушивали до постоянно веса и анализировали на содержание оксида
бериллия фотонейтронным методом.
Результаты
экспериментов, представленные в таблице 2, показали, что промышленно-приемлемое
извлечение бериллия в раствор (~90 %) достигается за 9 ч сульфатизации концентрата при 300 °С.
Таблица 2 – Зависимость извлечения Ве в
раствор от температуры сульфатизации (продолжительность сульфатизации – 9 ч)
|
Темпера-тура, °С |
Остаток выщелачивания |
Извлечение Ве в раствор, % |
|
|
Масса, мг |
Содержание ВеО, % масс. |
||
|
300 |
350 |
1,78 |
88,9 |
|
280 |
350 |
2,24 |
86,1 |
|
260 |
375 |
2,60 |
82,6 |
|
240 |
375 |
3,09 |
79,3 |
На следующем этапе работ определяли
степень извлечения бериллия из берилла в водорастворимый сульфат бериллия,
но при различных
продолжительностях сульфатизации (τ) и её температурах (Т). Полученные данные приведены в таблице 3 и с использованием табличного процессора Excel графически представлены на
рисунке 3.
Таблица 3 – Зависимость извлечения бериллия в раствор от
продолжительности и температуры сульфатизации берилла
|
τ, ч |
Остаток выщелачивания |
Извлечение Ве в раствор, %
|
|
|
Масса, мг |
Содержание ВеO, % масс. |
||
|
Температура сульфатизации 300 °С |
|||
|
3,0 |
350 |
4,80 |
70,0 |
|
6,0 |
350 |
2,32 |
85,5 |
|
9,0 |
350 |
1,78 |
88,9 |
|
Температура сульфатизации 280 °С |
|||
|
3,0 |
345 |
5,11 |
68,5 |
|
6,0 |
345 |
2,86 |
82,4 |
|
9,0 |
350 |
2,24 |
86,1 |
|
Температура сульфатизации 260 °С |
|||
|
3,0 |
350 |
5,36 |
66,5 |
|
6,0 |
360 |
3,28 |
78,9 |
|
9,0 |
375 |
2,60 |
82,6 |
|
Температура сульфатизации 240 °С |
|||
|
3,0 |
360 |
5,66 |
63,6 |
|
6,0 |
365 |
3,98 |
74,0 |
|
9,0 |
375 |
3,09 |
79,3 |
τ, ч Извлечение Ве в раствор,
%
![]()
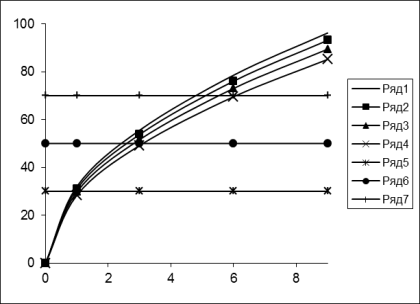
Рисунок 3 – Зависимости извлечения бериллия из берилла от
продолжительности и температуры его сульфатизации; ряды: 1
– 300 °С, 2 – 280 °С, 3
– 260 °С, 4 –240 °С, 5, 6 и 7 – вспомогательные прямые, соответствующие
извлечению бериллия в раствор
30, 50 и 70 %
С помощью
полученных графиков определены продолжительности сульфатизации, обеспечивающие
одинаковое извлечение бериллия в раствор (30, 50 и 70 %) при различных
температурах; полученные значения и результаты их обработки представлены в
таблице 4 и далее использованы для оценки кажущейся энергии активации взаимодействия берилла с серной кислотой. Для этого определяли
зависимости логарифма времени, необходимого для достижения одинаковой степени
извлечение бериллия в раствор при разных температурах его сульфатизации,
от обратной температуры, которая представлена на рисунке 4.
Угловые коэффициенты прямых lgτ = f(1/Т) связаны со
значением кажущейся энергии активации соотношением d(lgτ)/d(1/Т) = Eкаж./(2,3R) [3]. Для извлечений бериллия в раствор 30, 50 и 70 % угловые
коэффициенты равны соответственно 520,977; 520,973 и 520,977; кажущуюся энергию
активации рассчитывали по среднему значению, равному 520,976. Величина кажущейся энергии активации реакции берилла с серной кислотой составила
10,0 кДж/моль.
Таблица 4 – Продолжительность сульфатизации
берилла, обеспечивающая заданное извлечение бериллия в раствор при различных температурах
|
Т |
1/Т, К-1 |
τ, ч |
τ, мин |
lg τ |
|
|
°С |
К |
||||
|
Извлечение в раствор 30 % |
|||||
|
300 |
573 |
0,001745 |
0,874390 |
52,46340 |
1,719856 |
|
280 |
553 |
0,001808 |
0,933071 |
55,98426 |
1,748066 |
|
260 |
533 |
0,001876 |
1,012294 |
60,73764 |
1,783458 |
|
240 |
513 |
0,001949 |
1,116281 |
66,97686 |
1,825925 |
|
Извлечение в раствор 50 % |
|||||
|
300 |
573 |
0,001745 |
2,428861 |
145,7317 |
2,163554 |
|
280 |
553 |
0,001808 |
2,591863 |
155,5118 |
2,191763 |
|
260 |
533 |
0,001876 |
2,811926 |
168,7156 |
2,227155 |
|
240 |
513 |
0,001949 |
3,100782 |
186,0469 |
2,269622 |
|
Извлечение в раствор 70 % |
|||||
|
300 |
573 |
0,001745 |
4,760568 |
285,6341 |
2,455810 |
|
280 |
553 |
0,001808 |
5,080052 |
304,8031 |
2,484019 |
|
260 |
533 |
0,001876 |
5,511376 |
330,6826 |
2,519411 |
|
240 |
513 |
0,001949 |
6,077532 |
364,6519 |
2,561879 |
(1/Т)∙10-3 lg τ
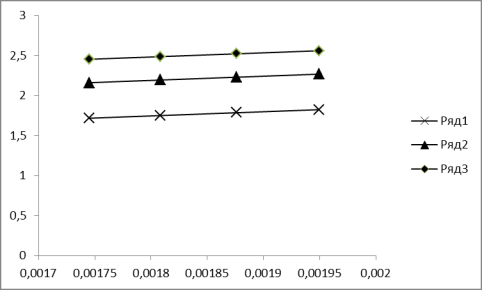
Рисунок 4 – Зависимости логарифма
продолжительности сульфатизации от её обратной температуры при извлечении бериллия 30 % (ряд 1), 50 % (ряд 2)
и
70 % (ряд 3)
Рассчитанное значение Eкаж. свидетельствует о том,
что исследованный процесс протекает в
диффузионной области. Поэтому можно предположить, что данный процесс
лимитируется скоростью диффузии молекул кислоты к реакционной поверхности через
слой образующихся продуктов реакции.
Список использованных источников
1 Самойлов В.И. Технологические процессы комплексной переработки бериллийлитиевого
минерального сырья: Дис. … докт. техн. наук. Екатеринбург, 2010. – 465 с.
2 Самойлов В.И. Экспериментальная разработка
перспективных химических методов
извлечения бериллия и лития из минерального сырья. – Усть-Каменогорск:
Медиа-Альянс, 2006. – 551 с.
3 Вольдман Г.М., Зеликман А.Н. Теория гидрометаллургических процессов.
– М.: Интермет Инжиниринг, 2003. – 424 с.