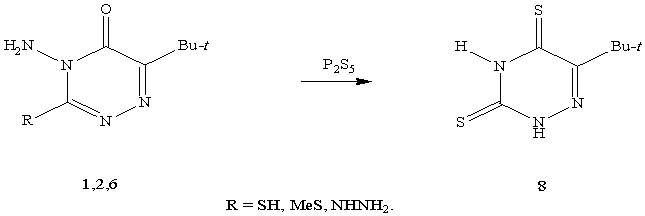Химия и химическая
технология /6.Органическая химия
Д.х.н. Миронович Л.М., Будыкина Д.В., Разиньков Д.Ю.
Юго-Западный государственный университет, г. Курск, Россия
РЕАКЦИОННАЯ СПОСОБНОСТЬ ПРОИЗВОДНЫХ 1,2,4-ТРИАЗИНА В РЕАКЦИЯХ
НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ
Реакционная способность производных
1,2,4-триазина интенсивно исследуется в связи с проявлением его производных
биологической активности. Среди производных 1,2,4-триазина, имеющих аминогруппу
в положении 4 триазинового кольца, найдены и широко применяются в сельском
хозяйстве в качестве гербицидов против сорных растений в посевах сои (зенкор),
картофеля (метаметрон). Широко известен препарат цефтриаксон, имеющий в своем
составе триазиновое кольцо, являющийся антибиотиком цефалоспоринового спектра действия. В качестве
противовирусного препарата применяют триазаверин. В последнее время много публикаций посвящено препарату
ламотриджину, оказывающему противосудорожное действие. Среди производных 1,2,4-триазина
особое место занимают 4-амино-1,2,4-триазины, имеющие несколько реакционных
центров: амино-, оксо-, тиоксогруппы и атомы азота гетероцикла. Наличие
функциональных групп позволяет проводить функционализацию производных
1,2,4-триазина и получать новые бициклические гетероциклические соединения.
Замыкание цикла проходит с участием атомов азота кольца [1].
Целью данного исследования явилось изучение
реакционной способности 4-амино-6-трет-бутил-5-оксо-3-тиоксо-2Н-1,2,4-триазина в реакциях нуклеофильного
замещения оксо-, тиоксо-, гидразиновых групп.
В качестве объекта исследования выбран
4-амино-6-трет-бутил-5-оксо-3-тиоксо-2Н-1,24-триазин (1), полученный
конденсацией тиокарбгидразида с калиевой солью триметилпировиноградной кислоты
при кипячении в щелочной среде.
Тиоксогруппа
в положении 3 гетероцикла легко замещается на гидразиновую группу. При
кипячении соединения 1 с гидразингидратом (85 %-ным) в спиртовой среде
получен 4-амино-6-трет-бутил-3-гидразино-5-оксо-1,2,4-триазин (2). Замещение тиоксо(метилмеркапто)группы
на гидразиновую группу проходит через образование комплекса Мейзенгей мера. Гидразиновая группа в положении 3
гетероцикла вступает в обычные реакции с карбонильными соединениями. При
кипячении соединения 2 с кетонами получены соответствующие N-(метил-R-метилиден)-N1-(4-амино-6-трет-бутил-5-оксо-1,2,4-триазин-3-ил)гидразины
(3-5). В условиях эксперимента аминогруппа в положении 4 триазинового кольца не
вступает в реакции с кетонами, что не противоречит литературным данным [1].
Увеличение стехиометрического количества кетона (1:2, 1:3) приводит к выделению
только продуктов 3-5. Реакции проводили в неполярном растворителе.
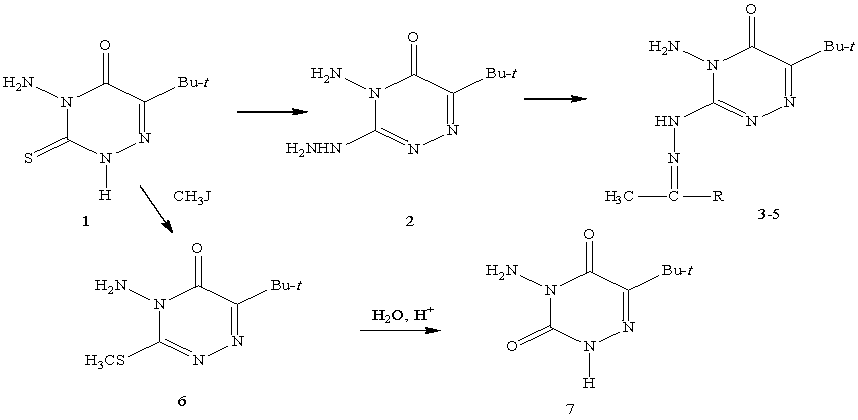
Метилирование 4-амино-6-трет-бутил-5-оксо-3-тиоксо-2Н-1,2,4-триазина
(1) иодистым метилом в водно-спиртовом растворе щелочи приводит к 4-амино-6-трет-бутил-3-метилмеркапто-5-оксо-1,2,4-триазину
(6).
Метилмеркаптогруппа гидролизуется в кислой среде
с образованием 4-амино-6-трет-бутил-3,5-диоксо-2Н-1,2,4-триазина (7). Реакцию проводят
при нагревании в водной кислой среде.
Структура соединений 3-7 установлена по
совокупности данных элементного анализа, ИК-, ЯМР-1Н -спектроскопии.
В спектрах ЯМР-1Н имеются синглеты протонов трет-бутильного заместителя при 1,28-1,32 м.д.; при 1,92-2 м.д.
расположены синглеты метильной группы (соединения 3-5), а при 2,54 м.д. синглет
метилмеркаптогруппы (соединение 6); мультиплет фенильного заместителя
расположен при 7,8-8,2 м.д.
В ИК спектрах соединений 1-7 валентное колебание
карбонильной группы в положении 5 триазинового кольца находится при 1632-1680
см-1. При 1705 см-1 расположено валентное
колебание карбонильной группы в положении 3 гетероцикла соединения 7.
Кипячение соединений 1,2,6 в пиридине с
пентасульфидом фосфора приводит к замещению оксо-, тиоксо-, метилмеркапто-,
гидразиновой групп на тиоксогруппу с одновременным отщеплением аминогруппы в
положении 4 триазинового кольца. Во всех случаях получено желтое
кристаллическое вещество, которое по данным элементного анализа, ИК- ЯМР 1Н,
масс-спектрометрии идентифицировано как 6-трет-бутил-3,5-дитиоксо-2Н,4Н-1,2,4-триазин
(8).
Литература
1.Миронович
Л.М., Промоненков В.К. Итоги науки и техн.
ВИНИТИ. Сер. Орг. Хим. 1990, 22, 267 с.