Міськів О.В., Нагорна
С.Ю.
Дніпродзержинський державний технічний університет
Залежність якості сульфату амонію від інтенсивності магнітної обробки маточного розчину
Сульфат
амонію – прозора кристалічна речовина, питома вага якої становить 1769 кг/м3,
містить 21,2% азоту або 25,8% аміаку,
24% сірки, яка у вигляді сульфат-іона надходить в ґрунт разом з добривом. У світовому
виробництві азотних добрив на долю сульфату амонію припадає більше 20% від всього виробництва
зв’язаного азоту, в нашій
країні 6-7% від всієї кількості азотних добрив, що випускаються. Цінність цього
добрива обумовлена високим вмістом азоту, в порівнянні з іншими азотними
добривами (чилійською
селітрою NаNO3, що
містить 15-16%,
норвезькою селітрою Ca(NO3)2, що містить 13-14% і природним добривом,
що містить 6-7% азоту); азот добре
засвоюється з ґрунту
корінням рослин. Сірка, що міститься
в сульфаті амонію, є
необхідним елементом живлення
для багатьох сільськогосподарських культур (буряка, бавовника, тютюну і ін.),
тому сульфат амонію можна вважати за добриво, що містить|утримує| живильних речовин більше
45% і що володіє високими агротехнічними властивостями.
Для
характеристики сульфату амонію як добрива велике значення має розмір його
кристалів. Дуже дрібні кристали легко розносяться вітром і у ґрунті
розподіляються нерівномірно. Дрібні кристали важче відділити від вологи, вони
легко злежуються, утворюють грудки, що також ускладнює їх введення у ґрунт.
Нами вивчені
можливості дії на процес кристалізації солі магнітним полем різної напруженості
для досягнення кінцевої мети – отримання крупнокристалічного добрива.
Виготовлена лабораторна установка моделююча промислову схему отримання сульфату
амонію за сатураторним способом (див.
рис. 1).
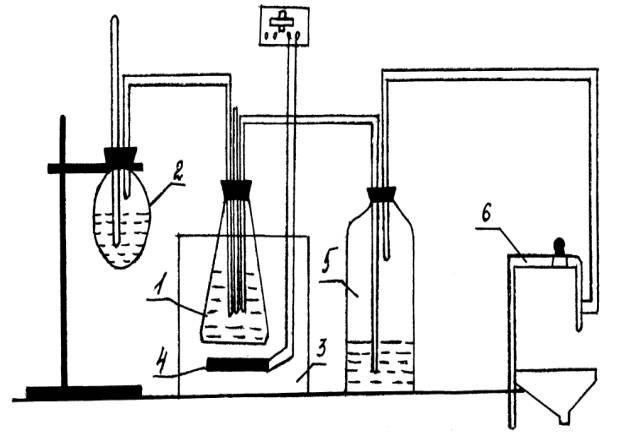
1 – нейтралізатор; 2 – колба з
розчином аміаку; 3 – термостат; 4 – нагрівач; 5 – поглинача залишкового аміаку; 6 – патрубок вакуумної
системи
Рисунок 1 – Схема лабораторної установки для
отримання сульфату амонію
Нейтралізацію розчину сірчаної кислоти проводили сумішшю аміаку і повітря, яку
отримували в процесі просмоктування повітря за допомогою вакуумної системи через 25%-вий
розчин аміаку. Нейтралізатор 1 встановлювали
у термостат 3, у якому за допомогою
нагрівача підтримували задану температуру.
Перед завантаженням суміші в нейтралізатор її
піддавали магнітній обробці на апараті УЕМ-1Т (універсальний
електромагніт) за різних напруженості магнітного поля та часу омагнічування.
У ході проведення дослідів виконали ряд визначень, а саме, кислотність маточного
розчину, концентрацію розчинів сірчаної кислоти (фільтрату) й аміаку до і після
експерименту за відомими методиками, прийнятими при поточному контролі якості
хімічних продуктів коксування.
В процесі досліджень провели чотири серії дослідів, які відрізняються один від одного напруженістю
та часом омагнічування розчину.
Результати дослідів наведені у таблицях 1 і 2.
Таблиця 1 – Залежність гранулометричного складу сульфату амонію від часу
обробки маточного розчину в магнітному полі
|
Найменування показників |
Час омагнічування, хв. |
|||
|
не ом. |
1 |
5 |
15 |
|
|
1.
Температура проведення досліду, °C |
58 |
58 |
52 |
48 |
|
2.
Кислотність маточного розчину, % |
4,4 |
4,5 |
4,2 |
4,1 |
|
3. Маса
отриманої солі, г |
11,3 |
17,1 |
22,2 |
28,3 |
|
4.
Гранулометричний склад, %, класи, мм > 1 мм 0,2 – 1,0 мм 0,16 – 0,2 мм 0,1 – 0,16 мм < 0,1 мм |
17,7 7,1 11,8 29,1 34,3 |
34,2 14 15,2 19,4 17,2 |
40,6 18 19,9 11,5 10 |
45,8 21 21,1 7,1 5 |
Таблиця 2 –
Залежність гранулометричного складу сульфату амонію від інтенсивності магнітної
обробки маточного розчину
|
Напруженість магнітного поля,
А/м∙104 |
Гранулометричний склад, %,
класи, мм |
||||
|
не омагнічений 4,0 8,0 12 |
> 1,0 |
0,2-1,0 |
0,16-0,2 |
0,1-0,16 |
< 0,1 |
|
17,7 34,2 40,6 45,8 |
7,1 14 18 21 |
11,8 15,2 19,9 21,1 |
20,1 13,4 9,5 7,1 |
25,3 11,2 8 5 |
|
Аналіз даних
дає підстави стверджувати, що зміна
напруженості магнітного поля та часу омагнічування розчину впливає на процес
отримання сульфату амонію, зокрема, його кристалізацію.
Розглядаючи
характер зміни розподілу вузьких класів крупності сульфату амонію отриманого з
необробленого та обробленого в магнітному полі різної напруженості маточного
розчину, можна зробити наступний висновок.
Сульфат
амонію, отриманий з неомагніченого маточного розчину, представлений в основному
класами крупності 0,16-0,1 мм і менше,
при цьому в ньому міститься відносно велика кількість тонкодисперсних класів
менше 0,1 мм, що є небажаним, оскільки збільшує злежуваність продукту і
утрудняє внесення його в ґрунт.
При цьому
магнітна обробка маточного розчину у всіх досліджуваних випадках сприяє
збільшенню вмісту найкрупніших класів і зменшенню тонко дисперсних (див. рис.
2). Найкрупніші кристали сульфату амонію отримані при обробці магнітним полем напруженістю
12∙104 А/м та часу дії 15 хв.
Таким чином,
для отримання бажаної крупності кристалів сульфату амонію в досліджуваному
діапазоні зміни напруженості магнітного поля обробка маточного розчину повинна
проводитися в межах напруженості
8∙104 – 12∙104 А/м при часу
омагнічування довше 5 хв.
Звертає увагу
на себе також той факт, що знижується температура утворення сульфату амонію та
збільшується маса отриманої солі. При зіставленні абсолютних величин цих
показників в сульфаті амонію, отриманого за традиційною технологією (без
омагнічування маточного розчину) і при омагнічуванні (діапазон зміни тривалості
1, 5 та 15 хв. при напруженості від
4∙104 до 12∙104 А/м відповідно) видно, що в
першому випадку температура випадіння кристалів в осад склала 58 ºC і при
цьому утворилося 11,3 г солі, а у другому – температура знижувалась з 58
ºC до 48 ºC, а маса утвореного сульфату амонію збільшувалась з 17,1
до 28,3 г. Вказаний ефект є позитивним, так як температура – це один з вагомих
факторів, який впливає на якість та вихід сульфату амонію. Кислотність під час
проведення дослідів підтримувалась в межах 4-5%.
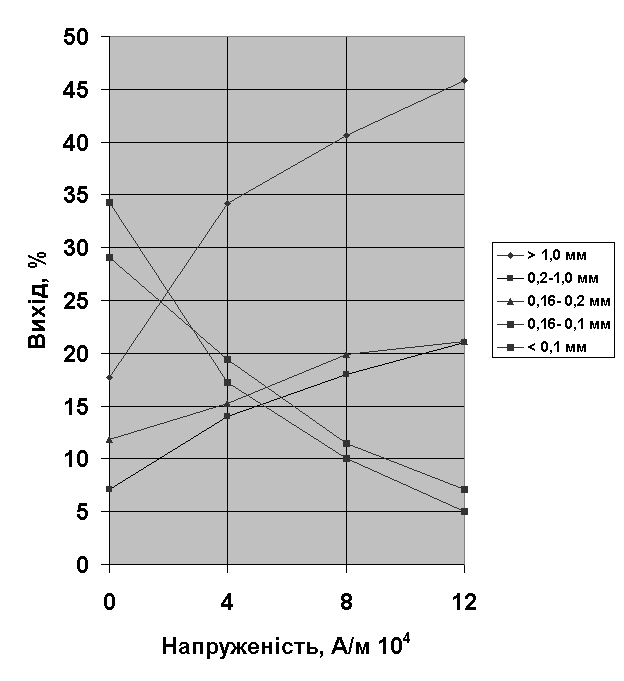
Рисунок 2 – Залежність
фракційного виходу кристалів сульфату амонію від напруженості магнітного поля