Биологические науки/9.Биохимия и биофизика
Рымко А.Н., Саунин А.В.*,
Коровашкина А.С.,
Зинченко А.И.
Институт микробиологии НАН Беларуси, Минск
*Международный государственный экологический университет
им. А.Д. Сахарова, Минск
ИСПОЛЬЗОВАНИЕ КОМПЛЕКСОВ СЛОИСТОГО ДВОЙНОГО ГИДРОКСИДА ДЛЯ ИММОБИЛИЗАЦИИ
ПЛАЗМИД, ОБОГАЩЕННЫХ CpG-МОТИВАМИ
Как известно, бактериальная ДНК (наряду с
другими бактериальными патоген-ассоциированными молекулярными структурами),
способна активировать разделы врожденного и адаптивного иммунитета человека и
животных. Эта активность обусловлена присутствием в молекуле бактериальной ДНК
неметилированных CpG-динуклеотидов. Особые участки
ДНК, содержащие такие динуклеотиды (CpG-мотивы),
распознаются одним из классов Toll-подобных
рецепторов (TLR9) на иммунокомпетентных
клетках и инициируют каскад сигнальных реакций, который приводит к активации
механизмов сначала врожденной, а затем и адаптивной ветвей иммунитета [1].
Созданные с применением
генно-инженерной техники препараты плазмидной ДНК (пДНК), обогащенной
CpG-мотивами (CpG-пДНК),
являются перспективными средствами для лечения многих заболеваний, но ввиду
низкой стабильности пДНК в русле крови, необходима разработка эффективных
способов её доставки в клетки-мишени.
Среди кандидатов в переносчики
пДНК рассматриваются неорганические слоистые двойные гидроксиды (СДГ), из-за своей
низкой токсичности, высокой емкости и повышенной способности проникать в клетки
[2].
По химической природе СДГ –
класс анионных глин. Их структуру описывают в виде металл-гидроксидных слоев, в
которых часть дивалентных катионов изоморфно замещена на катионы тривалентные, что
приводит к возникновению на слоях положительных зарядов. Эти заряды компенсируются
за счет интеркаляции гидратированных анионов в межслойное (галерейное) пространство
[3].
Целью настоящей работы явилось изучение
возможности получения комплекса СДГ с CpG-пДНК.
Материалы и
методы. CpG-пДНК получали, как описано нами ранее
[4].
Нитратную
форму СДГ (MgAl/NO3-СДГ) синтезировали методом, описанным в работе [5].
Для
синтеза комплекса СДГ с CpG-пДНК ионообменной реакцией к 600 мкл полученной выше суспензии MgAl/NO3-СДГ добавляли 5 мкг CpG-пДНК, реакцию проводили в течение 1 сут, при умеренном перемешивании, без
доступа воздуха и нормальных условиях.
Для
синтеза комплекса СДГ с CpG-пДНК методом соосаждения к 300 мкл 0,05 М раствора NH4OH, содержащего 5 мкг CpG-пДНК, покапельно и при постоянном
интенсивном перемешивании добавляли 300 мкл раствора, содержащего 0,02 М MgCl2 и 0,01 М Al(NO3)3.
Дальнейшая процедура полностью повторяла описанную выше процедуру синтеза
нитратной формы СДГ. Эффективность интеркаляции ДНК в состав СДГ оценивали спектрофотометрически.
Для
элюции плазмиды из комплекса с СДГ к его суспензии прибавляли 0,1 М калий-фосфатный
буфер (КФБ) со значениями pH 3,0 и 7,0. За ходом элюции следили на протяжении 1
ч. Степень элюции CpG-пДНК определяли по значению оптической плотности
супернатанта (λ=260 нм).
Приведенные в работе экспериментальные
данные представляют собой доверительные интервалы среднего арифметического для
95%-ного уровня вероятности.
Результаты
и обсуждение. В настоящее время комплексы
биомолекул с СДГ получают, как правило, двумя методами: соосаждением [6] и
ионным обменом [7].
Как видно
из таблицы 1, связывающая способность СДГ в отношении ДНК сильно зависит от
метода получения комплекса.
Таблица 1
Иммобилизационные свойства СДГ по
отношению к ДНК при разных способах получения комплексов СДГ-ДНК
|
Метод иммобилизации ДНК |
Эффективность связывания ДНК, мкг ДНК/мг СДГ |
|
Соосаждение |
830±90 |
|
Ионный обмен |
490±40 |
Так, при
использовании метода соосаждения, емкость СДГ по отношению к ДНК в 1,7 раза
больше, чем при использовании метода ионного обмена.
Следующим
этапом исследования было изучение динамики элюции CpG-пДНК из комплекса с СДГ при различных
значениях рН. Как видно из рисунка 1, освобождение
пДНК из комплекса с СДГ при нейтральном значении рН не отличается от скорости
освобождения при кислых значениях рН.
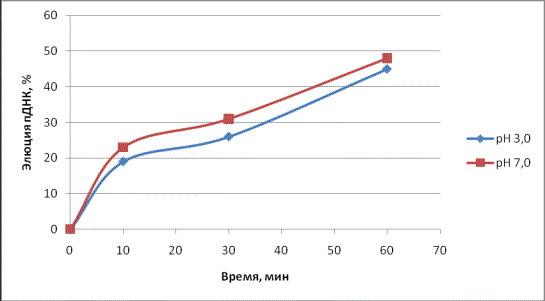
Рисунок 1. Динамика элюции CpG-пДНК из комплекса с СДГ в
0,1 М КФБ при различных значениях рН
Элюция CpG-пДНК
из комплекса с СДГ, предположительно, обязана не разрушению СДГ (что
свойственно комплексам, содержащим низкомолекулярные соединения), а протеканию
ионообменной реакции с замещением пДНК на неорганический фосфат, присутствующий
в буфере. Следует отметить, что визуально не наблюдалось растворения белого
осадка комплекса СДГ с CpG-пДНК при рН
равным 3,0, что еще раз подтверждает предположение о преимущественном
ионообменном механизме элюции ДНК из комплекса.
Такое атипичное поведение комплекса при
низких значениях рН, скорее всего, объясняется природой иммобилизованной
молекулы ‒ высокополимерной ДНК.
Элюция
ДНК из комплекса СДГ с CpG-пДНК также зависит и от объёма элюирующего буфера. Так, при увеличении
объема 0,1 М КФБ, увеличивается и степень элюции CpG-пДНК. Данная зависимость отражена на рисунке 2.
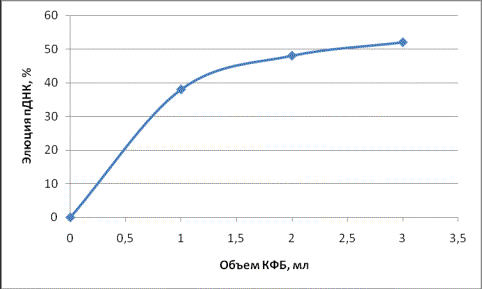
Рисунок 2. Зависимость элюции
CpG-пДНК из комплекса с СДГ от объема 0,1 М КФБ (рН 7,0)
Таким образом, в ходе
проделанных экспериментов были впервые получены устойчивые комплексы СДГ с CpG-пДНК различными методами. Показано преимущество метода соосаждения для
иммобилизации CpG-пДНК на СДГ. Отражена динамика элюции CpG-пДНК
из комплексов с СДГ в буферный раствор при различных значениях рН. Продемонстрирована
зависимость элюции CpG-пДНК из комплекса с СДГ от объема элюента.
Литература:
1.
Krieg, A.M. CpG motifs in bacterial DNA and their immune effects / A.M.
Krieg // Annu. Rev. Immunol. ‒ 2002. ‒ Vol. 20. ‒ P. 709‒760.
2. Choi, S.J. Anticancer drug-layered hydroxide
nanohybrids as potent cancer chemotherapy agents /
S.J. Choi, J.M. Oh, J.H. Choy // J. Phys. Chem. Solids. ‒2008. ‒Vol.
69, № 5-6. ‒P. 1528–1532.
3. Sugar–anionic clay composite
materials: intercalation of pentoses in layered double hydroxide /
S. Aisawa [et al.] // J. Solid State Chem. ‒ 2003. ‒ Vol. 174, № 2.
‒ P. 342–348.
4.
Коровашкина, А.С. Создание штамма
Escherichia coli ‒ продуцента плазмидной ДНК, обогащенной
иммунотропными СрG-мотивами
/ А.С. Коровашкина, С.В. Квач, А.И. Зинченко // Стремления ‒ 2011: сб. материалов
II Междунар. научн.-практ. конф. мол. ученых,
Минск, 14-18 ноября 2011 г. Минск, Беларуская наука, 2011. ‒Т.1. ‒ С.
184‒187.
5. Иммобилизация
диаденозинтетрафосфата включением в слоистый двойной гидроксид / Д.В. Бурко [и
др.] // Wschodnia spolka–2009: materialy V Miedzynarodowej naukowi-praktycznej konferencji,
Przemysl, 07–15 wrzesnia 2009. – V. 6. – S. 28–32.
6. Comparison of different synthesis
routes for Mg–Al layered double hydroxides: Characterization of the structural
phases and anion exchange properties / H.W. Olfs [et
al.] // Appl. Clay Sci. ‒ 2009. ‒ Vol. 43, № 3–4. ‒ P. 459–464.
7. Intercalation of nucleotides into
layered double hydroxides by ion-exchange reaction /
S. Aisawa [et al.] // Appl. Clay Sci. ‒ 2005. ‒ Vol. 28, № 1-4. ‒
P. 137–145.