К.х.н. Каримова Л.М., д.т.н. Жумашев
К., Кайралапов Е.Т.
Химико-металлургический
институт им. Ж.Абишева, Казахстан
Исследование процесса выщелачивания обожженного чернового концентрата
руды Анненского месторождения
В последние годы в ряде стран возросло внимание к
гидрометаллургическим и комбинированным способам извлечения меди из
минерального сырья [1]. Особое место занимает сульфатизирующий обжиг [2] с
последующей гидрометаллургической переработкой продукта обжига. Ранее [3] была
установлена оптимальная температура обжига, обеспечивающая получение
преимущественно сульфатного огарка, пригодного для выщелачивания ценных
компонентов.
Существует много промышленных способов перевода меди в раствор. При определенных условиях выщелачивания можно
достигнуть практически полного перевода в
раствор меди, причем основными факторами, влияющими на
растворение, являются природа и концентрация растворителя и температура.
Исследование проводили с
серной кислотой как наиболее распространенным промышленным и легко транспортируемым
растворителем в гидрометаллургии, для которого характерна достаточная
растворяющая способность. Значительную часть ее рядом способов можно
регенерировать в процессе осаждения меди из растворов.
Для определения оптимальных условий извлечения меди в раствор (ценных
компонентов) были проведены опыты на основе математического обобщения
традиционного планирования эксперимента по методу Зейделя-Гаусса-Малышева [4].
Исследования проводили с перемешиванием на магнитной мешалке в
термостатированной ячейке. Изучали влияние температуры (t, 20–80 0С), концентрации
серной кислоты (![]() , 25-120 г/л) продолжительности опыта (τ, 20-120 мин.), отношения жидкого
к твердому (Ж:Т, 2:1 – 10:1). Графики частных зависимостей по извлечению меди в
раствор и приведены на рисунке 1. Химический состав обожженного флотационного
концентрата Анненского рудника представлен в таблице 1.
, 25-120 г/л) продолжительности опыта (τ, 20-120 мин.), отношения жидкого
к твердому (Ж:Т, 2:1 – 10:1). Графики частных зависимостей по извлечению меди в
раствор и приведены на рисунке 1. Химический состав обожженного флотационного
концентрата Анненского рудника представлен в таблице 1.
Таблица 1 – Результаты химического анализа обожженного флотационного
концентрата Анненского рудника
|
Компонент |
Cu |
Fe |
Al |
Zn |
Mg |
Mn |
Sобщ. |
Sсульфатн. |
Ag г/т |
Au г/т |
|
Содержание,
% |
6,35 |
4,26 |
3,86 |
1,10 |
0,57 |
0,09 |
3,47 |
3,40 |
156 |
0,3 |
εCu,% εCu,% б а t, 0C τ, мин
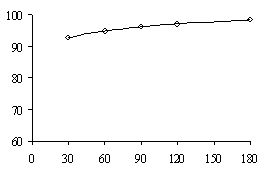
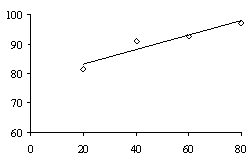
εCu,% εCu,% г в Ж:Т
![]()
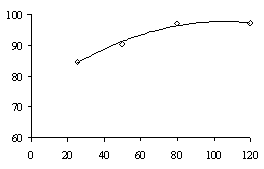
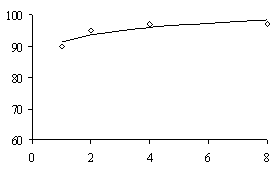
Точки – экспериментальные данные; линии – аппроксимирующая
функция
εCu,%– извлечение меди в раствор, а – влияние
температуры;
б – продолжительности выщелачивания; в – концентрации серной
кислоты;
г – отношение Ж:Т
Рисунок
1 – Зависимости извлечения меди в раствор
после
выщелачивания от заданных факторов
Из данных опытов
рисунка 1 следует, что с ростом температуры от 20 до 80 0С извлечение меди в раствор увеличивается, что
обусловлено повышением растворимости компонентов и как следствие - ослабления
фактора «высаливания». При этом извлечение меди в раствор в исследуемом
интервале повышается с 81,2 до 97,08 соответственно.
Зависимость извлечения меди в раствор от продолжительности выщелачивания
возрастает в интервале 30-120 мин с 92,78 до 97,08%.
Неполное растворение
меди (т.е. извлечение его в раствор не превышает 98%) и необходимость
выщелачивания в течение 3 часов связано с наличием в огарке спекшихся комочков,
на распад которых требуется определенное время, а также присутствие в огарке
почти нерастворимой формы меди, заключенных в пустую пароду.
Извлечение меди увеличивается с повышением концентрации
серной кислоты в растворе. Лучшие показатели по извлечению меди получены при
концентрации серной кислоты 120 г/л.
Соотношение Ж:Т в наибольшей
степени влияет на результаты выщелачивания меди. При изменении Ж:Т от 1 до 8
извлечение меди в раствор возрастает от 89,94 до 97,15, при снижении Ж:Т
извлечение уменьшается, так как при этом пульпа становится плотной и возникают
диффузионные затруднения.
Полученные уравнения для извлечения меди в раствор с учетом
значимых функций для описания совокупности действующих факторов обобщаются согласно
[4] в виде их произведения с нормировкой по центральному экспериментальному
значению в степени (n-1),
где n – число частных функций. По
центральному (ц) для всех функций условию: t = 80 0С, ![]() = 120 г/л, τ
= 120 мин, Ж:Т=4:1, значение εCu, ц =96,92%.
Обобщенное уравнение выразится как
= 120 г/л, τ
= 120 мин, Ж:Т=4:1, значение εCu, ц =96,92%.
Обобщенное уравнение выразится как
![]() . (1)
. (1)
При
сопоставлении результатов эксперимента и расчета нашли значения коэффициента
корреляции для извлечения меди в раствор R=0,9883, tR =158,70>2, что
подтверждает адекватность описания данных эксперимента настоящим уравнением.
Таким образом, исследовано влияние различных факторов на процесс
выщелачивания. Повышению извлечения меди
в раствор способствует продолжительность растворения огарка и увеличение
температуры. Установлено, что достаточно высокую степень извлечения меди в
раствор можно достичь при условиях: t –80 0С, τ – 120 мин., ![]() – 100 г/л, Ж:Т
4:1. Выход кека при этих условиях составляет 74,6%.
– 100 г/л, Ж:Т
4:1. Выход кека при этих условиях составляет 74,6%.
При полученных оптимальных условиях выщелачивания проверена возможность
повторного использования сернокислого раствора после первого выщелачивания с
целью увеличения концентрации меди в растворе, что позволило получить вторичный
раствор с содержанием меди 29,025 г/л, что вполне достаточно для ведения процесса
электролиза меди.
Литература:
1.
Худяков И.Ф., Тихонов А.И., Деев В.И., Набойченко С.С.
Металлургия меди, никеля и кобальта. – М.:Металлургия, 1977. –Т.1.
2.
Саргсян Л.Е., Оганесян А.М. Обжиг сульфидно-цинкового
концентрата с получением преимущественно сульфатного огарка для эффективного
выщелачивания//Цветные металлы, 2006. -№7. –С.16.
3.
Саргсян Л.Е., Оганесян А.М. Активированный сульфатизирующий
обжиг халькопиритового концентрата для серно-кислотного выщелачивания//Известия
вузов. Цветная металлургия, 2010. -№5. –С.11-13.
4. Малышев В.П. Математическое описание результатов многофакторного эксперимента, проведенного по методу Зейделя-Гаусса// Вестник АН Каз ССР.-1978.-№4.-С.31-38.