Кириллов И.М.
Тульский Тульский
Государственный университет, Россия
Биотопливный элемент на основе
мембранной
фракции бактерий Gluconobacter oxydans
В связи с
грядущим глобальным истощением источников полезных ископаемых, используемых для
нужд энергетики, одним из перспективных направлений является разработка
альтернативных источников электроэнергии, в том числе биотопливных элементов
(БТЭ), представляющих собой устройства, которые используют биологические
компоненты как катализаторы для генерации электричества. Одними из
перспективных микроорганизмов, на основе которых возможно создание БТЭ,
являются бактерии Gluconobacteroxydanssubsp. industrius. Данные микроорганизмы характеризуются мембранной
локализацией основных ферментов клеточного метаболизма – дегидрогеназ,
осуществляющих неполное окисление углеродных субстратов, что обеспечивает
легкий доступ медиатора к активным центрам фермента. Ферменты обладают более
высокой каталитической активностью по сравнению клетками, но процесс их выделения
увеличивает стоимость биокатализатора, поэтому перспективным является
применение в качестве биокатализатора мембранной фракции бактерий.
Целью
данной работы являлось определение параметров работы модели
медиаторногобиотопливного элемента на основе мембранной фракции бактерий Gluconobacteroxydanssubsp.
industrius(BKMB-1280).
Ферментные препараты, содержащие
мембранлокализованные и цитоплазматические дегидрогеназы бактерий G. oxydans, получали из разрушенной
ультразвуком биомассы бактерий путем последовательного центрифугирования. На
начальном этапе работы необходимо выбрать оптимальное содержание мембранной
фракцииG. oxydans в
кювете, при котором достигается максимальное значение генерируемого потенциала.Зависимость генерируемого
потенциала в зависимости от содержания мембраннойфракцииG. oxydans в ячейке БТЭ представлены
на рисунке 1.
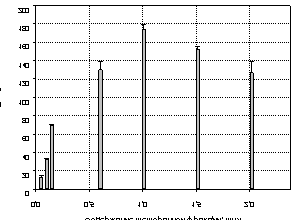
Рис. 1. Зависимость генерируемого
потенциала в зависимости от содержания мембранной фракции (мг/л) G. oxydans.
Максимальное
значение генерируемого потенциала наблюдается при содержаниимембранной фракции
ванолите1 мг/л.
Далее при
содержании биокатализатора1мг/л была исследована зависимость генерируемого
потенциала от концентрации медиатора 2,6-дихлорфенолиндофенола(рис. 2).
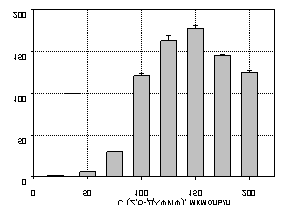
Рис. 2. Зависимость генерируемого
потенциала от концентрации медиатора 2,6-ДХФИФ в анолите.
Как можно видеть
максимальное значение генерируемого потенциала наблюдается при использовании 150мкмоль/л
2,6-ДХФИФ в анодной ячейке.
Для ускорения
передачи электронов с поверхности мембранной фракции 2,6-ДХФИФ использовался
совместно с ФМС.На рисунке 3приведены значения генерируемых потенциалов при
совместном использовании 150мкмоль/л2,6-ДХФИФ и феназинметасульфата (ФМС)сразличной
концентрацией в анодном отделении.
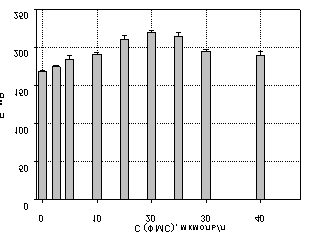
Рис. 3. Значения генерируемых
потенциалов при использовании 150 мкмоль/л 2,6-ДХФИФ и ФМС различнойконцентрации.
Максимальное
значение генерируемого потенциала наблюдается при использовании смеси 150 мколь/л
2,6-ДХФИФ и 20 мкмоль/л ФМС.
Важно отметить,
что время генерации потенциала в макете БТЭ, на основе мембранной фракции, без
дополнительного «помощника» медиатора 2,6-ДХФИФ составляет 30-35 минут, а при совместном
использовании 2,6-ДХФИФиФМС в анолите, время генерации потенциала составляла
3-5 минут, т.е. снижается в 10 раз.
Важной задачей является определение мощностных характеристик макета БТЭ
на основе мембранной фракции бактерий G.oxydans при использовании
медиаторов как в анодном, так и катодном пространстве (3мМ/л K3[Fe(CN)6] в католите).Применение биокатализатора на основе мембранной
фракции при использовании ГЦФ в католите позволяет увеличить генерируемый
потенциал на 20 мВ по сравнению с отсутствием ГЦФ, генерируемый потенциал
составляет 240 мВ, при этом снизить значение внутреннего сопротивления элемента
со 120 до5 кОм, а удельную мощность увеличить с 0,5 до 6 мВт/м2.
Таким образом, максимальное значение
генерируемого потенциала, при использовании 1 мг/л мембранной фракции бактерий G. oxydans,
при комбинировании 150 мколь/л 2,6-ДХФИФ и 20 мкмоль/л ФМС в анолите и 3мМ/л K3[Fe(CN)6] в католите.