Ганикель Д.А.
Инновационный Евразийский университет, Республика Казахстан
Влияние температуры на
каталитические свойства Pd-ПЭГ/ZnO катализатора
Введение
Нанесенные
на неорганический оксид, стабилизированные полимером палладиевые катализаторы,
как правило, работают при температуре 40 ОС и при нормальном
атмосферном давлении. Реакции могут протекать и при меньших и при больших
температурах.
Теоретическая часть
Pd-ПЭГ/ZnO
(палладий-полиэтиленгликоль/оксид цинка),КР (крахмал).
Традиционные пропиточный
и адсорбционный способы получения нанесенных катализаторов включают стадии высокотемпературных прокаливания и
восстановления для прочного закрепления металлов на поверхности носителей и их
активации. Gabor A. Somorjai с сотрудниками в качестве стабилизаторов
наночастиц, а также при нанесении их на оксиды для получения катализаторов
активно использовали поливнилпирролидон [1].Предлагаемые авторами катализаторы готовятся закреплением
полимер-протектированных наночастиц на носитель с
последующими обычными
стадиями
высокотемпературного прокаливания и восстановления, что приводит к разрушению
полимерной оболочки и сохранению наночастиц металла на носителях. Были получены полимер-протектированные платиновые и родиевые наночастицы в
мезопористом силикагеле марки SBA-15, причем SiO2 синтезировался вокруг наночастиц. В таких
условиях в одном мезопористом канале располагается одна наночастица (рисунок
1).

Рисунок 1 – Монодисперсные платиновые наночастицы, инкапсулированные
в каналы мезопористого силикагеля марки
SBA-15. Размеры частиц изменяются при сохранении общего содержания металла в
катализаторе – 1%Pt.
Аналогичный
подход был использован в работе [2] при приготовлении нанесенных катализаторов
на основе дендримерных комплексов металлов, которые наносились на оксид
кремния, а затем прокаливались и
восстанавливались водородом при высоких
температурах, при этом дендримерная оболочка выжигалась, а на поверхности
носителя формировался равномерный слой наночастиц платины:
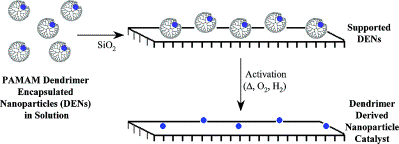
Рисунок 2 – Схема получения наночастиц платины
Приготовленные
таким образом каталитические системы показали высокую активность в процессе
гидрогенизации толуола и окисления СО.
Основным остается метод, при котором наночастицы,
стабилизированные полимерами (в основном,
поливинил-пирролидоном) формируются в растворе, а затем осаждаются на
поверхность носителей с последующими стадиями прокаливания и восстановления,
присущими обычным нанесенным системам.
Был
предложен простой способ закрепления тонкого слоя ПМК (пористых мембранных
катализаторов) на поверхности
неорганических оксидов [3], исключающий высокотемпературные
стадии прокаливания и восстановления.
Вводимые в систему полимеры привносят собственные уникальные свойства (гибкость и подвижность сегментов полимерных цепей, набухаемость,
подвижность и, в связи с этим легкость настройки на объемные молекулы, как в
случае белковой части ферментов) в поведение каталитических систем.
Тем не менее, вызывает
интерес температурный режим приготовления катализаторов и проведения реакции
гидрирования в зависимости от температуры.
С этой целью была
приготовлена серия катализаторов в разном температурном диапазоне и лучший из
них также протестирован в разном температурном диапазоне.
Экспериментальная часть
Катализаторы были приготовлены выше указанным способом,
стакане с рубашкой, температура приготовления поддерживалось для 10 ОС прохладной водой из под
крана, для 25 ОС при комнатной температуре, в остальных случаях через
термостат. Таким образом, в этой серии опытов катализаторы готовились из водных
растворов, нагретых до 10, 25, 40, 60 и 80 ОС
при времени адсорбции метала на полимер 2 часа.
Далее приготовленные катализаторы были протестированы в
модельной реакции гидрирования аллилового спирта. Низкая активность наблюдалась на катализаторах, приготовленных
при 10 и 25 ОС, возможно
из-за недостаточного содержания палладия, поскольку катализатор выдерживался в
маточном растворе только два часа, что при данных температурах недостаточно для
достижения равновесного содержания палладия в полимере. Также эти катализаторы
по цвету были светло коричневые, ближе к бежевому цвету и в маточном растворе
визуально было видно наличие не адсорбированных ионов палладия. Максимальная скорость гидрирования достигалась на образце,
приготовленном при 40 и 60 ОС.
Эти катализаторы имели, обычный для палладиевых катализаторов приготовленных
данным методом, коричневый цвет и маточный раствор был бесцветен. Возможно, это
связано с тем, что палладий полностью адсорбировался на полимере.
Невысокая скорость реакции на катализаторе, полученном
при 80ОС, связана, по-видимому, с частичным разрушением полимера при
котором мог выделиться водород и восстановлением Pd(II) выделенным водородом в
Pd(0) в процессе приготовления
катализатора. Темно-серый цвет осадка, в отличие от всех других светло-желтых и
коричневых, подтверждает наличие восстановленного палладия.
На рисунке 3 показано влияние температуры приготовления Pd-ПЭГ/ZnO
(полиэтиленгликоль/оксид цинка) катализаторов
на их активность в гидрировании аллилового спирта (0,18 моль/л) в этаноле (25
мл).
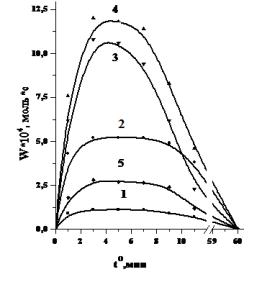
Рисунок 3 – Влияние температуры
приготовления Pd-ПЭГ/ZnO катализаторов
на их активность в гидрировании аллилового спирта
Таким образом, наиболее активными оказались катализаторы
приготовленные при температуре 40 и 60ОС. Однако готовит
катализаторы при 40 и 60ОС энергетически невыгодно, тем более время
адсорбции металла на полимер 2 часа, можно увеличить даже до 5 часов.
Катализатор приготовленный при комнатной температуре слегка уступал по
активности и в следующей серии опытов было решено исследовать время адсорбции
метала на полимер в диапазоне с 1 часа до 5 часов. Зависимость скорости
гидрирования от времени адсорбции металла на полимер Pd-ПЭГ/ZnO катализаторов даны на рисунке 4

Рисунок 4 - Зависимость скорости
гидрирования от времени адсорбции металла на полимер Pd-ПЭГ/ZnO катализаторов
Как видно из рисунка 4 зависимость не противоречить
общепринятой изотерме адсорбции Ленгмюра и для приготовления катализатора
достаточно трех часов адсорбции активной фазы на полимер после двухчасовой
адсорбции полимера на носитель.
Таким образом, решено
готовить катализаторы при комнатной температуре и временем адсорбции полимера
на носитель 2 часа и временем адсорбции активной фазы на полимер 3 часа.
Выбор температуры
проведения реакции гидрирования.
Многие химические реакции протекают в определенных
условиях, таких как температура, давление, объем, наличие или отсутствие катализатора. На современном этапе, в силу
множества факторов, главным из которых является, так называемая "зеленая
химия", многие реакции предпочтительны в мягких условиях. Эти условия
атмосферное давление, комнатная или не большая температура, наличие
гетерогенного катализатора (гетерогенные катализаторы легко выводятся из
реакционной среды, не перемешиваются ни с субстратом, ни продуктом реакции) и
выбор растворителей.
Объемом для реакции является объем реактора, где мало
что можно изменить. Наиболее безопасным является нормальное атмосферное
давление, кроме того проведение реакции при атмосферном давлении легче
локализовать последствия в случае непредвиденных ситуации. Относительно
катализатора все более или менее ясно, это как уже было отмечено Pd-КР/ZnO.
Растворителем будет вода, так как она, во первых, хорошо связанна с принципами
зеленой химии и во вторых в воде полимерная часть катализатора легче набухает и
вследствие этого на поверхность набухшего полимера "выворачиваются"
нижние слои полимер - металлического комплекса
и соответственно увеличивается удельная площадь катализатора. А, как
известно активность гетерогенного катализатора не в последнюю очередь зависит
от реакционной поверхности. Остается только температурный режим проведения
реакции гидрирования.
В
следующей серии опытов на готовом Pd-ПЭГ/ZnO катализаторе определялась наиболее оптимальная
температура проведения реакции. Реакции проводились в диапазоне 10, 25, 40, 60
и 80 ОС. Оказалось, что
наиболее активно катализатор реагирует при 40 ОС. По всей видимости, при температурах 10 и 25 ОС полимерная часть
катализатора набухает плохо и находится в коллапсном состоянии. Известно, что
тем больше температура, тем больше в ней происходит внутримолекулярное движение
и тем больше набухает полимер. Казалось бы,
дальнейшее повышение температуры должна привести к росту скорости
гидрирования, однако при 40 ОС
активность катализатора наибольшая. По-видимому, дальнейшее повышение
температуры приводит к деструкции
полимера. Так при 60 ОС
активность катализатора снижается в силу того что полимер-стабилизатор только
начинает нарушаться а к 80 ОС
в полимере происходит глубокие, не восстанавливаемые нарушения. Это также
сочетается с правилом Вант-Гоффа, что на каждые 10 ОС повышения температуры скорость реакции увеличивается
2-4 раза. Данные зависимости активности Pd-ПЭГ/ZnO катализатора от температуры проведения реакции
даны на рисунке 5.
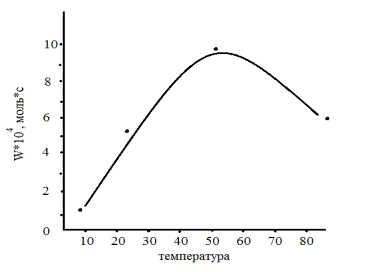
Рисунок 5 - Зависимость активности Pd-ПЭГ/ZnO
катализатора от температуры
Вывод
Таким образом, наиболее оптимальным температурным
режимом проведения реакции гидрирования на Pd-ПЭГ/ZnO катализаторе является 40ОС. Дальнейшее
повышение температуры приводит к деструкции катализатора, и он теряет свою
активность.
СПИСОК
ЛИТЕРАТУРЫ
1)
Помогайло
А.Д., Розенберг А.С., Уфлянд И.Е. Наночастицы
металлов в полимерах.
Москва: Химия, 2000.
2)
Гусев
А.И. Наноматериалы, наноконструкции, нанотехнологии. М.:Физматлит, 2007.
3)
Стайлз
Э.Б - Пер. с англ. /Под ред. А. А. Слинкина. — М.: Химия, 1991.