Минасян С. М., Галагудза М.
М., Дмитриев Ю. В., Васильева М. С., Боброва Е. А., Бадриханова Л. Р., Курапеев
Д. И., Снегирёв М. А., Павлов А. Г., Карпов А. А., Сонин Д. Л., Сафрошина Е.
В., Усков И. С., Нифонтов Е. М., Королёв Д. В., Губадова Л. В., Власов Т. Д.,
Викторова Ю. П.
Федеральный Центр Сердца, Крови и Эндокринологии им.
В. А. Алмазова, Санкт-Петербург, Россия.
Санкт-Петербургский Государственный Медицинский
Университет им. акад. И. П. Павлова, Санкт-Петербург, Россия.
Санкт-Петербургский Государственный Университет,
медицинский факультет, Санкт-Петербург, Россия.
Оптимизация
методов защиты миокарда от тотальной ишемии-реперфузии (экспериментальное
исследование).
Актуальность
проблемы. К настоящему времени комплекс
мероприятий для интраоперационной защиты сердца от ишемического/реперфузионного
повреждения достаточно хорошо разработан. Центральное место среди методов
защиты миокарда занимает кардиоплегия (КП) (Жидков
И. Л. и соавт., 2006). До сих пор в
клинике нередко встречаются осложнения, связанные с ишемическим повреждением
сердца во время операции, а именно, синдром малого выброса и интраоперационый
инфаркт миокарда (Masse
L., Antonacci M., 2005). Это связано как с неадекватной защитой миокарда, так и с исходным
его повреждением вследствие основного заболевания (Susumu I. et al., 2006).
Причинами, способствующими развитию ишемических повреждений во время операции,
являются гипертрофия миокарда, атеросклеротический и постинфарктный кардиосклероз,
низкая исходная фракция выброса, суммарное время наложения зажима на аорту и
др. (Гордеев М. Л., 2001; Локшин Л. С. и
соавт., 1998, Tan T. E. et al., 2003). В связи с этим
проблема интраоперационной защиты миокарда остается актуальной и требует проведения
комплексных экспериментально-клинических исследований. При этом системные
целенаправленные экспериментальные исследования, посвященные данной проблеме,
практически отсутствуют. Несмотря на активное успешное использование в клинике
кровяной КП, интерес к кристаллоидной КП не уменьшается, что связано, прежде
всего, с невозможностью использовать прогрессивную методику кровяной КП в детской,
и, особенно, в неонатальной кардиохирургии. Между тем, именно эта группа
больных зачастую требует для проведения коррекции сложных врожденных пороков
сердца длительной аноксии и, как следствие, тщательной интраоперационной защиты
миокарда (Бураковский В. И. и соавт., 1996). Таким образом, дальнейшее совершенствование методик кристаллоидной
КП представляет большой практический интерес, а исследование механизмов защиты
миокарда с помощью различных вариантов КП представляет собой актуальную научную
проблему.
Цель работы: исследовать
эффективность различных методик кардиоплегии и различных вариантов
кардиоплегических растворов для защиты миокарда от тотальной ишемии в
эксперименте на модели перфузии изолированного сердца крысы по Лангендорфу.
1.
Сравнить
эффективность различных способов защиты сердца от тотальной ишемии с
использованием известных кардиоплегических растворов.
2.
Разработать
ряд кардиоплегических растворов на основе буферного раствора Кребса-Хенселейта
и испытать их в эксперименте.
3.
Изучить
особенности защиты миокарда кардиоплегическими растворами с различным ионным
составом, с различным содержанием глюкозы, маннитола, компонентов буферных
систем, а также провести сравнение эффективности внеклеточных и внутриклеточных
кардиоплегических растворов.
4.
Исследовать
изолированное влияние температурного фактора как способа защиты миокарда от
тотальной ишемии, а также его влияние в сочетании с кардиоплегическими
растворами.
5.
Исследовать
гиперполяризационные кардиоплегические растворы, содержащие эсмолол,
ацетилхолин и аденозин в сочетании с нормальным уровнем калия.
Материалы и методы
исследования
Эксперименты были проведены на 250 крысах-самцах массой
200-300 г линии Wistar с использованием методики перфузии изолированного
сердца по Лангендорфу. После извлечения сердца его подключали к модифицированному
аппарату Лангендорфа и начинали ретроградную (через аорту) перфузию модифицированным
буферным раствором Кребса-Хенселейта под постоянным давлением 80 мм рт. ст.
Состав буферного раствора Кребса-Хенселейта: Na+ 143 ммоль/л, K+
5,9 ммоль/л, Ca2+ 1,5 ммоль/л, Mg2+ 1,2 ммоль/л, Cl-
125,1 ммоль/л, НСО3 -25 ммоль/л, SО42-
1,2 ммоль/л, Н2РО4- 1,2 ммоль/л, глюкоза
11 ммоль/л. Насыщение буферного раствора карбогеном (5% СО2 и 95% О2)
производилось с целью его оксигенации и доведения рН до уровня рН 7,4. Напряжение
кислорода при этом составляло 100-120 мм рт. ст. Температура перфузата и сердца
составляла 37,0±0,1°С. Во время функционирования препарата изолированного
сердца регистрировали следующие параметры: систолическое, диастолическое
(ДВЛЖД) и пульсовое давление (ПВЛЖД) в левом желудочке, частоту сердечных
сокращений (определялась по кривой внутрилевожелудочкового давления), объёмную
скорость коронарной перфузии. В ходе глобальной ишемии регистрировали среднее
давление в левом желудочке (ВЛЖД). После завершения периода реперфузии
производилось гистохимическое исследование размеров необратимо поврежденной
зоны миокарда с помощью окрашивания срезов сердца трифенилтетразолия хлоридом
(ТТХ). Базальные и апикальные
поверхности всех срезов фотографировали цифровой камерой Olympus
С-4000, сопряженной с помощью микрофотографического устройства с микроскопом
МБС-10 (ЛОМО, Санкт-Петербург). Изображения срезов обрабатывали компьютерным методом, который позволяет рассчитать
площадь этих двух зон. Затем, суммируя результат по всем срезам, вычисляли
объём зоны необратимого повреждения по отношению к общему объёму ткани. Статистическая
достоверность различий функциональных данных в каждой временной точке, а также
размеры зоны инфаркта оценивалась с помощью непараметрического критерия
Манна-Уитни. Все функциональные данные, а также размер инфаркта выражались в
виде «среднее ± стандартное отклонение».
Значения р менее чем 0,05 рассматривались
как достоверные.
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ
Перфузия
изолированного сердца теплокровных животных и антеградная КП имеют одинаковую методику
исполнения, т. е. КП – это перфузия изолированного сердца человека. Для
перфузии изолированного сердца теплокровных животных наиболее удачен буферный
раствор Кребса-Хенселейта (БРКХ), который был предложен в 1932 году и с тех пор
не имеет себе альтернативы. Поэтому в настоящей работе производилась разработка
КПР на его основе с добавлением различных компонентов, вызывающих мгновенную асистолию.
В работе
была исследована эффективность целого ряда КПР оригинального состава на основе
БРКХ (табл. 1, 2), имевших следующие важнейшие отличительные особенности:
1). КПР№1:
для достижения асистолии в растворе была повышена концентрация ионов калия и
магния (до 25 и 16 ммоль/л, соответственно) с одновременным снижением
концентрации кальция до 0,3 ммоль/л.
2). КПР№1П.
Данный раствор отличался от КПР№1 концентрацией ионов калия (10 ммоль/л),
магния (10 ммоль/л), кальция (1 ммоль/л). Эти изменения были сделаны по следующим
причинам: 1) после наступлении асистолии для её поддержания требуются меньшие
концентрации калия и магния; 2) в результате снижения осмолярности этого КПР появляется
возможность добавить в него дополнительные кардиопротективные субстанции без
превышения допустимой осмолярности; 3) в случае использования КПР для высокообъёмной
КП или для постоянной коронарной перфузии концентрация ионов кальция должна
быть нормальной или немного сниженной.
3). КПР№1реф:
представляет собой модификацию КПР№1, отличающуюся наличием коллоидного
компонента – гидроксиэтилкрахмала (ГЭК) с молекулярной массой около 130 кДа и
концентрацией 5%. В остальном состав КПР№1реф аналогичен КПР№1.
4). КПР№1М-Гл
и КПР№1-Гл: внеклеточные КПР, являющиеся модификацией КПР№1 с увеличенным
содержанием глюкозы (до 100 и 240 ммоль/л, соответственно) и повышенной
осмолярностью.
5). КПР№3:
внутриклеточный КПР с содержанием ионов натрия 25 ммоль/л. При его создании
преследовали цель выявить кардиопротективные свойства КПР с высоким содержанием
глюкозы (247 ммоль/л). Для сохранения осмолярности на уровне 380 мосмоль/л
концентрацию натрия снизили до 25 ммоль/л.
6). КПР№4,
КПР№7, КПР№9 представляют собой семейство КПР для гиперполяризационной КП,
созданных на основе БРКХ. Для индукции асистолии в БРКХ с нормальным уровнем
калия и магния включили ацетилхолин-хлорид (КПР№4), эсмолол (КПР№7), аденозин
(КПР№9).
7). КПР№5:
модификация КПР№1 с увеличенной концентрацией бикарбонат-аниона до 75 ммоль/л для
усиления буферной ёмкости.
8). КПР№6:
гипермагниевый КПР, в котором концентрация ионов калия составляла 5,9 ммоль/л
(как в БРКХ), а концентрация ионов магния - 16 ммоль/л.
9). КПР№8:
разновидность КПР№1П с добавлением 106 ммоль/л маннита для уменьшения
внутриклеточного и интерстициального отёка миокарда.
Таблица 1.
Состав разработанных на основе буферного раствора
Кребса-Хенселейта
кардиоплегических растворов (КПР) (в ммоль/л) (часть
1).
|
|
КПР№1 |
КПР№1П |
КПР№1реф |
КПР№3 |
КПР№1Гл |
КПР№1Гл-М |
|
Na+ |
143 |
110 |
143 |
25 |
143 |
143 |
|
К+ |
25 |
10 |
25 |
25 |
25 |
25 |
|
Са2+ |
0,3 |
1 |
0,3 |
0,3 |
0,3 |
0,3 |
|
Mg2+ |
16 |
10 |
16 |
16 |
16 |
16 |
|
Сl- |
141,8 |
95,8 |
141,8 |
26,6 |
141,8 |
141,8 |
|
Н2РО4- |
1,2 |
1,2 |
1,2 |
1,2 |
1,2 |
1,2 |
|
НСО3- |
25 |
25 |
25 |
25 |
25 |
25 |
|
SO42- |
16 |
16 |
16 |
16 |
16 |
16 |
|
Глюкоза |
11 |
11 |
11 |
247 |
240 |
100 |
|
ГЭК |
- |
- |
5% |
- |
- |
- |
Таблица 2.
Состав разработанных на основе буферного раствора
Кребса-Хенселейта
кардиоплегических растворов (КПР) (в ммоль/л) (часть
2).
|
|
КПР№5 |
КПР№6 |
КПР№8 |
КПР№4 |
КПР№7 |
КПР№9 |
|
Na+ |
143 |
143 |
110 |
143 |
143 |
143 |
|
К+ |
25 |
5,9 |
10 |
5,9 |
5,9 |
5,9 |
|
Са2+ |
0,3 |
0,3 |
1 |
1,5 |
1,5 |
1,5 |
|
Mg2+ |
16 |
16 |
10 |
1,2 |
1,2 |
1,2 |
|
Сl- |
93 |
123,3 |
95,8 |
125,7 |
125,7 |
125,7 |
|
Н2РО4- |
1,2 |
1,2 |
1,2 |
1,2 |
1,2 |
1,2 |
|
НСО3- |
75 |
25 |
25 |
25 |
25 |
25 |
|
SO42- |
16 |
16 |
10 |
1,2 |
1,2 |
1,2 |
|
Глюкоза |
11 |
11 |
11 |
11 |
11 |
11 |
|
Ацетилхолин |
- |
- |
- |
500 мг/л |
- |
- |
|
Эсмолол |
- |
- |
- |
- |
1 |
- |
|
Аденозин |
- |
- |
- |
- |
- |
200 мкг/л |
|
Маннит |
- |
- |
106 |
- |
- |
- |
Разработанные
на основе БРКХ КПР сравнивали с официнальными КПР Кустодиол и КПР госп. Св.
Томаса №2. Также исследовалась эффективность указанных официнальных КПР в различных
температурных режимах.
Протокол экспериментов:
1.
Контроль. После периода стабилизации осуществляли 60-минутную нормотермическую
(+37ºС) тотальную ишемию путём выключения перфузии. Затем осуществляли
120-минутную реперфузию и оценку размера некроза.
2.
Опытные группы с КП. Протокол эксперимента аналогичен контролю, но на 1-й, 21-й
и 41-й минутах 60-минутной ишемии в аорту вводили КПР под давлением 80 мм рт.
ст. в течение 4-х, 2-х и 2-х минут, соответственно.
Эксперименты
с КПР выполняли в тепловом режиме (температура КПР и сердца в период ишемии +37ºС),
в холодовом режиме (+5ºС), а также в тепловатом режиме (+22ºС) для
КПР госп. Св. Томаса №2, так как именно эта температурная точка представляет наибольший
интерес в плане совершенствования тепловатой КП.
Согласно
имеющимся стандартам, кристаллоидные КПР используются только в холодовом режиме
в сочетании с наружным охлаждением сердца, причем целевая температура сердца не
должна превышать +11ºС. В данном исследовании во многих экспериментах
температура сердца и КПР составляла 37ºС, что противоречит вышеописанному
правилу. Такой температурный режим был выбран для оценки влияния именно
химического состава КПР на его эффективность и исключения возможного
кардиопротективного действия низкотемпературного фактора.
Во время
экспериментов параметры гемодинамики изолированного сердца регистрировали в
следующих временных точках: после окончания стабилизационного периода (ДВЛЖД,
ПВЛЖД, ЧСС, КП), ВЛЖД на 5, 15, 25, 35, 45, 55 минутах ишемии в контроле и в
группах с гипотермией без КП (в группах с КП - на 5 и 15 минутах 20-минутных
периодов ишемии), ПВЛЖД и ДВЛЖД на 5 и 30 минутах реперфузии. Исходно функциональные
параметры сердец во всех экспериментальных группах были одинаковыми и
статистически не различались между собой.
Исследование внеклеточных кардиоплегических растворов
на основе
буферного раствора Кребса-Хенселейта в различных
температурных
режимах в сравнении с официнальными кардиоплегическими
растворами.
Исследование
КПР№1 в тепловом (+37ºС) режиме продемонстрировало значительный
кардиопротективный потенциал этого КПР. Размер некроза при этом был достоверно
выше, чем в холодовом режиме, но значительно ниже, чем при использовании КПР
госп. Св. Томаса №2 и КПР Кустодиол в тепловом режиме (табл. 3). Положительные
результаты от применения КПР№1 были ожидаемы, так как его основа, а именно
БРКХ, как отмечалось выше, хорошо себя зарекомендовал для перфузии изолированного
сердца теплокровных животных и близок по своему химическому составу к плазме
крови.
Таблица 3.
Размер некроза сердца в экспериментальных группах
|
Группа |
Температурный
режим |
Размер
некроза, % |
|
Контроль |
+37°С |
77,9±7,0 |
|
КПР№1 |
+37°С |
14±5* |
|
КПР№1
|
+5°С |
7,6±3,1* |
|
КПР№1П |
+37°С |
19,2±8,2* |
|
КПР№1реф |
+37°С |
8,8±3,8* |
|
КПР
госп. св. Томаса №2 |
+37°С |
49±9,8# |
|
КПР
госп. св. Томаса №2 |
+5°С |
6,7±4,7* |
|
КПР
госп. св. Томаса №2 |
+22°С |
6,4±3,1* |
|
КПР
Кустодиол |
+37°С |
83,9±8,6 |
|
КПР
Кустодиол |
+5°С |
7,9±2,1* |
Примечание: *р<0,01 в сравнении с контролем и с КПР госп. св.
Томаса №2 в тепловом режиме (+37°С), #р<0,05 в сравнении с
контролем.
Испытание КПР№1 в холодовом режиме при температуре
+5ºС не выявило никаких преимуществ и недостатков перед КПР госп. Св.
Томаса №2 и КПР Кустодиол при их использовании также в холодовом режиме –
разница по размеру некроза между указанными группами отсутствовала (табл. 3), а
динамика восстановления сократимости в период реперфузии была одинаковой в
группах КПР№1 и КПР госп. Св. Томаса №2, значительно превосходя таковую для КПР
Кустодиол (табл. 4). Этот факт является доказательством преимущества внеклеточных
КПР над внутриклеточными в плане восстановления насосной функции сердца.
При
исследовании КПР№1П в тепловом режиме результаты оказались почти такими же, как
и в случае КПР№1. Однако асистолия при введении первой дозы КПР№1П наступала
медленнее - в конце 2-й или на 3-ей минуте инфузии, в то время как при инфузии
КПР№1 - мгновенно (через 5-10 секунд). Этот факт позволяет рекомендовать КПР№1П
только для повторных эпизодов КП, либо в конце 1-го эпизода, когда асистолия
уже наступила под действием другого КПР. КПР№1реф показал несколько лучшие, чем
КПР№1П, результаты по размеру некроза, но не отличался от КПР№1П в плане сократимости
в период реперфузии.
Таблица 4.
Пульсовое (ПВЛЖД) и диастолическое (ДВЛЖД) давление в
левом желудочке в период реперфузии
|
|
Т,°С |
ПВЛЖД, мм рт. ст. |
ДВЛЖД, мм рт. ст. |
||
|
5 мин. |
30 мин |
5 мин |
30 мин |
||
|
Контроль |
+37°С |
Асистолия |
17,5±6,5 |
99,2±5,3 |
91,4±7,6 |
|
КПР
№1 |
+37°С |
97,2±10,2* |
104,1±13,9* |
24,1±7,7* |
11,0±6,0* |
|
КПР
№1 |
+5°С |
114,8±12,0** |
85,8±5,1** |
3,0±1,8** |
5,4±3,4** |
|
КПР
№1П |
+37°С |
83,2±3,2* |
91,2±19,3* |
29,8±6,2* |
9,4±3,2* |
|
КПР
№1реф |
+37°С |
96,5±11,1* |
83,8±6,5* |
32,3±8,4* |
17,5±3,7* |
|
КПР
госп. Св. Том. №2 |
+37°С |
6,4±2,5 |
24,1±8,8 |
82,8±7,9 |
53,8±17,2 |
|
КПР
госп. Св. Том. №2 |
+5°С |
114,7±11,5** |
94,1±24,6** |
3,6±1,7** |
3,9±3,2** |
|
КПР
госп. Св. Том. №2 |
+22°С |
113,8±9,5** |
78,9±9,0** |
8,2±3,9** |
9,9±4,0** |
|
КПР
Кустодиол |
+37°С |
Асистолия |
Асистолия |
52,0±8,1 |
44,0±7,0 |
|
КПР
Кустодиол |
+5°С |
87,6±38,0* |
55,4±8,5* |
14,3±8,3* |
9,2±4,0* |
Примечание: *р<0,05 в сравнении с контролем, **р<0,01 в
сравнении с контролем.
Исследование
КПР госп. Св. Томаса №2 в различных температурных режимах показало его высокую
эффективность в холодовом режиме и крайне низкий кардиопротективный эффект в
тепловом режиме (табл. 3, 4). Как указывалось ранее, тепловой режим в данных
экспериментах использовался специально для того, чтобы исключить протективное
действие гипотермии и оценить эффективность самого КПР. Результат по КПР госп.
Св. Томаса №2 в тепловом режиме убедительно показал, что сам по себе этот КПР
обеспечивает явно недостаточную кардиопротекцию. Интересные результаты были
получены при исследовании КПР госп. Св. Томаса №2 при температуре +22ºС: размер
некроза и восстановление сократимости достоверно не отличались от значений, полученных
при +5ºС. Таким образом, фармакохолодовая КП с использованием этого КПР
одинаково эффективна при уровнях гипотермии +5ºС и +22ºС и, вероятно,
при любой другой температуре в интервале от +5ºС до +22ºС.
При
анализе результатов эффективности КПР Кустодиол обращает на себя внимание тот
факт, что при его использовании в холодовом режиме величина некроза достоверно
не отличалась от таковой для КПР госп. св. Томаса №2 в аналогичном режиме
(табл. 3). Однако, при использовании КПР Кустодиол как в тепловом, так и в
холодовом режимах отмечалась худшая динамика восстановления сократимости сердца
(табл. 4), что в целом характерно для внутриклеточных КПР и является их
недостатком. Более того, при исследовании КПР Кустодиол в тепловом режиме имелась
недостоверная тенденция к увеличению размера некроза по сравнению с контролем
(табл. 3). Таким образом, КПР Кустодиол в отсутствии гипотермии вообще не
оказывает кардиопротективного действия. Это может быть связано со значительными
нарушениями трансмембранного градиента ионов натрия (в условиях нормотермии),
что может приводить к повреждению кардиомиоцитов и отсутствию кардиопротекции.
Влияние изолированной гипотермии на эффективность
защиты миокарда
В ряде
экспериментов было исследовано влияние на эффективность защиты миокарда
изолированной гипотермии в двух режимах - глубокой (+5°С) и промежуточной
(+22°С) гипотермии. В этих группах протокол эксперимента соответствовал
контрольной группе, но в течение всего периода тотальной 60-минутной ишемии
осуществлялось наружное охлаждение сердца.
# ** **
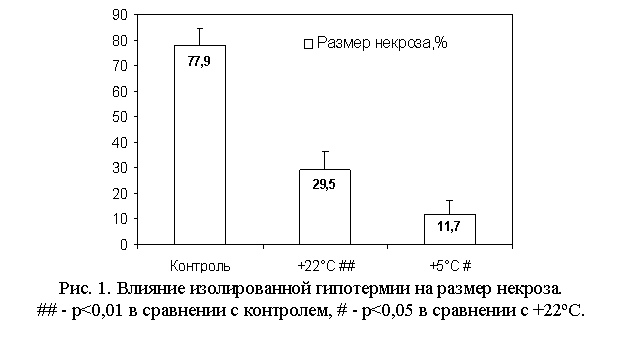
При ишемии и изолированной
гипотермии +5ºС асистолия возникала немедленно
после помещения сердца в охлаждающий раствор. При ишемии миокарда и
изолированной гипотермии +22ºС немедленной асистолии не наступало. Поэтому
сразу после ишемизации сердца в коронарные артерии в течение 10 секунд инфузировали
раствор, содержащий 25 ммоль/л KCl и 133 ммоль/л NaCl. Затем наступала тотальная ишемия. Кратковременность
инфузии и химический состав раствора исключают возможность наличия кардиопротективного
эффекта данной процедуры.
При
глубоком наружном охлаждении сердца до температуры +5ºС наблюдалась выраженная
кардиопротекция (рис. 1). Выраженность кардиопротекции при +22ºС была значительно
ниже, чем при глубокой гипотермии. Размер некроза при этом более чем в 2 раза превышал
значение, полученное при глубокой гипотермии, но был достоверно ниже, чем в
контрольной группе. С другой стороны, восстановление сократительной функции
левого желудочка в постишемическом периоде и динамика ишемической контрактуры в
ходе 60-минутной глобальной ишемии при +5ºС и +22ºС не различались
(табл. 5, 6).
Таблица 5.
Пульсовое (ПВЛЖД) и диастолическое (ДВЛЖД) давление в
левом желудочке в период реперфузии в экспериментах с изолированной гипотермией
|
Группа |
ПВЛЖД, мм рт. ст. |
ДВЛЖД, мм рт. ст. |
||
|
5 мин. |
30 мин. |
5 мин. |
30 мин. |
|
|
Контроль |
Асистолия |
17,5±6,5 |
99,2±5,3 |
91,4±7,6 |
|
ГТ
+5°С |
103,1±15,0** |
91,2±7,0** |
9,7±4,4** |
7,5±4,6** |
|
ГТ
+22°С |
105,4±12,9** |
93,5±14,8** |
8,2±4,6** |
6,2±2,8** |
Примечание: ГТ – гипотермия, **р<0,01 в сравнении с
контролем.
Таблица 6.
Динамика давления в левом желудочке в течение
60-минутной ишемии
|
Группа |
5 мин. |
15 мин. |
25 мин. |
35 мин. |
45 мин. |
55 мин. |
|
Контроль |
5,7±4,0 |
19,1±11 |
58,8±23,3 |
51,6±15,4 |
47,5±13,3 |
46,6±9,4 |
|
ГТ
+5°С |
5,4±2,7 |
4,2±3,0* |
4,3±3,3** |
4,4±2,1** |
4,1±2,8** |
4,0±2,7** |
|
ГТ
+22°С |
4,1±3,5 |
6,4±5,0* |
8,5±6,0** |
10,1±7,5* |
10,5±5,2** |
11,5±6,2** |
Примечание: ГТ – гипотермия, *р<0,05 в сравнении с контролем;
**р<0,01 в сравнении с контролем.
В литературе
имеются данные о том, что при снижении температуры ниже +22ºС усиление
протективного эффекта гипотермии прекращается, а повреждающее действие
возрастает (Buckberg G. D., 1991). Однако
проведенные эксперименты показали, что защитное действие гипотермии,
проявляющееся ограничением размера некроза, усиливаются при снижении
температуры миокарда в диапазоне от +22 ºС до +5 ºС.
Сравнение эффективности внеклеточных и внутриклеточных
кардиоплегических растворов
Важное
практическое значение для клинической практики, а также для понимания механизма
кардиопротективного действия КПР имеет сравнение эффективности КПР вне- и
внутриклеточного типа. Термин «внеклеточный КПР» означает, что концентрация
ионов натрия в составе КПР такая же, как в интерстициальной жидкости и плазме
крови или немного ниже, в диапазоне примерно от 100 до 145 ммоль/л; во
внутриклеточном КПР концентрация ионов натрия низкая, около 10-30 ммоль/л, что
примерно соответствует концентрации ионов натрия в цитоплазме клеток (Hensley F. еt al., 2008).
К КПР внеклеточного типа относятся, в частности, КПР№1 и КПР№1реф,
а к растворам внутриклеточного типа – КПР Кустодиол и КПР№3. В результате проведенных экспериментов было
обнаружено, что КПР№1 и КПР№1реф в тепловом режиме обеспечивают мощный
кардиопротективный эффект в виде уменьшения размера некроза, тогда как при
использовании КПР внутриклеточного типа (Кустодиол и КПР№3) в тепловом режиме
размер некроза не отличался от контрольной группы (рис. 2). Аналогичные данные
были получены и в отношении постишемического восстановления систолической и
диастолической функции левого желудочка.
Таблица 7.
Влияние кардиоплегических растворов вне- и внутриклеточного
типа на размер некроза (при +37ºС).
|
Группа |
Размер
некроза, % |
|
Контроль |
77,9±7,0 |
|
КПР№1 |
14±5,0** |
|
КПР№1реф |
8,8±3,8** |
|
КПР№3 |
83,4±2,8 |
|
КПР
Кустодиол |
83,9±8,6 |
Примечание: ** - p<0,01 в
сравнении с контролем.
Вероятно,
преимущество КПР внеклеточного типа перед внутриклеточными КПР состоит в том,
что в первом случае не нарушается ионный баланс натрия по обе стороны плазмалеммы
кардиомиоцита.
Исследование кардиопротективных свойств гипермагниевых,
гипербикарбонатных и маннитол-содержащих кардиоплегических растворов
Отдельные
теоретические предпосылки позволяют предполагать, что повышенная концентрация
ионов магния в КПР при нормальном уровне ионов калия способно обеспечить асистолию
и защитный эффект, сравнимый со стандартной гиперкалиевой КП. В настоящей
работе использование КПР№6 с концентрацией Mg2+ 16 ммоль/л
и нормальной концентрацией калия сопровождалось тенденцией к увеличению размера
некроза по сравнению с КПР№1 (табл. 7), однако скорость наступления асистолии была
такой же быстрой, как и в группе КПР №1.
Использование
КПР с повышенной концентрацией бикарбонат-аниона показало неудовлетворительные
результаты (табл. 7). Ожидалось, что повышенная буферная ёмкость КПР должна
оказать положительное влияние на состояние кардиомиоцитов благодаря уменьшению
внутриклеточного ацидоза. Возможным объяснением отрицательного результата может
являться исходно высокое значение рН этого КПР.
Таблица 8.
Размер некроза в экспериментальных группах с
использованием гипермагниевого, гипербикарбонатного и маннитол-содержащего КПР
(при температуре +37ºС).
|
Группа |
Особенность состава КПР |
Размер некроза, % |
|
Контроль |
- |
77,9±7 |
|
КПР№1 |
Внеклеточный
гиперкалиевый КПР на основе
БРКХ |
14±5,0* |
|
КПР№5 |
Гипербикарбонатный
КПР ([С]
HCO3 - 75
ммоль/л) |
56,3±7,4*# |
|
КПР№6 |
Гипермагниевый
([C] Mg2+ - 16 ммоль/л) КПР с нормальной концентрацией ионов
калия |
24,3±8,5* |
|
КПР№8 |
КПР
с добавление маннитола (106 ммоль/л) |
58,9±8,6*# |
Примечание: *-p<0,05 в сравнении с контролем; #-p<0,05 в сравнении с КПР№1.
Испытание
КПР с добавлением маннитола также показало отрицательные результаты, поскольку размер
некроза оказался достоверно выше, чем при использовании КПР№1 (табл. 7). Можно
предполагать, что в условиях ишемии, когда проницаемость микрососудов и
клеточных мембран повышена, маннитол выходит из внутрисосудистого во внесосудистое
пространство и способствует переходу воды в интерстиций и/или в клетку, усиливая
её отек и провоцируя лизис.
Таким
образом, результаты проведенных исследований показали, что использование
повышенной концентрации ионов магния в сочетании с нормальным уровнем калия не
имеет преимуществ по сравнению с гиперкалиевой КП, а увеличение содержания в
КПР бикарбоната выше физиологической концентрации и добавление маннитола
ухудшают защитные свойства КПР.
Кардиопротективная эффективность кардиоплегических
растворов
с повышенным уровнем глюкозы
Согласно
некоторым данным, повышение концентрации глюкозы в КПР приводит к возрастанию
их кардиопротективного потенциала за счет улучшения энергетического метаболизма
кардиомиоцитов в условиях ишемии.
Различие
в размере некроза между группами КПР№1 и КПР№1-Гл было недостоверным (табл. 8)
при наличии отчетливой тенденции к увеличению размера некроза в группе с
повышенной концентрацией глюкозы. При использовании КПР№1М-Гл величина некроза
была достоверно (р<0,05) выше, чем в группе с КПР№1. Между контрольной
группой и группой КПР№3 достоверной разницы по величине размера некроза не обнаружено
(табл. 8).
Вероятно,
отрицательный результат использования КПР№3 с концентрацией глюкозы 247 ммоль/л
можно объяснить поступлением глюкозы в кардиомиоциты с последующей ее анаэробной
утилизацией и накоплением лактата. Возникающий осмотический градиент
способствует транспорту внеклеточной воды внутрь клетки и наступлению ее осмотического
лизиса. Альтернативным объяснением неэффективности КПР№3 является его внутриклеточный
характер. Очевидно, что максимальное увеличение осмолярности КПР может способствовать
сохранению изо- или гиперосмолярности внеклеточного компартмента после
поступления глюкозы в клетку. С учетом этого были разработаны КПР№1-Гл и
КПР№1М-Гл. Результаты их испытаний оказались значительно лучше, чем КПР№3, но,
тем не менее, размер некроза при их применении был выше, чем в группе КПР№1. Полученные
результаты свидетельствуют о том, что для обеспечения максимального защитного
эффекта КПР концентрация глюкозы в нем не должна превышать 11 ммоль/л.
Таблица 9.
Размер некроза в экспериментальных группах с
использованием
кардиоплегических растворов (КПР) с повышенным уровнем
глюкозы
(при температуре +37ºС).
|
Группа |
Концентрация
глюкозы в КПР, ммоль/л |
Размер
некроза, % |
|
Контроль |
- |
77,9±7,0 |
|
КПР№1 |
11 |
14±5,0** |
|
КПР№3 |
247 |
83,4±2,8 |
|
КПР№1-Гл |
240 |
25,6±9,8** |
|
КПР№1М-Гл |
100 |
23,3±3,3**# |
**-p<0,01 в
сравнении с контролем; #-p<0,05
в сравнении с КПР№1
Исследование эффективности гиперполяризационной
кардиоплегии
Концепция
гиперполяризационной КП основана на более физиологичном способе достижения
остановки сердца за счет гиперполяризации мембраны кардиомиоцитов под действием
различных фармакологических агентов.
Таблица 10.
Размер некроза в экспериментальных группах с
использованием
гиперполяризационных КПР (при температуре +37ºС).
|
контроль |
77,9±7 |
|
КПР
№1 |
14±5
** |
|
КПР
№4 |
56,7±22,5
# |
|
КПР
№7 |
34,9±+11,1
** # |
|
КПР
№9 |
---------- |
** - p<0.01 в
сравнении с контролем, #- p<0.05 в
сравнении с КПР№1
В настоящем исследовании КПР№7, содержащий эсмолол в
концентрации 1 ммоль/л, вызывал надёжную асистолию, наступавшую несколько
медленнее, чем при использовании КПР№1 или КПР госп. Св. Томаса №2. При этом результат
по размеру некроза не может быть признан удовлетворительным (рис. 3).
Гиперполяризационная КП с помощью ацетилхолина (КПР№4) сопровождалась асистолией,
но при этом в течение периода ишемии наблюдались спонтанные систолы,
по-видимому, связанные с феноменом ускользания. Размер некроза в данной группе достоверно
не отличался от контроля (рис. 3). КПР№9,
содержащий аденозин, не вызывал надежной асистолии вне зависимости от его концентрации
в КПР, в связи с чем размер некроза не измерялся.
ВЫВОДЫ
1.
Разработанные на основе
буферного раствора Кребса-Хенселейта кардиоплегические растворы обеспечивают
высокую степень защиты миокарда от тотальной ишемии и превосходят по своей
эффективности известные кристаллоидные растворы, а именно, раствор госпиталя
Св. Томаса №2 и раствор «Кустодиол» в отсутствие сопутствующей глубокой
гипотермии.
2.
Включение в состав
кардиоплегического раствора маннита, а также наличие повышенной концентрации
бикарбонат-аниона или глюкозы ухудшает кардиопротективные свойства
кардиоплегического раствора.
3.
Эффективность
внеклеточных кардиоплегических растворов (имеющих физиологическую или слегка
пониженную концентрацию ионов натрия) превосходит эффективность внутриклеточных
растворов.
4.
Гиперполяризующие
кардиоплегические растворы, содержащие эсмолол или ацетилхолин в сочетании с
физиологической концентрацией ионов калия и магния, не обеспечивают должного
уровня защиты миокарда от тотальной ишемии; гиперполяризующий раствор,
содержащий аденозин, даже не обеспечивает достижения устойчивой асистолии.
5.
Изолированная
гипотермия, не сочетающаяся с кардиоплегией, является эффективным и безопасным
методом кардиопротекции при тотальной ишемии. При воздействии изолированной
гипотермии понижение температуры миокарда с 22ºС до 5ºС
сопровождается прогрессивным возрастанием эффективности кардиопротекции, однако
в случае сочетания гипотермии с кардиоплегией значение температуры в указанном
диапазоне не влияет на степень защиты миокарда.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1.
Разработанные в
результате работы кардиоплегические растворы, показавшие высокую
кардиопротективную эффективность, могут быть рекомендованы для тестирования в
клинических испытаниях.
2.
Полученные результаты
свидетельствуют о необходимости пересмотра возможности использования в
клинических условиях кардиоплегических растворов, содержащих маннит, а также с
высокой концентрацией глюкозы (100 и более ммоль/л).
3.
Среди различных
вариантов кристаллоидных кардиоплегических растворов преимущество следует
отдавать растворам внеклеточного типа, оказывающим более выраженный
кардиопротективный эффект.
4.
При выполнении холодовой
кристаллоидной кардиоплегии во избежание потенциального повреждающего действия
гипотермии возможно поддержание температуры миокарда на более высоком уровне,
чем общепринятые +10-11ºС, но не превышающем +22°С.
Литература
1.
С. М. Минасян, А. А.
Шмонин, К. А. Мищенко, М. М. Галагудза.
Использование методики перфузии изолированного сердца по Лангендорфу для исследования
эффективности кардиоплегических растворов // Актуальные проблемы
патофизиологии: Материалы межвузовской конференции молодых учёных. – СПб., 2006.
– С. 70–71.
2.
С. М. Минасян, И. А.
Шмонина, А. А. Кузьмина, Л. Р. Бадриханова. Сравнение гипотермии и тепловой
кардиоплегии как способов защиты миокарда от ишемического повреждения в
эксперименте // Актуальные проблемы патофизиологии: Материалы межвузовской
конференции молодых учёных. – СПб., 2007. – С. 89–91.
3.
С. М. Минасян, Л. Р.
Бадриханова, Д. И. Курапеев, Ю. В. Дмитриев, К. И. Ершова, Е. В. Сафрошина, М.
С. Васильева. Сравнительная оценка эффективности кардиоплегических растворов с
различным содержанием глюкозы в эксперименте // Актуальные проблемы
патофизиологии: Материалы межвузовской конференции молодых учёных. – СПб.,
2008. – С. 61-62.
4.
С. М. Минасян, М. С.
Васильева, И. С. Усков, Д. И. Курапеев, Д. А. Зверев, Е. А. Боброва, Ю. В.
Дмитриев. Сравнительное исследование кардиопротективной эффективности глубокой
и умеренной гипотермии при глобальной ишемии-реперфузии сердца крысы //
Актуальные проблемы патофизиологии: Материалы межвузовской конференции молодых
учёных. – СПб., 2009. – С. 76–77.
5.
С. М. Минасян, М. М.
Галагудза, М. С. Васильева, Д. А. Зверев, А. Е. Павлов, Е. А. Боброва.
Кардиопротекция за счёт управляемой гипотермии миокарда в эксперименте // Актуальные
вопросы кардиологии: Материалы ХVI ежегодной научно-практической конференции. –
Тюмень, 2009. – С. 160–161.
6.
Л. В. Губадова, С. М.
Минасян, М. С. Васильева, Ю. В. Дмитриев, И. С. Усков. Исследование
кардиоплегического раствора на основе раствора Кребса-Хенселейта в эксперименте
// Сб. тез. докл. II международного молодежного
медицинского конгресса «Санкт-Петербургские научные чтения – 2009». – CПб.,
2009. – С. 204.
7.
Л. В. Губадова, Ю. П.
Викторова, С. М. Минасян, Ю. Н. Григорова, Ю. В. Дмитриев, Е. А. Боброва, И. С.
Усков. Экспериментальное исследование кардиоплегического раствора на основе буфера
Кребса-Хенселейта, содержащего коллоидный компонент // Актуальные проблемы
патофизиологии: Материалы межвузовской конференции молодых учёных. – СПб.,
2010. – С. 53–55.
8.
С. М. Минасян, М. М.
Галагудза, Д. И. Курапеев, Ю. В. Дмитриев, Л. В. Губадова, Е. А. Боброва.
Экспериментальное исследование кардиоплегических растворов на основе буферного
раствора Кребса-Хенселейта // Бюллетень НЦССХ им. А. Н. Бакулева РАМН:
Материалы 14 ежегодной сессии научного центра сердечно-сосудистой хирургии им.
А. Н. Бакулева РАМН. – М., 2010. – С. 222.
9.
С. М. Минасян, Л. Р.
Бадриханова, М. М. Галагудза, Д. И. Курапеев. Сравнительное исследование
защитного эффекта гипотермии, ишемического прекондиционирования и
модифицированных кардиоплегических растворов при ишемии-реперфузии изолированного
сердца крысы // Регионарное кровообращение и микроциркуляция. – 2008. – Т. 7, №
2(26). – С. 72–78.
10. С. М. Минасян, М. М. Галагудза, Д. Л. Сонин, Е. А.
Боброва, Д. А. Зверев, Д. В. Королёв, Ю. В. Дмитриев, М. С. Васильева, Ю. Н.
Григорова, Т. Д. Власов. Методика перфузии изолированного сердца крысы // Регионарное
кровообращение и микроциркуляция. – 2010. – Т. 8, № 4(32). – С. 54–59.
11. С. М. Минасян, М. М. Галагудза, М. С. Васильева, Д. И.
Курапеев, Д. А. Зверев. Защита миокарда от глобальной ишемии/реперфузии с
использованием кардиоплегического раствора на основе буфера Кребса-Хензелайта
// Российский физиологический журнал им. И. М. Сеченова. – 2010. – Т. 96, № 4. –
С. 353–361.
12.
С. М. Минасян, М. М.
Галагудза, Д. И. Курапеев, Ю. В. Дмитриев, Ю. П. Викторова, А. Г. Павлов, Е. А,
Боброва, Т. Д. Власов. Разработка кристаллоидных кардиоплегических растворов на
основе буфера Кребса–Хенселейта // Сб. научных трудов «Трансляционная медицина»
(под ред. член-корр. РАМН, проф. Е. В. Шляхто). – СПб., 2010. – C. 333–344.