Физика/8. Молекулярная физика
к.т.н., доц. Магеррамов М. А.,
Бакинский Государственный Колледж
Пищевой Промышленности
Д.т.н., проф. Гореньков Э. С.
Всероссийский НИИ Консервной и
Овощесушильной Промышленности
О возможности расчета термодинамических свойств плодоовощных
соков на основе уравнения состояния
В
данной работе рассмотрена возможность оценки величин некоторых
термодинамических параметров (теплоемкость и др.) на основе уравнения состояния
с использованием основным термодинамических соотношений. Методика расчета
предложенная Гусейновым К.Д. [1], модифицирована нами в работах [2,3].
Для проведения
расчетов было использовано уравнение вида:
![]() , (1)
, (1)
где а0, а1 и а2 – являются постоянными для
каждой изотермы.
Для
температур Т= 280.16К
эти постоянные имели следующие значения:
а0 =
0,910707·10-3 ![]() , а1=
– 1,854436
, а1=
– 1,854436 ![]() , а2= –
41491,1449
, а2= –
41491,1449![]() .
.
С
изменением температуры эти значения также меняются.
Это
уравнение позволяет оценить величину изменения энтальпии, изобарной
теплоемкости, а также термические величины жидких пищевых продуктов (в. т.
числе гранатового сока).
Термодинамическая
выражение изменения энтальпии имеет вид:
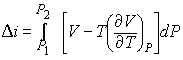 (2)
(2)
Для
вычисления этого интеграла надо определить величину ![]()
![]() из термического уравнения
состояния (1):
из термического уравнения
состояния (1):
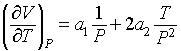 (3)
(3)
Значения
(1) и (3) подставим в (2)
и после интегрирования в пределах от Р1 до Р2
получим следующее уравнение:
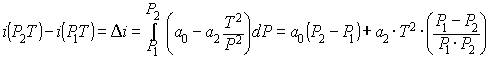 ;
;
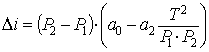 (4)
(4)
Эта
зависимость позволяет вычислить изменение энтальпии гранатово-го сока при
различных температурах в пределах давления от Р1 до Р2.
Нами
вычислены значения Δi при различных температурах и
давлении ΔР = 10 МПа
Эти
результаты представлены в таблице 1.
Таблица 1.
Значение Δi для гранатового сока сорта Гюлейша Азербайджанская
при различных температурах и давлении Р=10 МПа
|
Т, К |
280.16 |
304.18 |
334.19 |
362.19 |
378.17 |
402.18 |
|
|
40.880 |
45.700 |
52.700 |
60.514 |
66.130 |
76.130 |
Графическая
зависимость ![]() при
при ![]() является характерной
кривой для жидкой фазы вещества. Согласно методике расчёта изменения энтальпии
с помощью зависимости
является характерной
кривой для жидкой фазы вещества. Согласно методике расчёта изменения энтальпии
с помощью зависимости ![]() нами определено значение
энтальпии для температурного шага
нами определено значение
энтальпии для температурного шага ![]() К при Р=10
МПа.
К при Р=10
МПа.
Графический
анализ функции ![]() позволил установить
следующую эмпирическую зависимость:
позволил установить
следующую эмпирическую зависимость:
![]() (5)
(5)
Здесь
С0=161.280![]() , С1= –
4.658
, С1= –
4.658![]() , С2=0.01516
, С2=0.01516![]() .
.
Теперь
мы можем воспользоваться следующей термодинамической зависимостью, для расчета
изобарной теплоемкости (Ср)
гранатового сока:
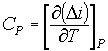 (6)
(6)
Тогда
производная от (5) по температуре дает для теплоемкости следующую зависимость:
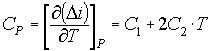 ,
,![]() (7)
(7)
Таким
образом, мы определили зависимость СР=φ(Т) при Р=10МПа, с помощью которой можно вычислить
значение изобарной теплоемкости гранатового сока при различных температурах.
Эти
данные приводятся в таблице 2.
Таблица 2.
Изобарная теплоемкость гранатового сока сорта Гюлейша
Азербайджанская. при Р=10МПа
|
Т,К |
280.16 |
320.16 |
334.16 |
362.16 |
402.18 |
|
|
3.832 |
5.022 |
5.629 |
7.055 |
7.532 |
Полученные
значения теплоемкости могут быть использованы как опорные данные для
определения зависимости изобарной теплоемкости от давления; определим эффект
давления на изобарную теплоемкость.
Для
этой цели можно воспользоваться следующей термодинамической зависимостью:
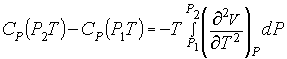 , (8)
, (8)
где Ср (Р2Т) и Ср (Р1Т) – значения теплоемкости при
давлениях Р2 и Р1 и температуре Т. Чтобы оценить значение интеграла
допустим, что при Р=const зависимость удельного объема от температуры имеет вид:
![]() (9)
(9)
Вторая
производная по Т от этой зависимости
позволяет определить при Р=const:
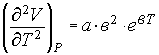 (10)
(10)
Эти результаты
позволяют получить из (8):
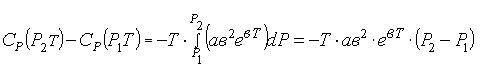 (11)
(11)
Если
учесть, что ![]() , тогда получим:
, тогда получим:
![]() (12)
(12)
Значение
в определяется из (11) следующим
образом:
Из
формулы ![]() для двух значений V и Т при Р=const получим:
для двух значений V и Т при Р=const получим:
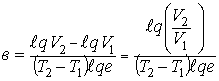 (13)
(13)
Ниже
приводятся результаты вычисления значения в,
а также комплекса ![]() при различных
давлениях (Р1=30МПа
и Р2=50 МПа):
при различных
давлениях (Р1=30МПа
и Р2=50 МПа):
При
Т=280.01К и в=2.3397
ּ10-4,(1/К) получим:
![]()
![]()
Так
вычисляется в и комплекс ![]() для других
температур. Тогда зависимость (12) может быть записана в следующей форме:
для других
температур. Тогда зависимость (12) может быть записана в следующей форме:
![]() , (14)
, (14)
где значения СР(Р1Т)=СР(10МПа,Т)
приведены в таблице (2). По
зависимости (14) мы определили
значения изобарной теплоемкости при раз-личных температурах и давлениях. Эти
результаты приводятся в таблице 3.
Таблица 3.
Изобарная теплоемкость гранатового сока сорта Гюлейша
Азербайджанская. ![]()
|
Т, К |
Давление, МПа |
||
|
10 |
30 |
50 |
|
|
280.16 |
3.382 |
3.500 |
3.269 |
|
320.16 |
5.022 |
4.695 |
4.459 |
|
340.16 |
5.629 |
5.280 |
5.021 |
|
362.16 |
7.055 |
6.682 |
6.405 |
|
402.18 |
7.532 |
6.906 |
6.806 |
Имея
значения при 293К теплоемкости, удельного объема и коэффициента теплопроводности
можно оценить величину температуропроводности a получим:
![]() и
и ![]()
для температуры ![]()
Термическое
уравнение состояния (1)
позволяет определить также термические величины (тепловое расширение αр
и изотермическую сжимаемость βТ:
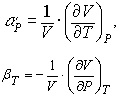 (15)
(15)
Тогда
величину изохорной теплоемкости можно легко определить термодинамическим соотношением:
![]() , (16)
, (16)
![]() . (17)
. (17)
По
теории жидкостей и растворов предложены несколько работ. Имеется теория
вязкости М.Ф.Широкова, Егера, Бриллуэна, А.М.Бачинского, Ференкеля, Панченко и
др. [4,5]. Но все эти теории имеют определенные ограничения. Мы здесь
рассмотрим теорию А.М.Бачинского и Френкеля. Предложенные ими расчетные
уравнения для вязкости жидкости имеют теоретические основы, хотя и не описывают
вязкостные свойства многих жидкостей. А.М.Бачинский экспериментально обнаружил,
что между удельным объемом жидкости и ее текучестью существует линейная зависимость.
Это положение нами проверялось для гранатового сока сорта Гюлейша Азербайджанская.
Получена линейная зависимость. Уравнение прямой в координатах ![]() будет иметь вид:
будет иметь вид:
![]() , (18)
, (18)
где ![]() , ω – собственный объем частиц жидкости, С – определенная постоянная.
, ω – собственный объем частиц жидкости, С – определенная постоянная.
На
основании полученной линейной зависимости легко определяются ω и С.
Теория
Френкеля более точно описывает вязкость жидкой фазы вещества, где предлагается
следующая формула:
![]() (19)
(19)
где к – постоянная Больцмана, ΔU – энергия активации частиц, А – величина постоянная. Формула (19)
хорошо передает экспоненциальную зависимость вязкости от температуры. Энергии
активации можно определить из формулы (19) на основании опытных значений
вязкости η1 и η2:
![]() (20)
(20)
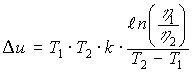 (21)
(21)
Для
гранатового сока можно определить значения для температур Т2=334.16 К и Т1=310.27
К.
При
этих условиях для энергии активации сока получим следующее значение:
ΔU =1.2·10-20Дж.
(22)
Расчёт
энергии активации при более высоких температурах показывает её уменьшение, что
соответствует закономерностям молекулярной физики. При нагреве сока объем его
увеличивается, то есть увеличивается расстояние между частицами, а также
координационное число, что способствует уменьшению энергии активации.
Таким
образом, предложенная нами методика расчета калорических (Ср, Сv), а также изменения термодинамических
и термических величин при различных параметрах состояния может быть применена
многокомпонент-ным пищевым жидкостям, каким является также гранатовый сок.
Литература
1.
Гусейнов К.Д.
Исследование термодинамических и переносных свойств ряда кислородсодержащих
органических веществ в широком интервале параметров состояния: Автореф. Дисс…
д- ра техн. наук. Баку, 1979.
2. Магеррамов М. А. Свойства плодов граната и их хранение
в модифици-рованной атмосфере. Баку, ААСУ, 2002, 185 с.
3. Магеррамов М.А.Математическое описание расчетов
теплофизических величин жидких пищевых продуктов // Производство и ремонт
машин: Сборник материалов международной научно-технической конференции – Ставрополь:
Издательство Ст. ГАУ «АГРУС», 2005. с. 191-197.
4. Панченков Г. М. Теория вязкости жидкостей,
Гостехиздат. М.-Л. 1947 г.
5. Юсупов . Расчет теплоемкости хлопкового масла при
повышенных параметрах температуры и давления //Хранение и переработка
сельхозсырья. 1996. № 4. с. 9-11