Технические науки /
6.Электротехника и радиоэлектроника
К.т.н. Микитенко В.И.
Национальный технический университет Украины «Киевский
политехнический институт», Украина
Моделирование и разработка многоканальных средств диагностики состояния
человека на основе анализа его инфракрасного излучения
Обеспечение хорошего
состояния здоровья населения является национальным приоритетом любой развитой
страны. Своевременное диагностирование заболеваний и их лечения повышают срок
активной жизнедеятельности человека на 15-20 %, что дает значительный
экономический эффект. Одним из направлений диагностирования является
медицинская термодиагностика, заключающаяся в регистрации пространственного
распределения собственного инфракрасного излучения человека с помощью
тепловизора и в следующем визуальном анализе термограммы. Популярность
термодиагностики обусловлена тем, что она дает возможность распознать симптомы
более 150 разных заболеваний на самых ранних стадиях их возникновения [1].
Ни один из существующих диагностических методов не имеет такой широты
диагностического диапазона, возможности выявления сразу многих групп
заболеваний. Высока также информативность метода – точность тепловизионной
диагностики при некоторых заболеваниях приближается к 100%, а в целом для
первичных обследований равна порядка 80%. К преимуществам современной
тепловизионной диагностики относится также возможность определять заболевание
задолго к него клинического проявления и даже при бессимптомном течения
болезни.
Сейчас
большой потенциал термодиагностических обследований является нереализованным
вследствие отсутствия точных моделей преобразования информации, которые
сопровождают возникновение аномальных состояний биологических объектов, его
регистрацию тепловизионными системами, а также восприятие и интерпретацию
наблюдателем.
Эффективность термодиагностики определяется двумя основными факторами –
полнотой регистрации тепловизором значимых признаков заболеваний и точностью
интерпретации тепловизионного изображения наблюдателем. Обеспечение адекватной
реализации обозначенных факторов на практике означает наличие недорогих
эффективных медицинских тепловизоров и моделей преобразования информации от
патогенных зон к зрительной системе наблюдателя. Разработке технических
аспектов термодиагностики и практическому использованию
термографии в биомедицинских исследованиях посвящено много работ отечественных
и зарубежных авторов, таких как, Г.Р.Иваницкий, Л.Г. Розенфельд, R.N. Lawson,
Б.Г. Вайнер и другие [2]. Однако, почти во всех роботах
тепловизор рассматривается как прибор наблюдения и радиометрии тепловых полей в
организме человека. Хотя экспериментальные и теоретические исследования
физиологии человека в части формирования теплового поля весьма распространены в
мире, вопросы образования тепловых полей под действием заболеваний изучены не
достаточно и практически отсутствуюет термографическая база данных (на подобие
рентгенографической). В настоящее время можно
констатировать, что комплексные исследования формирования инфракрасного
излучения патологическими зонами человека с одновременной разработкой методов
регистрации этого излучения, а также методик проектирования медицинских
тепловизоров с согласованными характеристиками основных блоков, объекта
наблюдения и зрительной системы являются недостаточными. Особенно актуальными
являются разработки конкретных недорогих технических решений, которые могут
быть внедрены в серийное производство.
На сегодня в медицинских
тепловизорах наиболее целесообразно использование микроболометрических матриц.
Для создания эффективного прибора необходимо разработать математическую модель
формирования и преобразования информации от патологической зоны человека к
наблюдателю, а также методы проектирования тепловизоров на микроболометрической
матрице с согласованными характеристиками объектива и матрицы для повышения
достоверности и прогностических возможностей получаемой диагностической
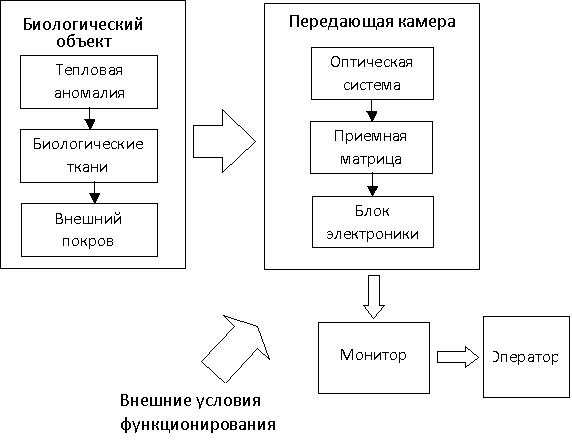
информации. Блок-схема модели изображена на рис. 1.
|
|
|
Рисунок 1 – Схема математической модели |
В
процессе исследований было проанализировано современное состояние медицинской
термодиагностики и обоснованы требования к характеристикам и параметрам
медицинских тепловизоров; определены факторы, которые влияют на изменение
поверхностной температуры кожного покрова; разработана математическая модель
инфракрасного излучения в патологической зоне для определения распределения
температуры внутри мышечных тканей и глубину расположения этой зоны, а также
модель, которая описывает процесс преобразования инфракрасного излучения от
зоны заболевания пациента к тепловизору с дальнейшим восприятием термограммы
наблюдателем для ее интерпретации. Были разработаны методы проектирования
медицинских тепловизоров, которые обеспечивают заданную температурную и
пространственную разрешающую способности, и методики согласования аберраций
объектива и геометрических параметров микроболометрической матрицы для
повышения качества изображения.
Основная идея проекта состояла в единой
архитектуре процесса разработки медицинских тепловизоров, которая содержит пять взаимосвязанных уровней формирования и
преобразования информации. Первый - медико-инженерный уровень состоит из модели
образования тепловых аномалий в биологических объектах (в частности – в
организме человека) при типичных нарушениях состояния организма. Второй уровень
объединяет медико-инженерные и технические методы для описания формирования
излучения внешних покровов объекта в инфракрасном диапазоне спектра. Два
обозначенных уровня фактически содержат математические модели формирования
значимых признаков фоно-целевой обстановки для дальнейшей их регистрации медицинским
тепловизором и интерпретации оператором. Третьей и четвертый уровни архитектуры
касаются непосредственно тепловизионных передающих камер в частях моделирования
превращения сигналов в них, согласования характеристик отдельных блоков между
собой и их адаптации к входным сигналам. Последний уровень описывает принятие
решения оператором термодиагностического комплекса относительно состояния
биологического объекта. При этом важно в полной мере учесть особенности
зрительного восприятия тепловизионных изображений патогенных зон оператором в
ходе их интерпретации. Уменьшение стоимости диагностического комплекса можно
ожидать за счет использования на третьем и четвертом уровнях методики расчетов
медицинской передающей тепловизионной камеры на основе недорогой микроболометрической матрицы.
Значительное внимание уделено исследованиям
биологического объекта на основе контроля динамики наиболее интегральных
показателей его функционального состояния (температуры и кислородного статуса)
с применением современных аппаратно-программных средств, которые используют
разные физические процессы. Это дает возможность быстрее и достовернее получать
информацию о состоянии человека, чем при использовании каждого метода отдельно.
Фактически термодиагностический комплекс с точки зрения источников информации
является многоканальным. Для обеспечения адекватного количества релевантной
информации на экране монитора были использованы методы комплексирования
информации [3]. Был разработан новый метод
комплексирования изображений на основе показателя успешности выполнения задачи (TTP - the targeting task
performance metric [4]).
Получены
как научные теоретические, так и прикладные результаты. В частности разработана
методика согласования параметров матричного приемника излучения с фокусирующей
оптической системой [5], предложен метод выявления термоаномальних зон на
поверхности тела человека с помощью инфракрасной термографии, проведения
анализа и интерпретация полученных данных с учетом кислородного статуса
организма (размеры и места локализации термоаномальних зон, температурные
градиенты, величина парциального давления кислорода в подкожных тканях). Пример
практического применения разработанных методов к диагностированию сосудистых
патологий приведен на рис. 2.
|
а) б) |
|
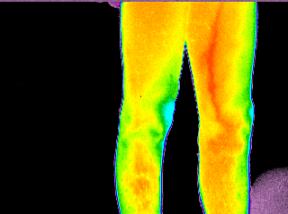
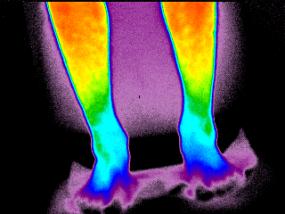
Рисунок
2 - Термограммы пациентов с сосудистыми патологиями: а) –
варикозно-измененная большая подкожная вена левого бедра; б) – нарушение
кровоснабжения дистальных отделов |
Показана (рис.2 а)
термограмма пациента с варикозно-измененной большой подкожной веной левого
бедра. Различие температуры с симметричным участком правого бедра
составляет 3,2°С. На рис. 2 б) представлена термограмма нижних
конечностей пациента, который жалоб не предъявлял, однако при обследовании
которого были выявлены снижения температуры до 28°С (показано стрелками) в
сравнении с относительной нормой 32,5°С. После дополнительной осцилометрии и
капиляроскопии сосудов стоп выявлена функциональная недостаточность
кровоснабжения дистальных отделов.
В целом была создана
научная основа для проектирования медицинских тепловизоров, которые
обеспечивают оптимальные для термодиагностики человека характеристики. В
дальнейшем для повышения эффективности массовой термодиагностики планируется
усовершенствовать методы обработки инфракрасных изображений на основе карт
информативности.
Литература:
1. Хижняк Л.Н. Диагностика
и контроль эффективности лечения заболеваний сосудов нижних конечностей с
использованием матричных термовизионных систем: дис. ... канд. мед. наук / Хижняк Л.Н. . –
Тула, 2005.
2. Розенфельд
Л.Г. Основы клинической дистанционной термодиагностики / Л.Г. Розенфельд. –
Киев: Здоровье, 1988. – 222 с.
3. Колобродов В.Г., Микитенко В.І. Комплексування інформації в
багатоканальних оптико-електронних системах спостереження: монографія /
Поліграфічний центр «Аверс», Київ, 2013. – 178 с.
4. Vollmerhausen
R. H. The targeting task performance (TTP) metric. A new model for predicting
target acquisition performance / Richard H. Vollmerhausen, Eddie Jacobs //
Technical report AMSEL-NV-TR-230. – 2004. – 126 p.
5. Рибалко М. С., Микитенко В. І., Мамута О. Д.
Узгодження діаметрів вхідних зіниць дзеркально-лінзового об’єктиву двоканальної оптико-електронної системи спостереження //
Вісник національного технічного університету України «КПІ», Приладобудування. –
2011. – № 42. – С. 54-61.