Медицина/8. Морфология
к.м.н. Купша
Е.И., доцент Бондаренко В.В.
Государственное учереждение “Крымский государственный медицинский университет
имени С.И. Георгиевского”, АР Крым, Украина
Гормезис. Морфологические признаки срыва адаптивной реакции при избыточной
митофагии, в гепатоцитах мышей при поступлении в организм ацетата свинца.
Известно, что низкие дозы токсинов и другие стрессоры
активируют адаптивный ответ организма против высоких доз того же агента. Этот
феномен обеспечивающий благоприятный биологический ответ известен как гормезис.
Одним из цитопротективных механизмов гормезиса, обеспечивающим выживание
клетки, является митофагия. В условиях физиологического оптимума митофагия
вносит вклад в поддержание клеточного гомеостаза удаляя потенциально опасные
или избыточные митохондрии, что способствует увеличения продолжительности жизни
и поднятию порога для повреждения, индуктирующего клеточную дисфункцию и
смерть. Высокие дозы агентов стимулирующие оба процесса – аутофагию и смерть
являются токсичными для клетки, в то время как низкие дозы, тех же агентов
вызывают гормезисный ответ адаптирующий клетки к стрессу [1].
Свинцовая интоксикация моделировалась нами на 6 самцах
белых мышей линии balb/c, которым, начиная с 1-месячного возраста, ежедневно
перорально вводили ацетат свинца в дозе 10 мг/кг/сутки в течение 60 суток.
Напряженность реализации репаративных процессов путем
внутриклеточной гиперплазии митохондрий с целью обеспечения гепатоцитов
энергодающими субстратами и недопущения органной недостаточности диагностировалась
незначительным превышением морфометрического показателя их площади профильного
поля в опыте над контрольными значениями - 24,35±0,08% и 21,00±0,9% (р
< 0,05). Существуют доказательства, что
увеличенное количество митохондрий может быть избыточным ввиду ослабления их
функции [2]. Известно, что аутофагия и биогенез работают как взаимосвязанные
механизмы обеспечивающие митохондриальное качество и клеточный гомеостаз. Возможно,
возрастание биогенеза является компенсаторным механизмом при дефектной
митохондриальной функции и в отсутствии сбалансированной митофагии дефектных
митохондрий неадаптивен. Ограничение
энергии стимулирует митофагию и в ответ митохондриальный биогенез [3].
Наблюдаемые частые картины слияния наружной мембраны
митохондрий с ГрЭПС, трактуемые рядом авторов как начальные этапы аутофагии,
призванной удалить поврежденные органеллы с целью недопущения индукции
митохондриального апоптозного пути и попытки компенсации нутриональной
недостаточности, могут свидетельствовать о развитии синдрома
капилляро-трофической недостаточности. Электронномикроскопический анализ выявил
ультраструктурные признаки некробиоза гепатоцитов. Очевидно, что клетки с
глубокими инвагинациями кариолеммы, кариопикнозом и тенденцией к маргинации
ядерного хроматина могут погибать как механизмом некроза, так и апоптоза (рис. 1).
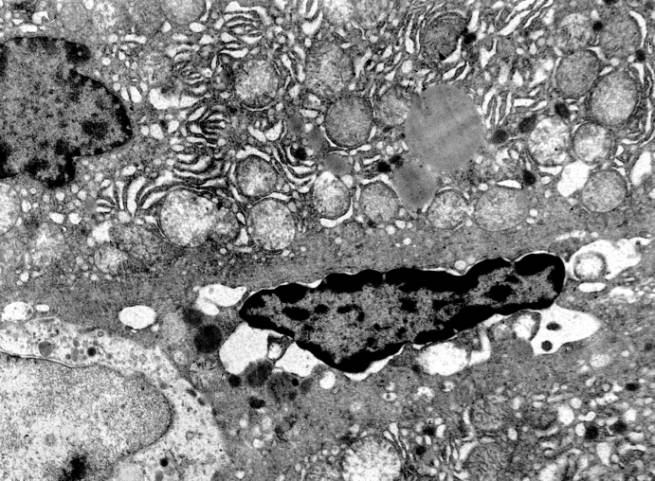
Рис.
1. Митофагия. Некробиоз гепатоцита. Сужение просвета гемокапилляра и
пространства Диссе. Гидропическая дистрофия и набухание ядра эндотелиоцита.
Самоповреждение клетки Купфера. Электронная микрофотография. Ув. х 12000.
Считается невозможным определить – является ли
возрастание аутофагических вакуолей результатом адаптивного ответа или
предвестником смерти клетки [4]. В тоже время, стабильно верифицируемые нами признаки
гемической гипоксии и морфологически подтвержденное отсутствие
приспособительного результата со стороны сосудистого русла при длительном
поступлении в организм малых доз свинца свидетельствуют о формировании
критически неблагоприятной метаболической микросреды для полноценной реализации
адаптивных программ гепатоцитов [5].
Таким образом, реализация долгосрочных адаптивно-приспособительных
реакций на внутриклеточном уровне гепатоцитов, околососудистых (иммуноцитов,
эндотелиоцитов) и стромальных коллагенсинтезирующих клеток возможна только в
условиях интегративной кооперации и развертывания саногенетических процессов
охватывающих все структурно-функциональные компоненты печеночных долек,
благополучие внутри которых гарантирует функциональную адекватность органа.
Литература:
1. Isabelle Martins. Hormesis, cell death and
aging /Isabelle Martins, Lorenzo Galluzzi and Guido Kroemer // AGING – 2011. – Vol.3,№9 – P.821-828.
2. Duncan JG. Insulinresistant heart exhibits a mitochondrial biogenic
response driven by the peroxisome proliferator-activated
receptor-alpha/PGC-1alpha gene regulatory
pathway / Duncan JG, Fong JL, Medeiros DM, Finck
BN, Kelly DP. // Circulation – 2007. – Vol.115 – P.909–917.
3. Gottlieb RA. Autophagy in
health and disease: 5. Mitophagy as a way of life / Gottlieb RA, Carreira RS. //
Am J Physiol Cell Physiol. – 2010. – Vol.299 – P.203-210.
4. Eizo Watanabe. Sepsis induces extensive
autophagic vacuolization in hepatocytes: a clinical and laboratory-based study /
Eizo Watanabe, Jared T Muenzer, William G Hawkins, Christopher G Davis, David J
Dixon, Jonathan E McDunn, Daniel J Brackett, Megan R Lerner, Paul E Swanson6 and
Richard S Hotchkiss // Laboratory Investigation – 2009. – Vol.89 – P.549–561.
5. Купша Е.И. Состояние
митохондрий гепатоцитов, внутридольковых и приносящих междольковых кровеносных
сосудов печени мышей при длительном поступлении в организм субтоксических доз
свинца /
Е.И. Купша, В.В. Бондаренко, А.Н. Грабовой // Проблемы, достижения и перспективы развития медико-биологических наук и
практического здравоохранения: тр. Крым. гос. мед. ун-та им. С.И. Георгиевского.
– Симферополь, 2006. – Т. 142, часть I. – С. 37–43.