Химия и химические технологии / 5. Фундаментальные проблемы создания новых материалов и технологий
*Донец С.С., *Бондарев
Н.В., **Зайцева И.С.
*Национальный
университет имени В.Н. Каразина, Харьков, Украина
**Харьковская
национальная академия городского хозяйства, Украина
Влияние состава
водно-ацетонитрильного растворителя на равновесный выход коронатов магния ([18C6Mg]Cl2)
Цель работы: моделирование равновесного выхода
короната магния (18-краун-6)MgCl2 в водно-ацетонитрильных (AN)
растворителях с содержанием ацетонитрила до XAN
= 0.35.
Задачи исследования: обосновать идентичность
термодинамических констант равновесий комплексообразования: Мg2+ + 18C6 = (18C6)Мg2+ и МgCl2 + 18C6 = (18C6)МgCl2; K[(18C6)Мg2+]=K[(18C6)МgCl2];
разработать итерационную процедуру определения концентрационных констант
устойчивости краун-эфирных комплексов хлорида магния (несимметричного
электролита); обосновать взаимосвязь между концентрационными константами
комплексообразования через эффекты среды (параметры переноса, первичные солевые
эффекты и эффекты равновесных
концентраций реагентов) при замене растворителя; оценить влияние первичных
эффектов водно-органических растворителей, первичных солевых эффектов и
равновесных концентраций реагентов на выход
короната магния.
Из условий химического равновесия
вытекает, что
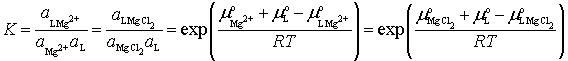 ,
,
следовательно K[(18C6)Мg2+]=K[(18C6)МgCl2], где
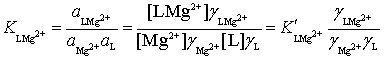 ,
,
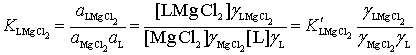 , L = 18C6
, L = 18C6
Ожидаемый равновесный выход хлорида короната
магния ![]() определялся по мольной доле этого вещества в равновесном состоянии
истемы:
определялся по мольной доле этого вещества в равновесном состоянии
истемы:
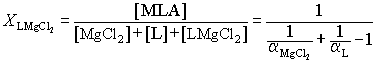
Последовательность
итерационной процедуры: в качестве начального приближения при оценке степени
комплексообразования используется термодинамическая константа устойчивости
короната магния; определяются равновесные концентрации реагентов: [MgCl2], [LMgCl2], [L]; определяется активность
растворителя; оцениваются средние ионные коэффициенты активности электролитов
по уравнению Робинсона-Стокса и коэффициенты активности лиганда; определяется
концентрационная константа устойчивости короната магния; итьерации повторяются
с учетом концентрационной константы комплексообразования до сходимости
результатов по степени комплексообразования (третий знак после запятой).
Показано (рис. 1), что начиная с концентраций ![]() = 1.2 и mоL = 0.6 моль/(кг растворителя) выход продукта LMgCl2 остается практически постоянным в
смесях с содержанием ацетонитрила 0.2 – 0.35 мольных долей.
= 1.2 и mоL = 0.6 моль/(кг растворителя) выход продукта LMgCl2 остается практически постоянным в
смесях с содержанием ацетонитрила 0.2 – 0.35 мольных долей.
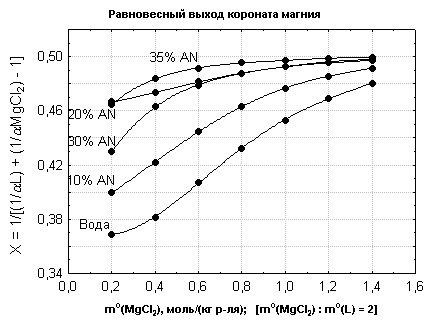
Рис.
1. Зависимость выхода короната магния в воде и водно-ацетонитрильных растворителях
от концентрации соли и лиганда
Для концентрационных констант ![]() образования комплексов хлоридов
короната магния в воде (w) и смешанном растворителе (sw) имеем
образования комплексов хлоридов
короната магния в воде (w) и смешанном растворителе (sw) имеем
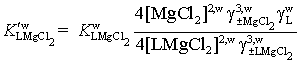 и
и 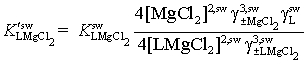
Тогда при замене воды на водно-ацетонитрильный
растворитель
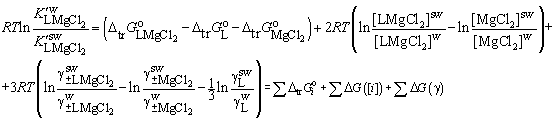
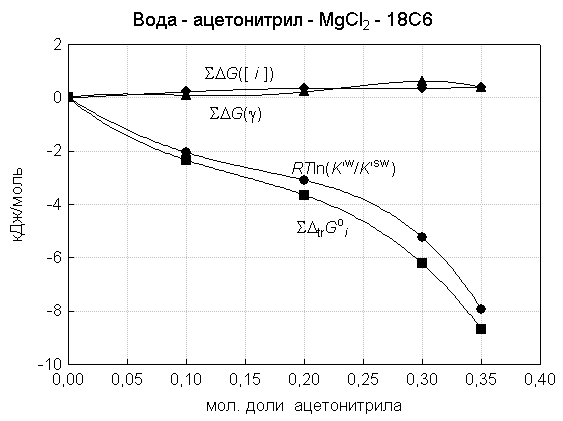
Рис. 2. Вклады первичных эффектов среды ![]() , равновесных
концентраций реагентов
, равновесных
концентраций реагентов ![]() и солевых эффектов
и солевых эффектов ![]() в изменение выхода продукта реакции MgСl2
+ L = LMgCl2
в изменение выхода продукта реакции MgСl2
+ L = LMgCl2
Увеличение выхода хлорида короната магния
в водно-ацетонитрильных растворителях зависит (рис. 2) преимущественно от
первичных эффектов среды (энергии Гиббса пересольватации реагентов).