Химия и химические
технологи
5. Фундаментальные
проблемы создания нових материалов и технологий
К.ф.-м.н. Скобєєва В.М., д.ф.-м.н.
Сминтина В.А., к.ф.-м.н. Малушин М.В.
Науково-дослідний інститут фізики Одеського національного університету імені І. І. Мечникова
Низько-температурний синтез
нанокристалів сульфіду кадмію у водному розчині желатини
Напівпровідникові нанокристали є важливим класом матеріалів внаслідок набування
через їх нанометровий розмір унікальних фізико-хімічних, електричних та оптичних властивостей.
Одним з методів приготування наночастинок є колоїдно-хімічний, в основі
якого лежить хімічна реакція між реагентами в розчині у присутності
стабілізаторів. Вибір стабілізатора визначається багатьма чинниками. Головним чинником є його здатність перешкоджати коагуляції
частинок, запобігаючи
їх подальшому росту. До стабілізаторів, які
найчастіше використовуються, відносяться органічні сполуки, наприклад,
поліфосфаты [1-4], триоктілфосфіни [5], і тіоли| [6]. Характеристики напівпровідникових матеріалів,
отриманих у
вищезгаданих стабілізаторах, приведені в роботі [7]. Проте органічні речовини
можуть бути екологічно небезпечними та дорогокоштовними.
З цієї точки зору придатним стабілізатором може
служити природний полімер – желатина, яка добре зарекомендувала себе у
виготовленні фотоматеріалів [8]. Желатина має значну
в”язкість, добру кліючу здатність,
низьку температуру плавлення (38 - 40о С). Желатина є високомолекулярним
з'єднанням, елементарна ланка якого представлена в ізоелектронному стані у
вигляді формули H2N-R1-COOH, що складається з амінових (H2N),
карбоксильних (COOH), полярних і неполярних основних і кислотних груп (R1).
Желатина є хорошим дисперсійним середовищем для нано- і мікрочасток. У желатину
швидко проникають розчини, що містять іони атомів металів і халькогенів.
Желатинові розчини здатні утворювати гелі, з яких при полімеризації виходять
досить міцні і прозорі плівки. Крім того, желатина є доступним, дешевим і
нетоксичним матеріалом.
На підставі вищевикладеного представляє інтерес отримання і дослідження нанокристалів сульфіду кадмію із
застосуванням желатинового розчину у якості стабілізуючого агенту. У синтезі НК
сульфіду кадмію у якості стабілізатора було використано два типа водних
розчинів желатин: харчової (I тип) та фотографічної (II тип) [8]. Для контролю процесу
синтезу нанокристалів сульфіду кадмію, їх розмірів проведені дослідження
спектрів оптичного поглинання, які відносяться до неруйнівних методів, що чутливі до
квантово-розмірних ефектів.
Синтез сульфіду кадмію здійснювався в результаті
обмінної хімічної реакції, що протікає у присутності желатинового розчину [9] при температурі 40оС
Cd(NO3)2 + Na2S
= CdS + 2NaNO3.
НК CdS були отримані в водних розчинах (5%) двох типів желатини при
однакових умовах синтезу. Через певні інтервали часу (1, 4, 8 і 12 хв) із
реакційного об`єму відбирали проби з розчином об`ємом 3 мл, який поливали на
скляні підкладки і отримані зразки висушували при кімнатній температурі.
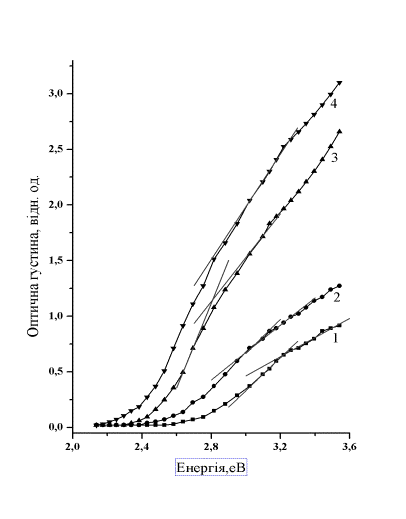
Спектри поглинання нанокристалів CdS типу I, II представлені на рисунках 1
і 2, відповідно. Край полоси поглинання, як для зразків типу I, так і типу II,
зміщений в область більших енергій відносно ширини забороненої зони об`ємного
сульфіду кадмію (2,5еВ [10]). Цей факт пояснюється
квантово-розмірним ефектом і є характерним для поглинання світла нанорозмірними
об’єктами. За законом міжзонного поглинання світла
сферичними наночастинками енергія першого оптичного переходу
(„ефективна” ширина забороненої зони) збільшується із зменшенням радіусу сферичної
наночастинки відносно ширини забороненої зони об’ємного
кристалу на величину, яка має назву енергії розмірного квантування [11]
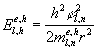 , (1)
, (1)
де
h – стала Планка; l і n – орбітальне та головне головне квантові числа; φl,n –
корені функції Бесселя, зокрема для першого оптичного переходу φ01
= 3,142; me,h – ефективні маси електрона та дірки. „Ефективна”
ширина забороненої зони (перший оптичний перехід, який відповідає переходу з
квантовими числами l=0, n=1),
Рис.1. Спектри
поглинання зразків типу I
в залежності
від часу синтезу, хвилини:
1(1), 4 (2),
8 (3), 12 (4).
визначалась
по значенню енергії, яка відповідає точці перегину на кривих поглинання [11]. Оцінені
таким методом величини „ефективної” ширини забороненої зони та, за виразом (1),
середнього радіусу нанокристалів CdS для різних інтервалів синтезу зведені у
таблицю 1.
Таблиця 1
Значення ширин забороненої зони Eg та середнього радіусу r нанокристалів CdS I та II типів в
залежності від часу синтезу
|
Час синтезу, хв. |
EgI ,eB |
EgII ,eB |
rI, нм |
rII, нм |
|
1 |
3,24 |
3,37 |
1,40 |
1,30 |
|
4 |
3,05 |
3,37 |
1,65 |
1,30 |
|
8 |
2,83 |
3,25 |
2,10 |
1,40 |
|
12 |
2,78 |
3,15 |
2,30 |
1,50 |
Помітно, що зі збільшенням концентрації реагентів ширина забороненої зони в
нанокристалах обох типів зменшується. До того ж ширина забороненої зони НК, які
були синтезовані у фотографічній желатині (тип II) має найбільшу величину для
всіх інтервалів процесу синтезу. Значення середніх радіусів нанокристалів CdS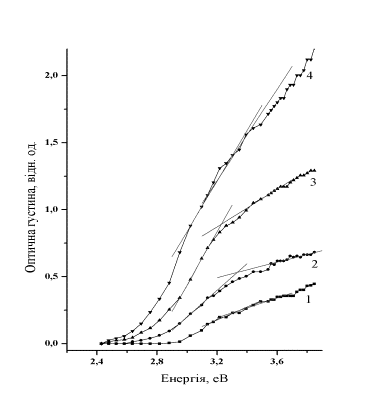
Рис.2. Спектри поглинання зразків
типу
II в залежності від часу синтезу, хвилини:
1 (1), 4 (2), 8 (3), 12 (4).
також суттєво
залежать як від часу синтезу, так і від типу желатини, а саме, при синтезі в
харчовій желатині формуються нанокристали більшого розміру, ніж в фотографічній
желатині. Характерно, що розмір нанокристалів, які отримані в фотографічній
желатині, змінюється менше в процесі синтезу ніж розмір нанокристалів, отриманих
в харчовій желатині. Нами було припущено, що однією із властивостей желатини,
яка виконує визначну роль у стабілізації розміру НК, є величина її в`язкості.
Виявилося, що для розчину 5% в`язкість фотографічної желатини на 23,5% більше,
ніж харчової, а саме: в`язкість харчової
– 3,238∙10-2 Пуаз, а фотографічної – 4∙10-2
Пуаз при температурі синтезу. Відмінність в величинах в`язкості желатин може
бути обумовлена її домішковим складом. Як уже визначалося вище, фотографічна
желатина містить менше домішок. Домішки, які проникають в молекулу желатини, ослаблюють
міцність окремих зв`язків в ланцюзі молекули, в результаті чого молекула
желатини розпадається на окремі ланцюжки і її в`язкість зменшується [8].
Таким чином, результати досліджень показали, що природний полімер - желатина є придатною речовиною для
отримання нанокристалів напівпровідникових сполук при низьких температурах.
Показано, що розміри нанокристалів, які отримані в 5% водньому розчині харчової
і фотографічної желатин змінюються, відповідно, в інтервалах 1,4-2,3 нм та
1,3-1,5 нм. Визначним фактором для стабілізації роміру нанокристалу є вязкість,
яка пов”зана з чистотою матеріалу.
Література
1. A. Henglein. J. Phys. Chem., V. 86 (1982), 2291-2299.
2. L. E. Brus. J. Chem. Phys., V. 79 (1983),
5566-5571.
3. L. E. Brus. J. Phys. Chem., 90 (1986), 2555-2560.
4. A. Mews, U. Banin, A. V. Kadavanich, A. P.
Alvisators, Ber.Bunsenges.
Phys. Chem., V.101 (1997), 1621-1625.
5. C. B. Murray, D. J. Noris, M. G.
Bawendi. J. Am. Chem. Soc., 115 (1993), 8706.
6. l. Spanhel, M. Haase, H.
Weller, A. Henglein. J. Am. Chem. Soc., V. 109 (1987), 5649-5655.
7. A. Eychmuller. J. Phys. Chem., B, V. 104 (2000), 6514-6528.
8. Миз К., Джеймс Т., Теория фотографического
процесса - Изд. «Химия», 1973. - С. 56-59.
9. В. М. Скобєєва, В. А. Сминтина, М. В. Малушин. Спосіб одержання наночастинок сульфіду кадмію. Патент № 29893, Бюл. № 2, 25.01.2008, Україна.
10. Madelung O., Martienssen,W.,
Eds; Landolt - Bornstein.
Numerical data and functional relationships in science and technology, Springer
- Verlag: Berlin, 1988, Volume III - 17b, pр.166 - 194.
11. Эфрос Ал.Л.. Эфрос А.Л. Межзонное поглощение света в
полупроводниковом шаре. – ФТП.1982. – Т.16, №7. - С.1209-1214.