1канаев А.Т.,
2Канаева З.К., 1Мырзаханова И.А.,
1Джамилова С.М., 1Бектемирова Г.Н.
1.Казахский Национальный
Педагогический университет имени Абая
2.Казхский Национальный Технический университет им К.Сатпаева
подбор окислителей и их концентрации для извлечение урана
Всего на территории Казахстана разведано 129
месторождений и рудопроявлений урана. Месторождения урана объединены в шесть
урановых провинций (Прибалхашская, Прикаспийская, Илийская,
Северо-Казахстанская, Сырдарьинская, Чу - Сарысуйская). Запасы и ресурсы шести
провинций составляют 1,69 млн. т урана. Из них около 1,2 млн. т пригодны для
добычи способом подземного выщелачивания.
Как известно, в процессе
выщелачивания в раствор переходит не только металл, но и многие другие
компоненты, поэтому развитию микроорганизмов могут препятствовать как высокая
концентрация ионов определенных элементов, так и компонентный состав
растворенных солей.
Выносливость диких штаммов Acid.ferrooxidans может быть
существенно повышена при культивировании их в лабораторных условиях с
постепенно возрастающими концентрациями ионов. В целях применения Acid.ferrooxidans в
гидрометаллургических процессах необходимо, чтобы они обладали повышенной
устойчивостью к содержанию различных компонентов в выщелачивающих растворах. [1]
В этом подразделе
исследований попытались выяснить роли окислителей на интенсификации процессов
извлечение урана и молибдена из руд в условиях сернокислотного выщелачивания.
Опыты
проводились на агитационной установке с рудой крупностью 0,055 мм, содержащих
0,210-0,245% урана и 0,030-0,035% молибдена. Плотность орошения составила 20-25% (Т:Ж=1:4). Время агитации составило
от 4 до 16 часов на качалке при 180 об/мин., температура 28оС.
Во
всех вариантах опыта концентрация H2SO4
находилась в пределах 15-20 г/л. в качестве окислителей были
использованы соли сернокислого железа Fe2(SO4)3, надсернокислый аммоний (NH4)2S2O8
и перманганата калия KMnO4.
В первом варианте
опыта (рисунок 1), где применяли в качестве окислителя Fe2(SO4)3 (1,16-5,8 г/л),
наблюдается следующая закономерность: с увеличением концентрации железа в
растворе, соответственно, повышается извлечение урана и молибдена. Максимальное
извлечение урана (68%) и молибдена (28,22%) в раствор было достигнуто при
концентрации железа 5,8 г/л. [2]
В последующем опыте
(рисунок 2) в качестве окислителя использовались соли надсернокислого аммония в
количестве от 2,5 г/л до 30,0 г/л. Установлено, что с повышением концентрации
окислителя (NH4)2
S2O8 поднимается степень
извлечения урана (95,2%) и молибдена (36,5 %).
Высокая степень
извлечения металлов связана с участием в процессе выщелачивания окислителя.
Так, в нашем предыдущем исследовании
при отсутствии окислителя железо извлекалось селективно и только в форме
двухвалентного. А при участии окислителей окисляется все железо, и при этом
дополнительно образуются окислители четырехвалентного урана.
Исследовано также
(рисунок 3 ) влияние различной концентрации перманганата калия (от 0,5 до 3,0
г/л) на извлечение урана. Выявлено, что
при концентрации KMnO4
от 1,5 до 3,0 г/л степень извлечения урана повысилась от 64,0 до 69,6%, а при отсутствии окислителя извлечено всего
13,7 % урана. [3]
В результате
выщелачивания урана из руды продолжительностью
70 суток установлено, что при концентрации 5 г/л серной кислоты в
раствор извлекалось 50,0
% урана, в варианте с 10 г/л серной
кислоты - 52,8 % урана, в опытах с 20 г/л серной кислоты - 58,0%. В контрольном
опыте извлечение урана составило 36,8 %.
С повышением концентрации серной кислоты заметно увеличивается её
расход.
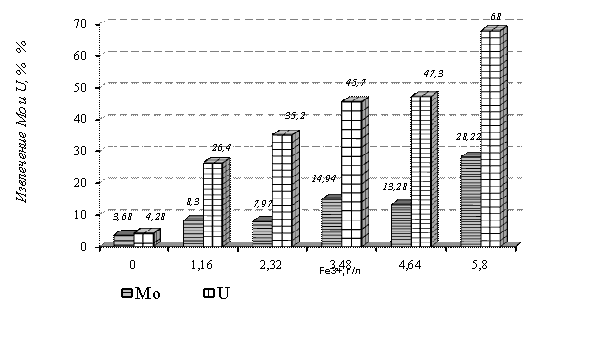
Рисунок 1 - Влияние концентрации окислителя Fe2(SO4)3 на извлечение урана
и молибдена из руд
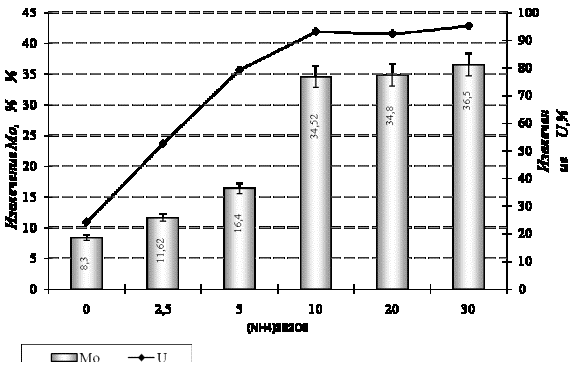
Рисунок 2 - Влияние концентрации окислителя (NH4)2S2O8 на степень извлечения урана
и молибдена из руды
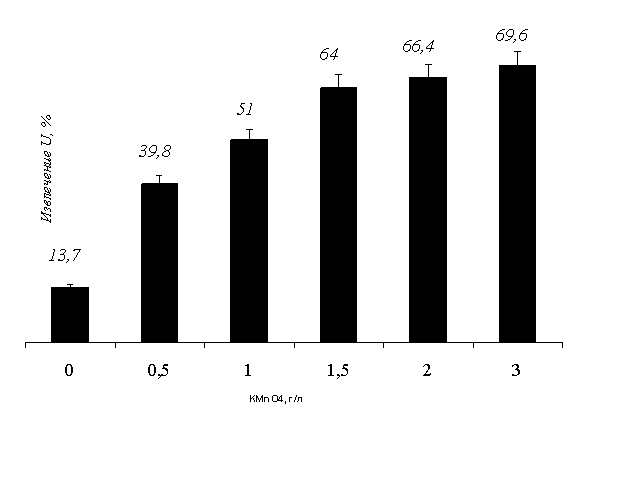
Рисунок 3 - Влияние окислителя KMnO4 на
извлечение урана из руд в кислой среде
Итак, при бактериально -химическом
выщелачивании отработанных руд штабеля №4 концентрация
серной кислоты в растворе не должна превышать 5-20 г/л, продолжительность
процесса выщелачивания - 40 суток. При таком установленном параметре мы можем
ощутимо сэкономить расход серной кислоты, которая в производственных условиях
кучного выщелачивания затрачивается в огромных количествах. [4]
Обследование рудной
массы на отработанных штабелях при определении химического состава руд и
соотношении четырех- и шестивалентного урана показали, что содержание металла в
руде остается еще на уровне товарного – 0,05%. На отработанных участках годами
происходили естественные окислительные процессы. За счет химического и
биологического окисления железа и серосодержащих минералов руда стала кислой и
доступной для повторного выщелачивания. Как показали результаты перколяционных
опытов с рудой штабеля №4, с использованием 0,51% растворов серной кислоты
можно извлечь до 60% урана. [5]
В ходе
промышленного испытания биотехнологического метода выщелачивания урана
на участке КВ РУ-1 СГХК получены
результаты.
С использованием биотехнологического
способа из отработанных и
бедно-товарных руд, уложенных в штабелях,
извлекался уран, за основу были
приняты выше исследованные направления кучного выщелачивания. Регламент технологических процессов был
установлен по рекомендации соискателя. Регулярно осуществлялось методическое
руководство и дистанционно
контролировалось ведение процессов.
До
настоящего времени микроорганизмы редкоземельных (уран, тантал и др.)
месторождений Казахстана практически мало изучены, поэтому наше внимание обращено к бактериальной
интенсификации процессов выщелачивания урана.
Из различных участков кучного выщелачивания (технологические растворы,
руда отработанных штабелей, растворы со всех испарительных карт) были выделены
железо и сероокисляющие бактерии Acid. ferrooxidans.
Установлено, что источником питания в энергетическом обмене для этих бактерий
являются восстановленные формы железа и серы, которые в руде встречаются в
основном в виде минерала пирита. Эти микроорганизмы в кислой среде интенсивно
окисляют пирит и другие железосодержащие минералы до трехвалентного железа -
сильного окислителя четырехвалентного урана и серной кислоты.
Литература:
1.
Камалов
М. Р. Роль микроорганизмов в выщелачивании металлов из руд Казахстана // Монография. _Алматы,1990г. –
С. 5-24.
2. Плюснин А.М., Гунин В.И. Самоорганизация зоны окисления сульфидных месторождений // Докл. АН СССР, 1998. - Т. 361, - № 5, - С. 675-678.
3. Ракчеев А.Д. Влияние химизма вмещающих пород на состав и
кислотно-основные свойства рудных минералов // Кислотно-основные свойства
химических элементов, минералов, горных пород и растворов. - Москва, 1982. - С.
91-115.
4. Яхонтова Л.К. Значение конституции сульфидов в процессе их
бактериального выщелачивания // Биотехнология металлов. Тр. междунар. семинара.
Центр междунар. проектов ГКНК. - Москва, 1985. - С. 222-33.
5.
Рыльникова М.В., Шадрунова И.В., Горбатова Е.А.
Геотехнологическая подготовка медных руд к обогащению // Экологические проблемы
и новые технологии комплексной переработки минерального сырья. Материалы
международного совещания «Плаксинские чтения-2002».-Москва, 2002.
- С. 42-43.