Н.Б. Егоров
Томский
политехнический университет
Синтез наноструктур Ag2S-Ag ПРИ ФОТОЛИЗЕ ВОДНЫХ
РАСТВОРОВ тиосульфата серебра
Известно, что ультрадисперсные
полупроводники могут использоваться как фотокатализаторы. Однако, не смотря на
большое количество исследований проводимых в этой области, проблема создания
фотокаталитических систем остается не решенной. Одним из подходов в решении
этой проблемы является получение полупроводниковых нанокристаллических
структур, имеющих участки, отличающиеся строением электронных уровней.
Получение подобных наноструктур – достаточно сложная задача и требует
многостадийного синтеза, состоящего в получении наночастиц с последующей
модификацией их поверхности [1].
Использование для получения наночастиц
фотохимического метода оправдано, уже тем, что благодаря простому регулированию
интенсивности потока квантов электромагнитного излучения, способных быстро и
эффективно вызывать реакции восстановления, можно легко осуществлять контроль
за количеством и размером образующихся наночастиц.
В качестве исходных соединений для
получения наночастиц металлов и халькогенидов фотохимическим методом можно
использовать водные растворы тиосульфатов тяжелых металлов, при облучении
которых УФ – излучением образуются металлы или сульфиды.
В данной работе показана возможность
одностадийного получения наноструктуры Ag2S-Ag при фотохимическом разложении водных растворов
комплексного тиосульфата серебра (КТС).
Состав комплексного соединения
соответствует формуле Na2(x-1)[Ag(S2O3)x], где количество лигандов х изменяется от двух до трех в зависимости от концентрации раствора
и от мольного соотношения ионов свинца и тиосульфат - ионов при синтезе
соединения [2].
Облучение водных растворов КТС
ультрафиолетовым излучением приводит к образованию твердофазных окрашенных
продуктов фотолиза. После облучения твердофазные продукты фотолиза отделяли
центрифугированием. Процедуру получения осадка повторяли многократно до
накопления продуктов фотолиза, достаточных для проведения рентгенофазового
анализа.
Облучение раствора КТС проводили в химическом
стакане диаметром 7,7 см, толщина слоя светочувствительного раствора при этом
составляла не меньше 1 см, что обеспечивало полное поглощение потока излучения.
В качестве источника излучения использовали ртутную лампу высокого давления с
нефильтрованным излучением. Облучение проводили в течение 30 мин.
Рентгенограмму осадка, полученного в
результате фотолиза, записывали на дифрактометре ДРОН – 3 со скоростью 4
град/мин (CuKa-излучение). Растворы светочувствительного соединения
получали смешением 0,1 М растворов нитрата серебра и тиосульфата натрия в
объемном соотношении 1:3. Результаты рентгенофазового анализа осадка
представлены на рис. 1.
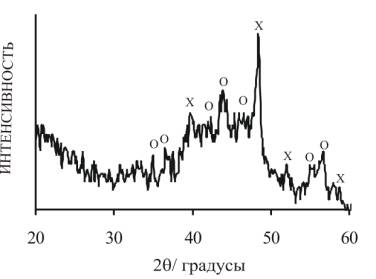
Рис. 1. Рентгенограмма осадка, полученного
при фотолизе водных растворов КТС. Крестиками обозначены рефлексы, относящиеся
к серебру. Кружками – к сульфиду серебра.
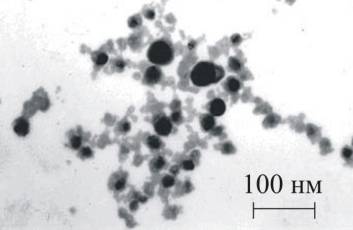
Рис. 2. Частицы,
образующиеся в течение 5 мин облучения раствора комплексного тиосульфата
серебра
Проведенные рентгенографические
исследования показали, что полученный в результате фотолиза осадок содержит
отражения, включающие основные рефлексы сульфида серебра и металлического
серебра. Образующийся сульфид серебра имеет структуру акантита.
Размеры зерен сульфида серебра и
металлического серебра, определенные по результатам измерения областей
когерентного рассеяния, составляют в среднем для сульфида серебра 25 нм и для
серебра 200 нм.
Данные
рентгенофазового анализа подтверждаются результатами электронной микроскопии.
Образующиеся в процессе фотолиза частицы серебра имеют наноразмер (рис. 2).
Электронномикроскопические исследования проводились на электронном микроскопе JEM-100CXII (JEOL, Japan) с
использованием сеток с формваровой пленкой-подложкой.
Литература
[1] Khairutdinov R.
// Russ. Chem. Rev. 1998.
v. 67, № 2. p. 125-139.
[2] Тудоряну К.И., Мигаль П.К., Долгиер В.Т. // Журн. неорг. химии. 1982. Т.27. Вып. 6. С. 1450-1454.