Н.Б. Егоров
Томский
политехнический университет
Фотолиз водных растворов
тиосульфата кадмия
Облучение водных растворов тиосульфатов
тяжелых металлов (Pb, Cd, Ag) УФ-излучением
приводит к их разложению с образованием различных твердофазных продуктов. В настоящей работе исследованы продукты фотолиза водных
растворов тиосульфата кадмия (ТК).
В качестве источника УФ – излучения
использовали ртутно – кварцевую лампу высокого давления с нефильтрованным
излучением.
ИК-спектры твердофазных продуктов фотолиза
снимали на ИК-Фурье спектрометре Nicolet 5700 в диапозоне 400-4000 см-1.
Образцы готовили в виде таблеток с бромидом калия.
Рентгенограммы записывали на дифрактометре
Shimadzu XRD 6000 CuKa -
излучение (l = 0,1936 нм). В данном
случае концентрации исходных растворов CdCl2 и Na2S2O3
составляли 0,1 моль×л-1. Образующийся при фотолизе твердые
продукты отделяли центрифугированием. Процедуру их получения повторяли
многократно до накопления количества, достаточного для проведения анализа.
Содержание кадмия в полученных продуктах
определяли комплексонометрическим титрованием трилоном Б. В качестве индикатора
использовали смесь эриохрома черного Т с хлоридом натрия. Для определения серы
полученные при фотолизе продукты обрабатывали царской водкой. При этом вся
содержащаяся в осадках сера переходила в сульфатную серу, содержание которой
определяли гравиметрическим методом после осаждения сульфат – ионов раствором
хлорида бария.
При облучении водных растворов ТК УФ-излучением
раствор окрашивается в коричнево-зеленый цвет.
Химический анализ осадка, полученного при
фотолизе, показал, что мольное соотношение Cd:S в нем
непостоянное и зависит от способа и длительности его отмывки. Исследование
полученного осадка методом ИК-спектроскопии показало, что в ИК-спектре
содержатся полосы поглощения при 1149 см-1, 1004 см-1 и
628 см-1, характерные для тиосульфат-иона [7] и полосы поглощения
при 3469 см-1 и 1622 см-1, характерные для молекул воды.
Многократная промывка водой и подкисленной водой до pH=2 не приводит к удалению тиосульфат-ионов из продукта
фотолиза (рис.1, кривая 1).
Удалить примеси из осадка, полученного при
фотолизе, возможно только при длительном нагревании его в воде или в 0.1 н. HCl (рис.1, кривая 2). При этом окраска продукта фотолиза
переходит из коричнево-зеленой в ярко желтую.
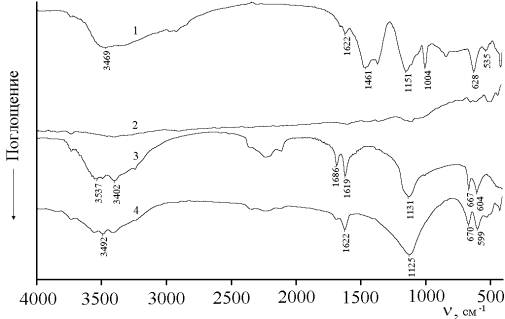
Рис. 1 ИК-спектры: 1-продукт фотолиза ТК;
2- продукт фотолиза ТК, отмытый при нагревании в 0,1 н. HCl; 3-осадок, полученный при добавлении к фотолизованному
раствору ТК раствора CaCl2; 4-сульфат кальция
Как показали данные рентгенофазового
анализа (табл. 1), продукт фотолиза ТК, прошедший отмывку при нагревании в 0.1
н. HCl, содержит набор отражений, включающих основные
рефлексы CdS.
Химический анализ отмытого от
тиосульфат-ионов осадка показал, что мольное соотношение Cd:S в нем
составляет 1:1. Таким образом, следует сделать вывод, что при фотолизе водных
растворов ТК основу твердофазного продукта составляет CdS.
Таблица 1. Данные РФА осадка, полученного
при фотолизе водных растворов ТК
|
CdS |
Продукт фотолиза |
||
|
2q |
I, % |
2q |
I, % |
|
26,514 |
100 |
26,76 |
100 |
|
30,709 |
22 |
30,28 |
63 |
|
43,983 |
47 |
43,88 |
41 |
|
52,094 |
35 |
52,40 |
26 |
|
54,598 |
5 |
55,40 |
17 |
На рис. 1 (кривая 3) представлен ИК-спектр
вещества, полученного после добавления раствора CaCl2 к
фотолизованному раствору ТК. Предварительно CdS был отделен центрифугированием. Для сопоставления на
рисунке представлен (кривая 4) ИК-спектр CaSO4,
полученного при добавлении раствора CaCl2 к раствору Na2SO4. Как
видно из рисунка ИК-спектр вещества, полученного из фотолизованного раствора ТК,
достаточно точно повторяет ИК-спектр CaSO4. Это позволяет сделать вывод о том, что вторым
продуктом фотолиза ТК являются сульфат-ионы SO42-.
Исходные растворы ТК имеют слабокислую или
нейтральную реакцию (в зависимости от содержания тиосульфат-ионов). В процессе
фотолиза в растворах происходит накопление ионов водорода.
Обработка твердофазных продуктов фотолиза
ТК н-гексаном не привела к обнаружению элементной серы.
Таким образом, конечными продуктами
фотолиза водных растворов ТК являются CdS, SO42- и H+. Полученные результаты дают основания предложить
суммарное уравнение процессов фотолиза ТК:
[Cd(S2O3)x]2(x-1)- + H2O
+ hn ® CdS + SO42-
+ (x-1)S2O32- + 2H+.