к.т.н., Кузенко Ю.Н., Лебеденко Ю.П.,
Михайлова Е.Н., д.т.н., проф. Панасенко В.А.
Государственное
учреждение «Государственный научно-исследовательский и проектный институт
основной химии» (ГУ «НИОХИМ»), Украина, г. Харьков
ТЕХНОЛОГИЯ ОЧИСТКИ ТВЕРДОГО ХЛОРИДА НАТРИЯ ДЛЯ ПРОИЗВОДСТВА СОДЫ
Аммиачный способ получения
кальцинированной соды, на долю которого приходится почти 70 % мирового ее
производства имеет два существенных недостатка: низкая степень использования
натрия из хлорида натрия (от 72 % до 76 %) и, как следствие большой объем
жидких отходов (от 9 до 10 м3 на 1 т соды).
Эти недостатки устраняются при получении
соды циклическим способом [1, 2]. Особенностью этого способа является
использования твердого хлорида натрия. Природный кристаллический хлорид натрия
практически всегда содержит растворимые и нерастворимые примеси (НП), которые
необходимо удалить без растворения исходного сырья при подготовке к его
использованию в производстве соды циклическим методом.
Предлагаемая технология очистки природного
кристаллического хлорида натрия разработана на примере галитовых отходов
производства хлорида калия из сильвинита галургическим способом. Преимуществом
технологии является ее применяемость для очистки твердого хлорида натрия
озерного и морского происхождения. Проба отходов имела следующий химический
состав в % мас.: NaC1 – 85,35; KC1 – 2,47; (MgC12 + CaC12)
– 0,49; железо в пересчете на FeC13 – 0,026; нерастворимые примеси,
включая кристаллы CaSO4 – 3,53; H2O – 8,13.
Разработанная технология очистки твердого
хлорида натрия от примесей поясняется схемой (рисунок).
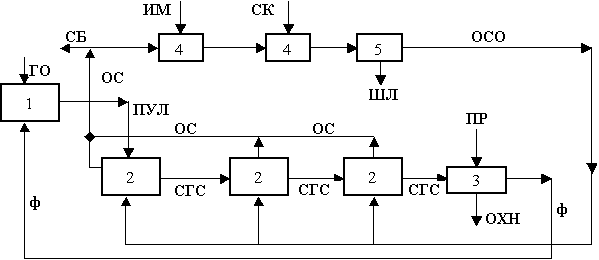

Рисунок. Структурная аппаратурно-технологическая схема
установки очистки галитовых отходов
Обозначения и используемые сокращения: 1 –
репульпатор; 2 – репульпатор-классификатор; 3 – центрифуга; 4 – реактор; 5 –
фильтр; ГО – галитовые отходы; ШЛ – шлам; ОХН – очищенный NaCl (Влажность – 5%,
мас.); ИМ – известковое молоко; СК – сода кальцинированная; ПР – вода на
промывку кристаллов NaCl; СБ – сброс рассола; ОС – осветленная суспензия; СГС –
сгущенная суспензия; ПУЛ – пульпа; ОСО – осветленная суспензия очищенная; ф – фугат.
На схеме установки имеются два циклических
потока. Первый цикл: – репульпатор 1
– каскад репульпаторов – классификаторов 2 – центрифуга 3 – репульпатор 1. Второй цикл: – реакторы 4 – фильтр 5 –
каскад репульпаторов – классификаторов 2. По верхней ветви первого циклического
потока течет сгущенная суспензия (СГС) с кристаллами хлорида натрия, а по
нижней ветви – фугат (Ф) из центрифуги 3. По верхней ветви второго циклического
потока течет осветленная суспензия (ОС) из каскада репульпаторов –
классификаторов 2 на стадию очистки от растворимых и (НП), а по нижней ветви –
осветленная суспензия (ОСО) (фильтрат), очищенная от растворимых и НП. Из ГО необходимо
удалить следующие примеси:
–
НП, включая кристаллы кальция сульфата;
–
хлориды магния и кальция;
–
сульфат кальция;
–
хлорид калия.
НП содержатся в ГО в большей части своей
массы в тонкодисперсном состоянии, как это обычно имеет место при производстве
хлорида калия галургическим методом. Эту часть НП можно удалить путем каскадной
гидроклассификации ГО в насыщенном по хлориду натрия рассоле. Крупные фракции
НП, случайно попавшие в ГО, пройдут через стадию очистки ГО и, в конечном
итоге, будут выведены из содового производства на стадии фугования суспензии с
кристаллами хлорида аммония. Реагентная содо-щелочная очистка репульпирующего
рассола от ионов магния, кальция, включающая подачу в рассол интенсифицирующей
добавки – хлорида кальция в виде дистиллерной жидкости, отхода содового
производства [3] происходит по химическим реакциям:
Ca(OH)2р +
MgC12р = Mg(OH)2т + CaC12
Na2CO3
+ CaSO4 = CaCO3т + Na2SO4
3Ca(OH)2 +2FeC13 = Fe(OH)3т + 3CaC12
Na2CO3
+ CaC12 = CaCO3т + 2NaC1.
Ионы магния и железа удаляются из
репульпирующего рассола с помощью известкового молока с образованием
практически нерастворимых тонкодисперсных Mg(OH)2 и Fe(OH)3.
Ионы кальция удаляются из репульпирующего рассола с помощью Na2CO3
(соды) с образованием практически нерастворимого тонкодисперсного CaCO3
(мела). Смесь тонкодисперсных «природных» и «синтетических» НП удаляется из
осветленной суспензии, выведенной из гидроклассификаторов 2, в фильтре 5.
Кристаллический KC1 при достаточно длительном контакте с репульпирующим
рассолом растворится в нем. Процесс растворения кристаллов KC1 будет
продолжаться до тех пор, пока рассол не будет насыщен одновременно по KC1 и
NaC1 (точка двойного насыщения). С увеличением температуры рассола точка
двойного насыщения будет смещаться в область повышенных концентраций KC1 и
пониженных концентраций NaC1. Примесь KC1 в ГО удаляется в описываемой
технологии очистки путем сброса («сдувки») сброса рассола части осветленной
суспензии, выведенной из гидроклассификаторов 2, на производство KC1.
Расчеты показывают, что подбором
температуры репульпирующего рассола можно обеспечить баланс прихода KC1 с ГО и
его расходом с потоком «сдувки» СБ. Этими же расчетами установлено, что для
вышеприведенного состава ГО при температуре процесса очистки ГО от примесей 35 °С.
одновременно достигается баланс прихода и расхода по KC1 и воде.
Вода ПР вводится в установку при промывке
осадка в центрифуге 3 и выводится с промытым осадком кристаллов NaC1 ОХН и с
потоком «сдувки» СБ. НП, поступающие в циклическое содовое производство с
осадком NaC1, выводятся из содового производства с осадками NaHCO3
(около 80 %) и NH4C1 (около 20 %).
Очистка ГО от НП должна обеспечивать
получение товарной соды, удовлетворяющей требованиям ГОСТ 5100-85 по массовой
доле НП не более 0,03 %. Для выполнения этого требования массовая доля НП в
сухом осадке NaHCO3, подаваемом на стадию кальцинации, должна быть
не более 0,03 / 1,585 = 0,0189 %, где 1,585 – коэффициент пересчета соды в
бикарбонат натрия.
Рассмотрим процесс очистки суспензии ГО от
НП в одной ступени каскада репульпаторов – классификаторов 2.
В ступень поступает:
– поток суспензии ГО, в котором доля жидкой фазы равна
Q, а содержание в ней НП равно Со;
– поток ОСО (см. рисунок) q, не содержащий НП.
Из ступени выходит:
– поток суспензии ГО, в котором доля жидкой фазы равна
Q, а содержание в ней НП равно С1;
– поток ОСО q, в котором содержание НП равно С1.
Степень очистки суспензии ГО от НП в ступени по
определению равна:
σ = (Со
– С1) / Со. (1)
Отсюда
С1 = Со (1 –
σ). (2)
Уравнение материального баланса ступени каскада по НП
Q * Со = Q *
С1 + q* С1. (3)
Из этого уравнения находим
С1 = Со*[Q/(Q + q)]. (4)
Из сравнения уравнений (2) и (4) находим
σ = q /(Q + q). (5)
Последовательно применяя уравнение (4) к
ступеням с номером 1, 2, 3 и т.д. находим, что в жидкой фазе суспензии в
ступени очистки с номером n концентрация НП будет равна:
Сn=Со*(Q/(Q+q))ⁿ. (6)
Испытания опытных репульпаторов –
классификаторов показало, что величина комплекса Q / (Q+q) может варьироваться
в интервале от 0,4 до 0,8.
Расчеты показывают, что в очищенном NaC1,
подаваемом на производство соды циклическим методом, массовая доля НП должна
быть не более 0,027%.
Таблица
Табуляция функции Сn / Со = [Q/(Q+q)]ⁿ
|
Q / (Q+q) |
Номер ступени очистки (n) |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
0,8 |
0,8 |
0,64 |
0,51 |
0,41 |
0,33 |
0,26 |
|
0,7 |
0,7 |
0,49 |
0,34 |
0,24 |
0,17 |
0,12 |
|
0,6 |
0,6 |
0,36 |
0,22 |
0,13 |
0,08 |
0,05 |
|
0,5 |
0,5 |
0,25 |
0,125 |
0,062 |
0,031 |
0,016 |
|
0,4 |
0,4 |
0,16 |
0,064 |
0,026 |
0,010 |
0,004 |
Только в этом случае будет обеспечиваться
массовая доля НП в соде не более 0,03% и НП не будут накапливаться в
циркулирующем потоке рассола. Если массовое соотношение твердой (Т) и жидкой
фаз (Ж) в суспензии в ступенях очистки равно 1 : 3 и такая суспензия (условно,
так как это не экономично) без дополнительного сгущения разделяется в центрифуге,
то концентрации НП в жидкой фазе суспензии должна быть равна 0,027 / 3 = 0,009
% (при фуговании суспензии НП из жидкой фазы переходит в осадок). При
использовании ГО вышеприведенного состава и массовой доле НП в нем 3,53 % в
жидкой фазе пульпы с Т : Ж = 1 : 3, поступающей в первую ступень очистки,
массовая доля НП будет равна 1,2 %. Установка очистки должна обеспечить
получение величины соотношения в последней ступени очистки Сn / Со = 0,009 /
1,2 = 0,0075.
Из таблицы видно, что при величине
комплекса Q / (Q+q) = 0,4 величина соотношения Сn / Со = 0,0075 будет надежно
достигается в установке, содержащей шесть ступеней очистки.
Если суспензию перед подачей в центрифугу
сгустить до обычной величины Т: Ж = 1 : 1,5, то массовую долю НП в жидкой фазе
суспензии можно повысить до величины 0,027 / 1,5 = 0,018 %, соотношение Сn / Со
повысить до величины 0,018 / 1,2 = 0,015, а число ступеней очистки в установке
уменьшить до четырех.
Выводы:
1. Установлены закономерности влияния
массового соотношение твердой и жидкой фаз в суспензии твердого хлорида натрия
на число ступеней очистки от примесей.
2. Показано, что для обеспечения массовой
доли нерастворимых примесей в товарной кальцинированной соде не более 0,03 %
можно надежно достигнуть в установке содержащей шесть ступеней очистки. Если
суспензию перед подачей в центрифугу сгустить до величины Т : Ж = 1 : 1,5, то
массовую долю нерастворимых примесей в жидкой фазе суспензии можно повысить до
величины 0,018 %, а число ступеней очистки в установке уменьшить до четырех.
3. Поскольку осадок хлорида натрия в
центрифуге перед выгрузкой подвергается промывке чистой водой, то можно с
уверенностью утверждать, что примеси MgCl2, CaCl2 и FeCl3
в выгруженном осадке твердого хлорида натрия будут практически отсутствовать.
Литература:
1. Микулин Г.И. Физико-химическое равновесие в системе NaCl + NH3 + CО2 + Н2О
→ NaHCO3 + NH4C1
при карбонизации аммиачного
рассола / Г.И. Микулин. – Харьков,
НИОХИМ, 1961. – Труды, Т. 63. – С.
53 – 82.
2. Кузенко Ю.Н. Создание безотходной
технологии производства соды кальцинированной [Текст] / Ю.Н. Кузенко // IV
Українська науково-дослідна конференція з технології неорганічних речовин: Тези
доповідей (14 – 16 жовтня 2008 р. м. Дніпродзержинськ).
3. Пат. 97844 UA, МКИ C01D7/18, C01D3/04,
C01D3/06. Спосіб реагентного очищення сирого розсолу від іонів магнію і кальцію
/ Ібрагімов А.Т., Сабітов А.Р., Фролов О.В., Кузенко Ю.М., Молчанов В.І.,
Малакей З.А., Васерман Л.З. Власник: Державний науково-дослідний і проектний
інститут основної хімії (НІОХІМ): Акціонерное общєство «Алюміній Казахстана».
Дата подання заявки 21.12.2009, Бюл. № 12; Дата публікації 26.03.2012. Бюл. №
6.