Артамонова
Г.Б., Шляховенко В.О.
Антиметастатична
дія глікопептидної протипухлинної вакцини.
Інститут експериментальної патології, онкології та радіобіології ім. Р.Є.Кавецького НАН
України.
Вступ. Аналіз сучасної наукової літератури
переконливо свідчить, що вакцинотерапія пухлин вже сформувалася як самостійний
досить перспективний напрям імунотерапевтичного лікування хворих на злоякісні
новоутворення [1-4]. Аутологині протипухлинні вакцини (ПВ), призначені для
пригнічення росту вже виявленої пухлини чи попередження розвитку рецидивів і
виникнення метастазів [5-7].
Однією з
найбільш важливих проблем, пов’язаних із застосуванням ПВ, є недостатня
ефективність їх дії, обумовлена низькою імуногенністю антигенів пухлинних
клітин [8], а також появою і накопиченням в організмі онкологічного хворого
низки порушень регуляторних і ефекторних ланок системи імунобіологічного
нагляду [8-10]. Однією з успішних стратегій підвищення ефективності
вакцинотерапії пухлин вбачається поєднане застосування разом з ПВ імунотропних
речовин природного та синтетичного походження – так званих ад`ювантів (Ад) [11,
12].
Серед
імунотропних речовин природного походження особливе місце займає група
полісахаридів, виділених з вищих грибів, що вже тривалий час широко
застосовуються з лікувальною метою у східній медицині [13, 14], а також здатні
потенціювати дію та знижувати вияв побічних ефектів хіміопроменевої терапії у
онкологічних хворих [15-17].
Тому, метою нашого дослідження було вивчити
антиметастатичну ефективність ПВ на експериментальній моделі пухлинного росту
карциномі легені Льюїс (CLL) в дозах 5 тис
та 100 тис ЕПК/тв. окремо та в поєднанні імуномодулятором,
полісахаридною фракцією, виділеною з плодового тіла гриба L. Еdodes (ПСФLE),
в профілактичному режимі.
Методи та матеріали.
Для отримання модельних систем пухлинного росту ПК
трансплантували у м`язи гомілки мишей лінії C57Bl/6. Епідермоїдну метастазуючу
карциному легені Льюїс трансплантували шляхом введення 400 тис. живих ПК у
м`язи гомілки [18]. Методом випадкового відбору миші попередньо були розділені
на дослідні і контрольні групи. Введення ГПВ окремо чи поєднано з ПСФLE здійснювали
у профілактичному та терапевтичному режимах згідно схем, наведених на рис 1, 2,
3 та 4. Тварини з контрольних груп аналогічно отримували ін`єкції
фізіологічного розчину хлориду натрію.
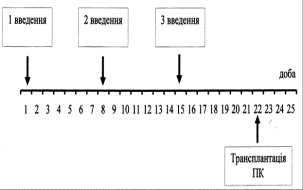 Рис 1. Схема 1 профілактичного введення досліджуваних субстанцій
Рис 1. Схема 1 профілактичного введення досліджуваних субстанцій
 Примітки: 1. шлях введення – п/ш; 2. кількість введень – 3;
3. разова доза ГПВ – 100 тис. ЕПК; 4. разова доза ПСФLE –
5,0 мг/кг маси тіла тварини.
Примітки: 1. шлях введення – п/ш; 2. кількість введень – 3;
3. разова доза ГПВ – 100 тис. ЕПК; 4. разова доза ПСФLE –
5,0 мг/кг маси тіла тварини.
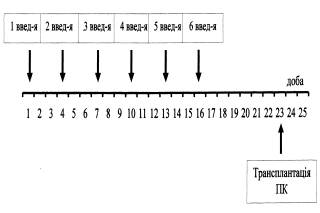
Рис. 2. Схема 2 профілактичного введення
досліджуваних субстанцій
Примітки: 1. шлях введення – п/ш; 2. кількість введень – 6;
3. разова доза ГПВ – 5 тис. ЕПК; 4. разова доза ПСФLE –
0,25 мг/кг маси тіла тварини.
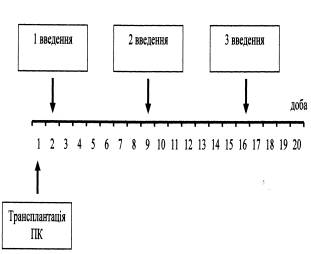 Рис. 3.
Схема 1 терапевтичного введення досліджуваних субстанцій
Рис. 3.
Схема 1 терапевтичного введення досліджуваних субстанцій
Примітки: 1. шлях введення – п/ш; 2. кількість введень – 3; 3. разова доза ГПВ –
100 тис. ЕПК; 4. разова доза ПСФLE – 5,0 мг/кг маси тіла тварини.
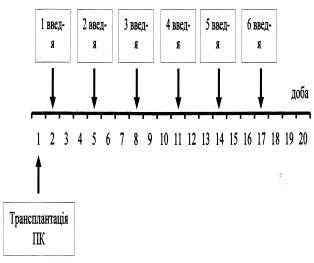 Рис.5. Схема 2 терапевтичного введення досліджуваних субстанцій
Рис.5. Схема 2 терапевтичного введення досліджуваних субстанцій
Примітки: 1. шлях введення – п/ш; 2. кількість введень – 6; 3. разова доза ГПВ – 5
тис. ЕПК; 4. разова доза ПСФLE – 0,25 мг/кг маси тіла.
Для
оцінки антиметастатичної дії досліджуваних протипухлинних засобів мишей
забивали на 28-му добу після трансплантації ПК, вилучали легені та досліджували
їх на предмет метастатичного ураження. Ефективність антиметастатичної дії
оцінювали з використанням показників, що характеризують процес метастазування,
зокрема за частотою та інтенсивністю метастазування, а також швидкістю росту
метастазів. Для цього враховували кількість тварин у групі з
ознаками метастатичного ураження легень, рахували середню кількість і
розраховували середній загальний об`єм метастазів у тварин із групи.
Результати, наведені у табл. 1, характеризують вплив профілактичного
застосування ГПВ окремо чи поєднано з ПСФLE на метастазування у
мишей з трансплантованою карциномою легені Льюїс. За таких умов введення
досліджуваних протипухлинних засобів найбільш виражена антиметастатична
активність була відмічена у мишей, які отримували ін`єкції ПВ у дозі
5 тис. ЕПК. У цій групі частота виникнення первинної пухлини
становила 90,0 % (у 9 із 10 тварин), а частота метастазування – лише
80,0 % (у 8 із 10 тварин). При цьому середня кількість метастазів досягала
7,6±2,3 у порівнянні з 13,4±5,2 у контролі (Р<0,05) та 14,2±2,7 при введенні
100 тис. ЕПК (Р<0,05), а об`єм метастазів наближався лише до
80,4±7,9 мм3 проти 101,8±11,6 (Р<0,01) та 107,6±13,1 мм3
(Р<0,01) відповідно. Слід зазначити, що згадані вище значення
показників, які характеризують процес метастазування, були достовірно нижчими у
мишей із цієї групи, якщо порівнювати з тваринами, які отримували ГПВ разом із
ПСФLE чи ПСФLE окремо.
Таблиця 1
Вплив профілактичного застосування ГПВ окремо чи поєднано з ПСФLE
на метастазування у мишей з трансплантованою епідермоїдною карциномою легені
Льюїс
Група n Частота метастазування, % Середня кількість метастазів(1) Середній об`єм метастазів, мм3(1) Контроль 8 100,0 13,4±5,2 101,8±11,6 ГПВ100 10 90,0 14,2±2,7 107,6±13,1 ГПВ5 10 80,0 7,6±2,3*/## 80,4±7,9**/##/аа/bb ПСФLE5,0 8 75,0 9,1±3,0 97,2±11,6 ПСФLE0,25 8 62,5 8,0±4,5* 112,1±8,9 ГПВ100
+ ПСФLE5,0 10 80,0 8,7±2,6# 99,3±12,7с ГПВ5
+ ПСФLE0,25 10 90,0 11,1±4,4 116,0±10,1
Примітки: 1. (1)При обчисленні середньої
кількості та середнього об`єму метастазів
не враховували тварин, у яких
візуально не було виявлено ознак метастатичного ураження легенів; 2.
ГПВ100 та ГПВ5 – ГПВ, введена у дозі 100 і
5 тис. ЕПК відповідно; 3. ПСФLE5,0 та ПСФLE0,25 –
ПСФLE, введена у дозі 5,0 та 0,25 мг/кг маси тіла тварини
відповідно; 4. *Р<0,05 та **Р<0,01 порівняно з
контролем; 5. #Р<0,05 та ##Р<0,01 порівняно із
застосуванням ГПВ100; 6. aaP<0,01 порівняно із
застосуванням ПСФLE0,25; 7. bbР<0,01 порівняно із
застосуванням ГПВ5 + ПСФLE0,25; 8. сР<0,05
порівняно із застосуванням ГПВ5 + ПСФLE0,25.
У всіх інших групах тварин, у
переважній більшості випадків, спостерігалася лише тенденція до вияву
антиметастатичної активності, оскільки всі відмічені зміни досліджуваних
показників не виявляли статистично значимої різниці у порівнянні з контрольними
значеннями, за винятком статистично значимого зменшення кількості метастазів
під впливом введення 0,25 мг ПСФLE / кг маси
тіла тварини до 8,0±4,5 (Р<0,05); при цьому показник частоти метастазування
становив 62,5 % (5 із 8), проти 100,0 % (8 із 8 тварин)
у контролі, тоді як ознак розвитку первинної
пухлини не було виявлено лише у 87,5 % (1 із 8) тварин (табл. 1).
Як свідчать дані з табл. 2, терапевтичне застосування ГПВ
відображалося на частоті метастазування у мишей з трансплантованою
епідермоїдною карциномою легені Льюїс. Зокрема при введенні
5 тис. ЕПК метастатичне ураження спостерігали лише у 66,7 % (6 із 9) тварин, тоді як у контролі – у 85,7 % (6 із 7)
мишей.
Однак, терапевтичне застосування ГПВ окремо чи поєднано з
ПСФLE у тварин із трансплантованою епідермоїдною карциномою легені
Льюїс у жодному з випадків статистично достовірно не вплинуло на кількість
метастазів, виявлених у легенях мишей (табл. 2). Хоча у групах тварин,
яким вводили ГПВ у дозі 5 тис. ЕПК чи 5,0 мг ПСФLE / кг
маси тіла тварини спостерігалася тенденція до вияву пригнічуючого впливу
досліджуваних субстанцій на процес розповсюдження метастазів.
Слід зазначити,
що хоча поєднане застосування ГПВ із ПСФLE не вплинуло на поширення
метастазів, оскільки не призводило до достовірно значимого зменшення їх
кількості у легенях, проте значно відобразилося на гальмуванні росту вогнищ
метастатичного ураження, про що свідчать знижені значення загального об`єму
метастатичних вузлів до 87,5±19,2 (Р<0,01) і 98,7±29,9 мм3
(Р<0,01) при введенні ГПВ100+ПСФLE5,0 чи ГПВ5+ПСФLE0,25
відповідно у порівнянні з контролем – 145,2±21,7 мм3
(табл. 2).
Таблиця 2
|
Група |
n |
Частота
метастазування, % |
Середня кількість
метастазів(1) |
Середній об`єм метастазів,
мм3(1) |
|
Контроль |
7 |
85,7 |
16,0±5,8 |
145,2±21,7 |
|
ГПВ100 |
9 |
85,7 |
13,4±4,0 |
120,2±17,9 |
|
ГПВ5 |
9 |
66,7 |
10,1±3,5 |
115,8±11,6 |
|
ПСФLE5,0 |
7 |
71,4 |
10,4±4,8 |
101,3±15,7** |
|
ПСФLE0,25 |
7 |
100,0 |
15,5±5,0 |
129,0±25,4 |
|
ГПВ100 + ПСФLE5,0 |
10 |
70,0 |
13,7±3,6 |
87,5±19,2**/# |
|
ГПВ5 + ПСФLE0,25 |
10 |
100,0 |
15,0±6,1 |
98,7±29,9**/а |
Вплив
терапевтичного застосування ГПВ окремо чи поєднано з ПСФLE на
метастазування у мишей з трансплантованою епідермоїдною карциномою легені Льюїс
Примітки: 1. (1)При
обчисленні середньої кількості та середнього об`єму метастазів не враховували
тварин, у яких візуально не було виявлено ознак метастатичного ураження легенів;
2. ГПВ100
та ГПВ5 – ГПВ, введена у дозі 100 і 5 тис. ЕПК відповідно;
3. ПСФLE5,0 та ПСФLE0,25 – ПСФLE, введена у
дозі 5,0 та 0,25 мг/кг маси тіла тварини відповідно; 4. **Р<0,01
порівняно з контролем; 5. #Р<0,05 порівняно із застосуванням ГПВ100;
6. aP<0,05 порівняно із
застосуванням ПСФLE0,25.
Висновок. ПВ виявляє
антиметастатичну активність, але через недостатню її імуногенність доцільно
разом з нею використовувати імуномодулятор. Полісахарид, виділений з плодового
тіла L. edodes, виявляє
антиметастатичну активність і може бути використаний у якості ад’юванта у
поєднанні з глікопептидної протипухлинною вакциною.
Література.
1. Aurisicchio L,
Ciliberto G. Patented cancer vaccines: the promising leads. Expert Opin Ther
Pat. 2010 May;20(5):647-60.
2. Cebon J.
Cancer vaccines: Where are we going? Asia Pac J Clin Oncol. 2010 Mar;6 Suppl
1:S9-15.
3.
Itoh K, Yamada A, Mine
T, Noguchi M. Recent advances in cancer vaccines: an overview. Jpn J Clin
Oncol. 2009 Feb;39(2):73-80.
4.
Srivastava PK. Therapeutic cancer
vaccines. Curr Opin Immunol 2006; 18 (2): 201–5
5.
Doyle K, Beer S, Vorhies P. The ongoing hopes and
challenges of cancer. Part 1. Oncol Business Rev, Jan 2010: 26–30.
6.Pijpers
F, Faint R, Saini N. Therapeutic cancer vaccines. Nat Rev Drug Discov. 2005; 4(8):623-4.
7.Dalgleish
AG, Whelan MA. Cancer vaccines as a therapeutic modality: the long trek.
Cancer Immunol Immunother 2006; 55 (8): 1025–32.
8.Бережная Н.М., Чехун В.Ф. Иммунология
злокачественного роста. Киев: Наукова думка, 2005. – 791 с.
9. Rabinovich
GA, Gabrilovich D, Sotomayor EM. Immunosuppressive strategies that are mediated
by tumor cells. Annu Rev Immunol. 2007;25:267-96.
10. Marigo I, Dolcetti L,
Serafini P, Zanovello P, Bronte V. Tumor-induced tolerance and immune
suppression by myeloid derived suppressor cells. Immunol Rev. 2008
Apr;222:162-79.
11. Higgins JP, Bernstein
MB, Hodge JW. Enhancing immune responses to tumor-associated antigens. Cancer
Biol Ther. 2009 Aug;8(15):1440-9. Epub 2009 Aug 1.
12. Dubensky TW
Jr, Reed SG. Adjuvants for cancer vaccines. Semin
Immunol. 2010; 22(3):155-61.
13. Daba A.S.,
Ezeronye O.U. Anti-cancer effect of polysaccharides isolated from higher
basidiomycetes mushrooms. Afr J Biotechnol 2003. – Vol. 2, № 12. – P.
672-678.
14. Borchers AT,
Krishnamurthy A, Keen CL, Meyers FJ, Gershwin ME. The
immunobiology of mushrooms. Exp Biol Med (Maywood). 2008; 233(3):259-76.
15. Fujimoto S, Furue H, Kimura
T, Kondo T, Orita K, Taguchi T, et al. Clinical
outcome of postoperative adjuvant immunochemotherapy with sizofiran for patients with resectable
gastric cancer—a randomised controlled
study. Eur J Cancer 1991;27:1114–8.
16. Hayakawa K, Mitsuhashi N, Saito Y, Takahashi M, Katano
S, Shiojima K, Furuta M, Niibe H. Effect of krestin (PSK) as adjuvant treatment
on the prognosis after radical radiotherapy in patients with non-small cell
lung cancer. Anticancer Res. 1993 Sep-Oct;13(5C):1815-20.
17. Smith
J.E., Rowan N.J., Sullivan R. Medicinal
mushrooms: their therapeutic properties and current medical usage with special
emphasis on cancer treatments.Cancer Research UK.,
2002. - 256 p.
18. Трещалина Е.М. Противоопухолевая активность веществ
природного происхождения. – Москва: «Практическая медицина», 2005. – 270 с.
В обзоре представлено влияние полисахаридной фракции
выделенной с плодового тела гриба L.
edodes (ПСФLE) и гликопептидной противоопухолевой вакцины (ПВ) на
метастазирование у мышей. Применение ПВ и ПСФLE отдельно или вместе подавляют процесс
метастазирования, в частности уменьшают частоту возникновения метастазов, е
тормозят рост и распространение метастазов. Антиметастатическая активность ГПВ
и ПСФLE зависит от режима, дозы и модельной системы
опухолевого роста.
Application of
PV and PSFLE
separately or it is united repress the process of innidiation, in particular
diminish frequency of origin of metastases, and also brake growth and
distribution of metastases. Antimetastatichna activity of GPV and PSFle depends
on the mode, dose and model system of tumour growth.