Шевченко Анастасія Павлівна
НТУУ "КПІ", Факультет біомедичної інженерії
Біомедичний матеріал на основі гідроксиапатиту та магнетиту
Медична сфера
вже давно переходить на лікування з використанням нанотехнологій, адже
можливість вилікувати пацієнта з найменшим шкідливим впливом на його організм є
досить перспективною.
Розглянемо
такий наноматеріал, як гідроксиапатит (ГАП). Він є біоактивним та біосумісним,
а також пришвидшує регенерацію кісток безпосередньо в місцях локалізації
ушкоджень. Враховуючи те, що регенераційні процеси в організмі людини суто
індивідуальні та залежать від віку, статі, загального стану здоров’я тощо,
знаходження методів контролю та впливу на ці процеси стає дуже важливим в
практиці лікування.
Одним з методів контролю над
регенераційними процесами в кістковій тканині є надання відновлюючому матеріалу
магнітних властивостей. Згідно досліджень, проведених італійськими вченими було
також продемонстровано збільшення проліферації остеобластів, тобто прискорення
регенерації кісткової тканини[1]. Звідси випливає доцільність створення
композиту з наданням йому магнітних властивостей, за допомогою додавання до ГАП
магнетиту. Такий матеріал дасть змогу пацієнтам, котрі мають пошкодження чи
захворювання в області опорно-рухового апарату, швидше відновлювати своє
здоров’я [2]. Особливо це актуально людям похилого
віку, регенеративні процеси яких майже призупинені. Тож основною проблемою створення
даного матеріалу є контроль над його регенеративною активністю в середовищі
організму.
Метою роботи
було: створити композиційний наноматеріал на основі ГАП та магнетиту, який
набув би магнітних властивостей, для контролю над процесами регенерації
кісткової тканини (КТ). Оскільки дослідження проведені італійськими вченими
показали підвищення проліферації клітин під впливом магнітного поля.
Розглянуто
два методи створення композиту: механічний та хімічний. Механічне змішування
проводиться в ступці його алгоритм наведений нижче[2].
Алгоритм
механічного синтезу композиту.
1.
Змішування: Оксалат
заліза, сахароза, ізопропанол розчиняються в дистильованій воді. В певному
порядку зливаються. Ретельно перемішуються протягом 90 хвилин механічним чи
магнітним змішуванням.
2.
Відстоювання: В
розчині має з’явитись осад протягом 3 годин.
3.
Повторне змішування –
допомагає одержати однорідну суміш.
Дані операції
повторюємо 3 рази.
4.
Фільтрація: Отриманий розчин зціджують через
фільтрувальний папір та осад висушують. На даному етапі ми отримаємо магнетит.
5.
Отримання композиту:
Магнетит (осад) змішують з гідроксиапатитом механічним способом в ступці
додаючи дистильовану воду.
Алгоритм
хімічного синтезу композиту:
1.
Змішування: Оксалат
заліза, сахароза, ізопропанол, гідроксиапатит розчиняють в дистильованій воді.
В певному порядку зливають. Ретельно переміщують протягом 90 хвилин механічним чи
магнітним змішуванням.
2.
Відстоювання: В
розчині має з’явитись осад протягом 3 годин.
Повторне змішування:
допомагає одержати однорідну суміш.
Дані операції
повторюємо 3 рази.
3.
Фільтрація: Отриманий
розчин зціджують через фільтрувальний папір та осад висушують. На даному етапі
ми отримаємо суміш готову до спікання.
4.
Розклад/відновлення:
Хімічна реакція розкладу/відновлення оксалату заліза має проходити в середовищі
важких вуглеводів (парафін) при температурі 450 оС (дозволено
відхилення на 5-10 одиниць).
Прилад для розкладу/відновлення –
лабораторна трубчаста піч з силітовим нагріваючим елементом, оскільки час
нагрівання до потрібної температури є
короткий.
Прилад для контролю за температурними
показниками в середовищі розкладу/відновлення – термопара. Суміш оксалату
заліза та гідроксиаптиту поміщають в спеціальний контейнер (кварцова трубка).
Далі контейнер розміщують всередині
трубчатої печі. Починають процес розкладу/відновлення, який триває 2 години при
температурі 450-460 оС. При розкладі/відновленні в середовищі важких
вуглеводів відбувається деструкція парафіну за рахунок розриву довгих ланцюгів.
Через дві години ми отримаємо композит.
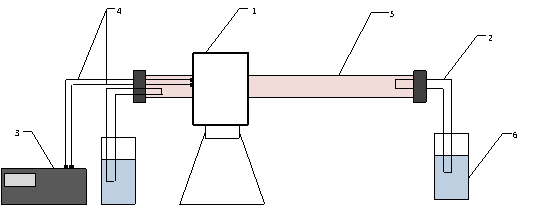
Рис. 1 Схема установки
для розкладу/відновлення композиційного матеріалу
Елементи схеми: 1.
Лабораторна трубчата піч з силітовим нагріваючим елементом 2.Трубка (2 штуки)
3.Термопара 4.Датчики температури 5.Колба з водою (2 штуки)
Опис результату проведеного
експерименту: отриманий порошок набув сірого кольору, оскільки відбулось змішування
сіруватого магнетиту та білого гідроксиапатиту. Емпірично перевіряємо магнітні
властивості: підносимо постійний магніт до отриманого композиту та чистого ГАП.
Спостерігаємо, що ГАП не реагує на магніт, композит відповідно притягується,
хоча сила притягання доволі мала, оскільки концентрація магнетиту низька.
Хімічний аналіз отриманого в ході
експериментальної роботи композиту показав допустимий для матеріалів
біомедичного призначення рівень вуглецю та заліза.
Таблиця 1
Результати хімічного
аналізу
|
Спосіб синтезу композиту |
Результати хімічного аналізу |
|
|
Вміст вуглецю |
Вміст заліза |
|
|
Механічне зміщування |
0,8 % |
1,04 % |
|
Хімічне змішування |
0,9 % |
0,96 % |
З даних, наведених в таблиці 1, бачимо
рівень заліза при механічному змішуванні є більшим ніж при хімічному, отже
композит отриманий хімічним змішуванням є менш токсичним оскільки не перевищує
позначку в 1%. Зокрема хімічне змішування дозволяє рівномірно розподілити
наночастинки магнетиту в гідроксиапатиті. Даний аспект підвищує однорідність
магнітних властивостей в композиті, а як наслідок і безпосередню якість матеріалу. Розглянуті
способи синтезу композиту створюють матеріал, що задовольняє нормам та вимогам
до медичних матеріалів. Але хімічне змішування переважає над механічним,
оскільки хімічне відбувається на молекулярному рівні. Беручи до уваги роботу з
наноматеріалами це є важливим позитивним фактором.
Тож було створенні та експериментально
перевірені умови для створення біомедичного композиційного матеріалу.
Список
літератури:
1.
Panseri S. Hydroxyapatite Bone
Substitutes to Enhance Tissue Regeneration: Evaluation In Vitro Using
Osteoblast-Like Cells and In Vivo in a Bone Defect / S. Panseri, C. Cunha, T.
D'Alessandro, M. Sandri, A. Russo // DOI: 10.1371 journal.pone – 2012 – 2-3 C.
2.
Уварова І.В. Наноматеріали медичного
призначення / І.В. Уварова, П.П. Горбик, С.В. Горобець, О.А. Іващенко, Н.В.
Ульянчич. – Київ: Наукова думка, 2014. – 230-235 с.