Физика /1.Теоретическая физика
Ястребов А.Ю.
Государственный морской университет имени
адмирала Ф.Ф.Ушакова ,
Россия
Энергетические зоны в кристаллах
Энергетические зоны. Химическую связь и
свойства кристаллических тел можно объяснить с использованием метода
молекулярных орбиталей. Согласно этому
методу при образовании химической связи образуются молекулярные орбитали,
охватывающие всю молекулу, причем происходит расщепление энергетических
состояний на связывающие молекулярные орбитали с низкой энергией и разрыхляющие
молекулярные орбитали с более высокой энергией.
При
взаимодействии большего числа электронов атомов образуется соответственно и
большее число молекулярных орбиталей и уменьшается разность энергий между ними
(рис.1).
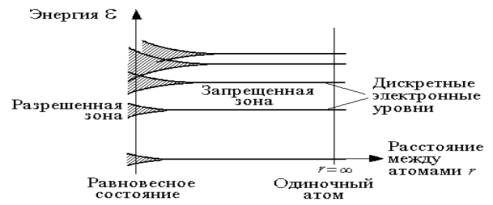
Рисунок 1. -Типичная схема образования энергетических
зон.
При
образовании кристаллов в химические связи вступает огромное число частиц N
и соответственно образуется огромное число молекулярных орбиталей, охватывающих
весь кристалл, разность между энергетическими уровнями молекулярных орбиталей чрезвычайно
мала. В результате образуются энергетические зоны, состоящие из огромного числа
подуровней (рис.2).
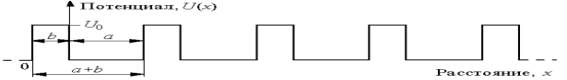
Рисунок 2. - Модели Кронига-Пенни.
Разность
между верхней и нижней энергиями зоны называется шириной зоны. Например, если
ширина зоны составляет 1 эВ, а в кристалле содержится 1
моль частиц, то разница между энергиями будет иметь порядок 10-21
кДж.
В изолированном атоме электроны способны
занимать лишь дискретные энергетические уровни, определяемые силами притяжения
к ядру и силами отталкивания от других электронов.
В результате из каждого дискретного
энергетического уровня атома или молекулы образуется энергетическая зона,
состоящая из очень близко расположенных энергетических уровней.
Типичная схема образования энергетических
зон. Дискретные уровни одиночного атома расширяются в энергетические зоны по
мере уменьшения межатомных расстояний в кристалле.
По мере сближения атомов сначала
расщепляются самые высокие энергетические уровни, затем по мере сближения
атомов – более низкие.
Самую верхнюю из зон, частично или полностью заполненную электронами, называют
валентной зоной, а ближайшую к ней незаполненную электронами – зоной
проводимости.
С точки зрения зонной теории все твердые
тела можно подразделить на две основные группы: материалы, у которых валентная
зона перекрывается зоной проводимости, и материалы, у которых валентная зона и
зона проводимости разделены запрещенной зоной.
Материалы, в энергетической диаграмме
которых запрещенная зона минимальна, относятся к проводникам,
материалы с узкой запрещенной зоной (менее
3 эВ) – к полупроводникам, материалы с широкой запрещенной зоной (более 3 эВ) – к диэлектрикам.
Электроны, находящиеся на этих уровнях,
приобретают способность перемещения по кристаллу. В модели Кронига-Пенни
решеточные потенциалы периодической
последовательностью прямоугольных потенциальных ям глубиной U и
шириной а, разделенных потенциальными барьерами шириной b,
так что постоянная решетки равна a + b.
Энергия электрона при этих условиях также
квантуется по периоду решетки: ξ=
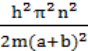 ;
;
где h=6.62*![]() ��=3.14, n = 1,2,3… , m=9.1*
��=3.14, n = 1,2,3… , m=9.1*![]() [кг].
[кг].
Стационарные состояния электрона описываются
квазиимпульсом P = hq,
аналогичным импульсу частицы в свободном пространстве при условии
q = p n/(a+b).
Таким образом, модель предсказывает серию
дискретных уровней, которые соответствуют уровням частицы “в ящике”. В таких
условиях электрон можно рассматривать находящимся внутри одной ячейки, хотя и
невозможно установить, в какой именно. Электрон обладает квазиимпульсом P = hq и
энергией e, которые
являются периодической функцией в пространстве волновых векторов (q-
пространство): e (q) = e (q + g) , где g - векторы обратной решетки abc.
В качестве элементарной ячейки обратной решетки выбирают первую зону Бриллюэна.
Научный
руководитель: к.п.н., доцент С.А.Мищик
ЛИТЕРАТУРА:
1. Бенуэлл К. Основы молекулярной спектроскопии:
Пер. с анг. М.: Мир, 1985. — 384 с.
2.
Вихман Э. Квантовая физика. – М.: Наука, 1974. — 391 с.
3. Савельев И.В. Курс физики. т.3.
Квантовая оптика. Атомная физика. Физика твердого тела. Физика атомного ядра и
элементарных частиц. М.: Наука. Гл. ред. физ.-мат. лит., 1989.—304 с.