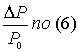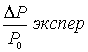Павлов А.М.
Восточно-Казахстанский государственный
университет им. С. Аманжолова
Усть-Каменогорск, Казахстан
Комплексы молекул и барический эффект
смешения газов
Экспериментальное исследование барического эффекта
смешения газов проводилось в [1, 2]. Попытки их теоретического описания были
сделаны в [3, 4, 5]. В [3] и [4] использовалась модель двух и трех жидкостей. В
[5] определялся барический эффект смешения с использованием только уравнения
состояния в вириальной форме. В данной статье делается попытка объяснить этот
эффект с использованием представлений о комплексах молекул.
В [5] считалось, что комплексы молекул автоматически
учитываются вторым вириальным коэффициентом. Позднее было выяснено, что это не
так. Второй вириальный коэффициент, подсчитанный теоретически, учитывает лишь
парные взаимодействия молекул независимо от того, на каком расстоянии друг от
друга они находятся. Комплекс представляет собой квазимолекулу, которая
характеризуется определенной энергией связи, что второй вириальный коэффициент
не учитывает.
Для построения теории барического эффекта смешения
газов будем находить из следующего уравнения состояния
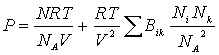 , (1)
, (1)
где
![]() … - число структурных единиц,
… - число структурных единиц, ![]() - число комплексов
размерности «k»,
- число комплексов
размерности «k», ![]() - число Авогадро.
- число Авогадро.
Введем сюда концентрацию комплексов ![]() и коэффициент
и коэффициент 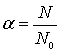 . Тогда (1) примет вид:
. Тогда (1) примет вид:
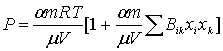 . (2)
. (2)
При
определенном выборе комбинационных соотношений для ![]() коэффициент
коэффициент ![]() в квадратной скобке
сокращается.
в квадратной скобке
сокращается.
Тогда давление смеси газов можно записать в виде
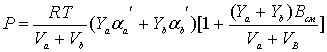 (3)
(3)
а
начальное давление до смешивания будет
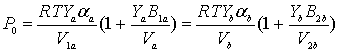 , (4)
, (4)
где
буквами a и b обозначены
смешиваемые газы и их характеристики. В (3) ![]() и
и ![]() представляют собой
коэффициенты
представляют собой
коэффициенты ![]() первого и второго
газа после смешивания. Предполагается, что после смешивания концентрация
комплексов того и другого газа вследствие их расширения до объема
первого и второго
газа после смешивания. Предполагается, что после смешивания концентрация
комплексов того и другого газа вследствие их расширения до объема ![]() изменится.
изменится.
Сложность задачи заключается в том, чтобы выразить ![]() и
и ![]() через
через ![]() и
и ![]() . Нетрудно доказать, учитывая определения
. Нетрудно доказать, учитывая определения ![]() , что
, что
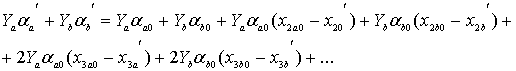
Можно показать, что примерно
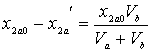
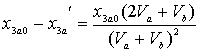 и т.д.
и т.д.
После подстановки этих выражений в (3) можно
определить ![]() :
:
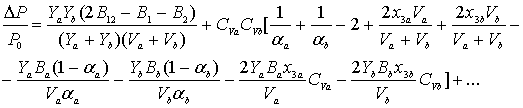 (5)
(5)
Если ввести сюда мольные плотности, то (5) примет вид:
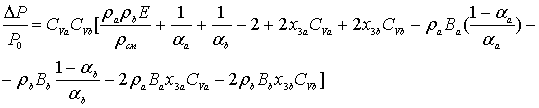 , (6)
, (6)
где
![]() ;
; 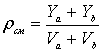 .
.
Если пренебречь процессами компелексообразования, то
будет ![]() ,
, ![]() и
и
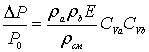 . (7)
. (7)
Формула
(7) проще, чем была раньше получена в [5]. Однако она дает достаточно большую
погрешность, что доказывает необходимость учета комплексов при описании данного
эффекта.
Следует еще отметить, что при выводе формул (5) и (6)
не учитывались смешанные кластеры молекул. Для такого пренебрежения имеются
следующие основания: при взаимодействии однородных молекул наблюдается
резонанс, который существенно увеличивает энергию связи. По нашим расчетам
вследствие резонансного взаимодействия энергия связи возрастает почти на
порядок. Однако, учитывая, что резонанс может давать не только притяжение, но и
отталкивание, можно считать, что резонансное взаимодействие увеличивает энергию
вдвое. Понятно, что резонансное воздействие может наблюдаться только у
однородных молекул, у которых квантовые переходы одинаковые. Конечно, и
разнородные молекулы могут объединяться в комплексы. Однако, из приведенных
выше соображений следует, что их должно быть меньше, чем однородных комплексов.
В заключение приведем сравнение расчетов барического
эффекта по выведенным формулам с экспериментом.
Таблица 1
Барический эффект смешения аргона с углекислым газом
при Т=293 К (![]() и
и ![]() подсчитаны
по давлению и плотности).
подсчитаны
по давлению и плотности).
|
Р0,бар |
ρа |
ρв |
|
|
|
10 |
0,4130 |
0,434 |
0,0072 |
0,005 |
|
40 |
1,6830 |
2,22 |
0,047 |
0,046 |
|
50 |
2,115 |
3,217 |
0,075 |
0,073 |
Как видно из таблицы, теория дает неплохое согласие с
опытом. Полученные здесь формулы существенно отличаются от подобных формул,
выведенных в [3] и [4] и более точно согласуются с экспериментальными данными.
Литература
1.
Брованов И.С.
Исследование сжимаемости некоторых бинарных смесей газов в области давлений 59-590
бар. Автореферат дисерт. на соиск. уч.ст. кан.физ.мат.наук. – Алма-Ата, 1975
2.
Шамсутдинов И.Г.
Исследование эффектов смешения некоторых газов при разных давлениях и
температурах до линии насыщения одного из компонентов. Автореферат дисерт. на
соиск. уч.ст. канн.физ.мат.наук. – Алма-Ата, 1982
3. Zandbergen Pand
Beenakker J.J.M. Theoretical determination of the volume change on mixing for
gaseous N2-M2 , Ar-H2 and Ar-N2 at
1700K up mo 100 at // Physics 33, 1967, 366-378 p.
4. Knoster M. and
Beenakker J.J.M. Corresponding states treatment for the excess enthalpy of
moderately dense gaseous mixtures // Physics 33, 1967, 410-423 p.
5.
Павлов А.М. К эффектам
смешения идеальных газов // Известия
вузов. Физика. 1985 № 1. с 120-121