Жакупова
А.Н., Евсеева Е.Ю.
Инновационный
Евразийский Университет, Казахстан
Воздействие алюминия на окружающую
среду и организм человека
Современное понятие экологии
человека.
Ученые всего мира уделяют большое внимание проблемам экологии, так как окружающая
природная среда и здоровье человека взаимозависимы.
Экология человека изучает законы взаимодействия природной среды и человека [1].
Экология (oikos - дом, жилище, logos - понятие, учение) занимается
изучением отношений растительных и животных организмов (включая человека).
Немецкий биолог и философ Эрнст Геккель (1834 – 1919 гг.) в своей книге под названием «Всеобщая морфология организмов» впервые
озвучил определение экологии как «... общей науки об отношении организмов к
окружающей среде, куда мы относим все «условия существования» в широком смысле
этого слова...». Так же мы можем там найти еще две точные формулировки
экологической науки: "Экология - это познание экономики природы,
одновременное исследование взаимоотношений всего живого с органическими и
неорганическими компонентами среды, включая непременно неантагонистические и
антагонистические взаимоотношения животных и растении, конкурирующих друг с
другом. Экология - наука, изучающая все сложности взаимосвязи и взаимоотношения
в природе, рассматриваемые Ч. Дарвиным как условия борьбы за существование».
Экология человека оценивает степень зависимости здоровья населения от
внешних факторов [2].
Рассмотрим причины, оказывающие влияние на здоровье населения согласно Всемирной
организации здравоохранения (схема 1):
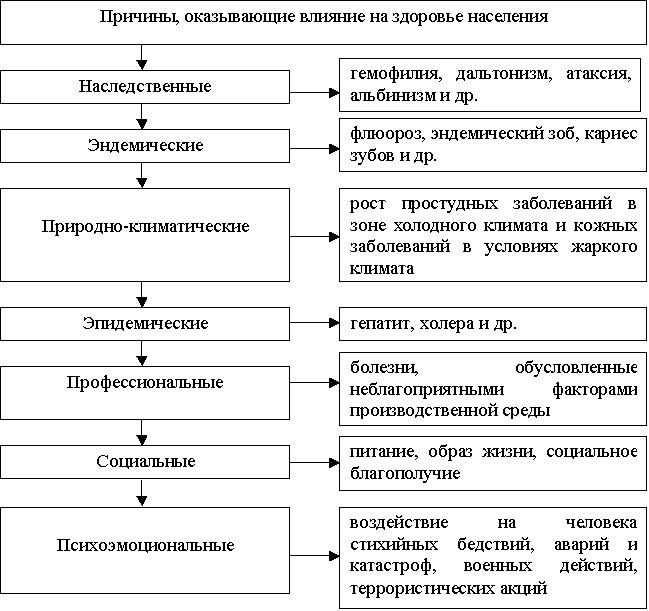
Схема 1 – Основные причины, влияющие на здоровье населения согласно
Всемирной организации здравоохранения
Следует отметить, что заболевания связанные с экологией, можно представить двумя
группами:
1 группа - экологически
обусловленные заболевания (эндемические заболевания; заболевания, которые
вызваны под воздействием радиации; химические отравления при выбросах в природную
среду);
2 группа - экологически зависимые заболевания (рост заболеваемости
населения; детская заболеваемость; рост онкологии и др.).
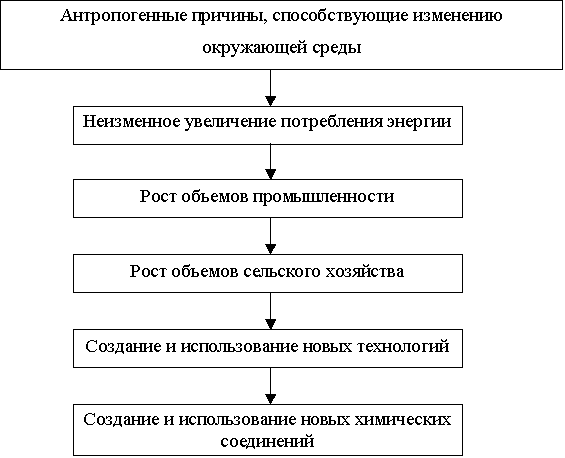 На схеме 2 приведены антропогенные
причины, которые способствуют изменению окружающей среды.
На схеме 2 приведены антропогенные
причины, которые способствуют изменению окружающей среды.
Схема 2 - Антропогенные причины, способствующие изменению окружающей среды
В результате человеческой деятельности в экосистеме Земли возникли следующие
аномалии: изменился и в настоящее время
продолжает изменяться газовый состав атмосферы, значительно проявляется
парниковый эффект. Вследствие этого резко изменился климат и
погода, в различных странах выпадают кислотные дожди, истончается озоновый
слой, что приведет к губительному действию ультрафиолетового излучения Солнца.
Основными источниками поступления в атмосферу техногенных загрязнений
являются: автомобильный транспорт, предприятия металлургии, нефтехимические
предприятия. Загрязнения, выбрасываемые в атмосферу, оседают в водоемах, на
поверхности почвы, затем попадают в грунтовые воды, заражая тем самым водоемы.
Особенно интенсивно загрязняется почва. Возле промышленных предприятий в
почве наблюдается накопление высоких концентраций следующих вредных химических
веществ: Pb, F, Hg, As, Mn, Cd, Ni. Все перечисленные химические
вещества приводят к возникновению заболеваний [3].
Медики очень обеспокоены тем, что состояние природной среды является неблагоприятным,
что отрицательно воздействует на здоровье человека. Все развитые страны ведут исследования
по решению экологических проблем.
У беременных женщин и новорожденных наблюдается нарушение функций
эндокринной, иммунной, кроветворной систем, вследствие проживания в
экологически неблагополучных местах.
Безусловно, загрязненная окружающая среда отрицательно
влияет на здоровье взрослого населения, причем в промышленных регионах значительная
часть трудоспособных жителей подвергается воздействию факторов профессиональной
вредности [4]. Так в экологически неблагоприятных регионах взрослое население
страдает хроническими заболеваниями дыхательных путей и легких в 2,5-3 раза
чаще, подвержено сердечно-сосудистым заболеваниям в 2-2,5 раза больше и болеет
расстройствами нервной системы в 1,2-1,9 раза. Рост загрязнения природной среды
химическими и радиоактивными веществами влечет за собой рост онкологических
заболеваний.
Алюминий: открытие, физико-химические
свойства, литофильность, биофильность, технофильность.
Алюминий был открыт в 1825 г. Гансом Эрстедом при действии амальгамы калия
на хлорид алюминия. Название
алюминий получил от латинского слова alumen – квасцы [5]. Содержание алюминия в земной коре составляет 8.8%.
Как писал более
100 лет назад Д.И.Менделеев в своем учебнике «Основы химии», из всех металлов
"алюминий есть самый распространенный в природе; достаточно указать на то,
что он входит в состав глины, чтоб ясно было всеобщее распространение алюминия
в коре земной. Алюминий, или металл квасцов (alumen), потому и называется иначе
глинием, что находится в глине" [6].
Основные физические свойства
алюминия представлены в таблице 1.
Таблица
1 - Физические свойства алюминия
|
Свойства алюминия |
|
|
Цвет |
Серебристо-белый |
|
Плотность |
2,7 г/см³ |
|
Температура плавления технического алюминия |
658 °C |
|
Температура плавления алюминия высокой
чистоты |
660 °C |
|
390 кДж/кг |
|
|
Температура кипения |
2500 °C |
|
10,53 МДж/кг |
|
|
24…32 кгс/мм² |
|
|
Пластичность технического алюминия |
35% |
|
Пластичность чистого алюминия |
50% |
|
Электропроводность |
37·106 См/м |
|
203,5 Вт/(м·К) |
|
|
Светоотражательная способность |
Высокая |
Алюминий образует
следующие сплавы: сплавы с медью
и магнием (дюралюминий), с кремнием (силумин).
Рассмотрим химические
свойства алюминия. Алюминий является активным металлом. На воздухе поверхность алюминия
покрывается пленкой оксида Al2О3, препятствующей доступу кислорода (O2)
к металлу, приводя к прекращению реакции, что является условием наличия антикоррозионных
свойств алюминия.
Алюминий реагирует с
растворами щелочей. При этом сначала растворяется защитная оксидная пленка по
реакции:
Al2О3 + 2NaOH + 3H2O
= 2Na[Al(OH)4].
Затем протекают
следующие реакции:
2Al + 6H2O = 2Al(OH)3 + 3H2,
NaOH + Al(OH)3 = Na[Al(OH)4],
или суммарно:
2Al + 6H2O + 2NaOH = Na[Al(OH)4]
+ 3Н2,
и в результате
образуются алюминаты: Na[Al(OH)4] - алюминат натрия, тетрагидроксоалюминат
натрия; К[Al(OH)4] - алюминат калия, терагидроксоалюминат
калия. В связи с тем, что для атома алюминия в этих соединениях характерно
координационное число 6, то действительные формулы данных
тетрагидроксосоединений следующие:
Na[Al(OH)4(Н2О)2]
и К[Al(OH)4(Н2О)2].
При нагревании
алюминий реагирует с галогенами:
2Al + 3Cl2 = 2AlCl3,
2Al + 3 Br2 = 2AlBr3.
Реакция между
порошками алюминия и йода начинает
происходить при комнатной температуре, путем добавления в исходную смесь
нескольких капель воды, которая в свою очередь играет роль катализатора:
2Al + 3I2
= 2AlI3.
Взаимодействие
алюминия с серой S
при нагревании приводит к образованию сульфида алюминия Al2S3:
2Al + 3S =
Al2S3,
далее сульфид алюминия
Al2S3 разлагается водой с образованием гидроксида
алюминия Al(ОН)3:
Al2S3
+ 6Н2О = 2Al(ОН)3 + 3Н2S.
В лабораторных
условиях гидроксид алюминия Al(OH)3 можно получить в виде студенистого
осадка обменными реакциями:
Al2(SO4)3 + 6NaOH =
2Al(OH)3 + 3Na2SO4,
или за счет добавления
соды Na2CO3 к раствору соли алюминия AlCl3:
2AlCl3 + 3Na2CO3 +
3H2O = 2Al(OH)3 + 6NaCl + 3CO2,
а также путем добавления
раствора аммиака NH3·H2O к
раствору соли алюминия AlCl3:
AlCl3 + 3NH3·H2O = Al(OH)3 + 3H2O + 3NH4Cl.
Алюминий является литофильным элементом (свойство, означающее химическое сродство к органическим веществам,
синоним гидрофобности), входит в состав силикатных, алюмосиликатных горных пород, образует
сульфатные, карбонатные, фосфатные, боратные минералы.
Технофильность (соотношение количества добываемого элемента к его
содержанию в земной коре) алюминия равна:
1,5*107 /0,088*4,7*107 = 3,62*10-9
где 4,7*107 триллионов т масса Земной коры.
Биофильность алюминия - отношение среднего содержания элемента в живом
веществе планеты к содержанию в земной коре - составляет:
7,45 / 8,8 = 0,84 или 84,0 %
Биохимическая функция алюминия.
Алюминий обладает большим сродством к кислороду, постоянной валентностью (III).
Алюминий входит в состав тканей животных и растений; в органах
млекопитающих животных обнаружено от 10-3 до 10-5% алюминия (на сырое
вещество).
Суточная потребность в алюминии взрослого человека составляет 35-49 мг. Алюминий
накапливается в печени, поджелудочной и щитовидной железах.
Образуя нерастворимые соединения с фосфатами, алюминий нарушает питание
растений и животных [7].
Получение алюминия и его
применение.
В промышленных условиях алюминий получают путем электролиза глинозема Аl2О3,
растворенного в расплавленном криолите NaSAlF6 при t=950° С.
Электролитная ванна – это железный кожух, футерованный изнутри огнеупорным
кирпичом. Рабочий объем электролитной ванны заполняется расплавленным
электролитом (6-8% Аl2О3 и 94-92% NaSAlF6).
Катодом служит подина ванны, анодом -
погруженные в электролит угольные обожженные блоки. При электролизе на катоде
выделяется расплавленный алюминий, на аноде - кислород, образующий с угольным
анодом угарный газ (CO) и углекислый газ (CO2).
Благодаря своим универсальным физико-химическим и механическим свойствам
алюминий нашел широкое применение:
- в электротехнике;
- в производстве зеркал;
- в качестве конструкционного материала в ядерных реакторах;
- является сырьем в авиационной и авиакосмической промышленности;
- в алюминиевых резервуарах хранят и осуществляют транспортировку жидких
газов (метан, кислород, водород), азотной и уксусной кислоты, чистой воды,
перекиси водорода и пищевых масел;
- для упаковки пищевых продуктов;
- для производства кухонной посуды;
- для отделки зданий и сооружений;
- в металлургии алюминий применяют в качестве легирующей добавки в сплавах на основе меди (Сu), магния
(Mg), титана (Ti), никеля (Ni), цинка (Zn) и железа (Fe);
- в производстве взрывчатых веществ.
Санитарно-гигиеническая
характеристика алюминия.
Алюминий относится к токсическим элементам.
ПДК алюминия установлена на уровне 0,5 мг/л, лимитирующий признак вредности
- санитарно-токсикологический, класс опасности - 2. Рекомендуемая ВОЗ
концентрация алюминия 0,2 мг/л обеспечивает компромиссное решение между
практическим применением солей алюминия при очистке воды и обесцвечиванием воды
в распределительной сети [8].
При электролитическом производстве алюминия возможны поражения
электрическим током, высокой температурой и вредными газами. Во избежание
несчастных случаев ванны изолируют, рабочие должны пользоваться сухими
валенками, спецодеждой. Обязательно должна поддерживаться вентиляция. При
постоянном вдыхании пыли металлического алюминия и его оксида может возникнуть
алюминоз легких.
Влияние алюминия на здоровье
человека.
Источниками поступления алюминия являются пища, вода, воздух, лекарства, посуда,
сделанная из алюминия.
Токсичность алюминия проявляется во влиянии на минеральный обмен веществ,
на функцию нервной системы человека. Избыток солей алюминия снижает задержку
очень важного элемента - кальция (Ca), уменьшает адсорбцию фосфора
(P). Проявления нейротоксического действия: нарушение двигательных функций, судороги,
снижение или потеря памяти.
Обобщая
вышеперечисленное, сделаем вывод: так как алюминий является токсичным элементом, то необходимо
снизить экологическую опасность алюминиевых производств путем разработки новых современных
технологий производства алюминия, эффективных технологий очистки сточных вод от
алюминия, а так же вести строгий контроль за выбросами и сбросами соединений
алюминия в природную среду.
Литература: