Вступ. Недостатність функції щитоподібної залози вважається однією з частіших
причин гормонального безпліддя у жінок і може супроводжуватися різними
порушеннями менструального циклу [2], фертильності[5], підвищують частоту самовільних абортів та внутрішньоутробної
загибелі плода, а в більш віддаленому періоді
несприятливо впливають на
когнітивний розвиток потомства [8]. Зміни гормонального профілю супроводжуються
порушеннями гемодинаміки в органах репродуктивної системи [4] .
Зміна васкуляризації яєчників може відображати їх реакцію на специфічні ангіогенні
сигнали і зміни метаболічних процесів в фолікулі, який розвивається і росте [1,
6]. Ультразвукова доплерометрія дозволяє здійснити
кольорове картування кровотоку в
яєчнику і отримати характеристики кривих швидкостей кровотоку в таких судинах: яєчниковій артерії в області її
впадання в ворота яєчників, стромальних артеріях, а також судинах стінки
фолікула і жовтого тіла [7, 9]. Застосування ультразвукового і
доплерометричного досліджень яєчників для діагностики деяких форм безпліддя і
моніторингу фолікулоґенезу в процесі лікування є неоціненним підґрунтям для
лікаря в плані аналізу функціонального резерву яєчників і прогнозування їх
відповіді на ендогенні стимулятори [3].
Матеріали та методи. Проводилось обстеження 58 жінок, які мали показники
зниженої функції щитоподібної залози (з них 50 (86,2%) з первинним та 8 (13,7%)
вторинним непліддям). В результаті детального обстеження безплідних жінок
субклінічний гіпотиреоз було виявлено у 28 жінок, вони склали 1 групу
обстежуваних. Маніфестний гіпотиреоз у жінок з непліддям було виявлено у 30 пацієнток, які склали 2 групу
обстежуваних. Контрольну групу склали 38 практично здорових жінки
репродуктивного віку без соматичної та гінекологічної патології, з двофазним
менструальним циклом. Крім того було відібрано групу порівняння у яку увійшли
30 жінок з маніфестним гіпотиреозом різного ступеню важкості, що знаходились на
лікуванні в РОЕД з метою корекції замісної терапії левотироксином, які не
пред’являли скарг на порушення репродуктивної функції і які за віком масою та
основними біохімічними показниками були ідентичні до обстежуваних пацієнтів 2
групи.
Спільно з
ендокринологом проводилася замісна терапія препаратами левотироксину, дозування
якого підбиралося в залежності від ступеня порушення функції ЩЗ. Контроль
ефективності проведеної терапії проводився через 3 місяці після початку
лікування. Критерієм адекватності призначеної дози левотироксину вважалось
зниження сироваткового рівня ТТГ нижче 2,0 мМО/л.
З метою
корекції дисліпідемій, що була характерною для більшості жінок з безпліддям та
гіпотиреозом і яка є, як було нами встановлено, предиктором репродуктивних
порушень у даного контингенту жінок, запропоновано включити в комплекс
лікувальних заходів засоби, які нормалізують ліпідний обмін. В якості
гіполіпідемічної терапії було визначено еспа-ліпон ®600 (по 1 табл. в день) –
тіоктова (альфа-ліпоєва) кислота, яка виявляє окрім гіполіпідемічної,
гепатопротекторну та дезіноксикуючу дію, є ендогенним антиоксидантом, стимулює
обмін холестерину, а по характеру біохімічних взаємодій близька до вітамінів
групи В.
Оскільки у
жінок 1 і 2 груп було виявлено порушення кровообігу в судинах матки та яєчників
(індексу резистентності та зменшення максимальної систолічної швидкості),
доцільним є призначення Актовегіну - вазоактивного препарату з протитромботичними
та антиоксидантними властивостями (А.
С. Аметов и др., 2007). Тобто для жінок 1 та 2 груп призначалося лікування:
1. Левотироксин по 50-200 мкг на добу щоденно;
2. Еспа-ліпон ®600 по 1 табл. на добу;
3. Актовегін по 1 драже тричі на добу.
Жінкам 4
групи проводилася терапія левотироксином по 50-200 мкг на добу.
З метою
вивчення функціонального стану матки та яєчників було проведено ультразвукове
дослідження разом з доплерометричним
картуванням, яке здійснювали на апараті «LOGIO 7 EXPERT» відповідно до фаз
менструального циклу протягом одного менструального циклу в ранню фолікулярну
(2-3 день менструального циклу), преовуляторну та середню и пізню лютеїнові
фази менструального циклу. Вказане обстеження проводилось всім жінкам.
Здійснювалось
визначення розмірів матки, товщини ендометія та фіксація показників гемодинаміки в маткових артеріях. При
дослідженні стану яєчників визначалися розміри преовуляторного фолікулу та стан
кровотоку в його стінці - максимальна систолічна швидкість (МСШ) та індекс
резистентності судин (ІР), розміри жовтого тіла та ступінь його васкуляризації.
Наведені дані отримані до початку
лікування та статистично оброблені за допомогою пакета статистичних програм
“Statistica 5.5 for Windows” (“Stat Soft”, США).
Результати досліджень
та їх обговорення.
При аналізі
ехографічних характеристик стану матки в процесі лікування було досліджено
динаміку змін товщини ендометрію. Стан яєчників оцінювали за їх величиною та
показниками васкуляризації і кровотоку.
Динаміка товщини
ендометрію, яка може легко контролюватися сонографічними методами, є
об’єктивним критерієм відгуку репродуктивної системи жінки на гормональні
зміни протягом менструального циклу.
При аналізі стану товщини ендометрію в різні фази менструального циклу було
встановлено, що у всіх обстежуваних існує кількісна динаміка змін товщини
ендометрію, яка відповідає фазам менструального циклу. Проте, якісне
відображення функціональної активності у вигляді менструацій було притаманно лише
жінкам контрольної групи. У всіх інших жінок на початку та в процесі
дослідження, як це було вказано нами вище, відмічались менструальноподібні
кровотечі. Таким чином вивчення динаміки змін товщини ендометрію у різні фази
менструального циклу зможе вказати на якісні зміни в ендометрії у відповідь на
гормональні впливи замісної терапії левотироксином та у комплексі з
активаторами місцевого метаболізму -
ліпоєвою кислотою та актовегіном.
В процесі
лікування було встановлено, що у І фазу маткового циклу показники товщини
ендометрію у обстежених жінок хоча і були дещо меншими ніж у жінок контрольної
групи, проте істотно від них не відрізнявся. Аналогічна картина спостерігалася
і після проведеної терапії: достовірних відмінностей між показниками товщини
ендометрію у обстежуваних та групою контролю виявлено не було (таб. 1).
Таблиця
1
Ехографічні
характеристики ендометрію в процесі лікування, M±m
|
|
І фаза циклу |
ІІ фаза циклу |
|
|
Група 1 (n=28) |
До лікування |
6,3±0,6 |
9,2±1,1• |
|
Після лікування |
6,6±0,6 |
9,7±1,0 |
|
|
Група 2 (n=30) |
До лікування |
6,2±0,6 |
8,8±0,6• |
|
Після лікування |
6,4±0,6 |
9,8±0,5• |
|
|
Група 3 (n=38) |
7,4±0,5 |
12,2±0,8 |
|
|
Група 4 (n=30) |
До лікування |
6,2±0,5 |
8,6±0,5• |
|
Після лікування |
6,5±0,6 |
8,8±0,4• |
|
Примітка: • – різниця вірогідна відносно показника групи контролю, р<0,05
Дещо інша картина спостерігалася при дослідженні
цього показника в середині ІІ фази. Було виявлено, що у всіх жінок як до
початку терапії так по її закінченню товщина ендометрію достовірно відрізнялась
від аналогічного показника групи контролю. Виключення становили жінки 1 групи,
у яких по закінченню проведеної терапії
не відмічали достовірних відмінностей товщини ендометрію порівняно з
аналогічним показником жінок 3 (контрольної) групи.
При
проведенні аналізу динаміки змін товщин ендометрію в процесі лікування було виявлено, що у 1 групі зміна товщини
ендометрію з початку проліферативної фази маткового циклу до середини
секреторної достовірно не відрізнявся від аналогічного показника групи контролю
як до початку лікування так і через 3 місяці лікування. Між собою ці показники
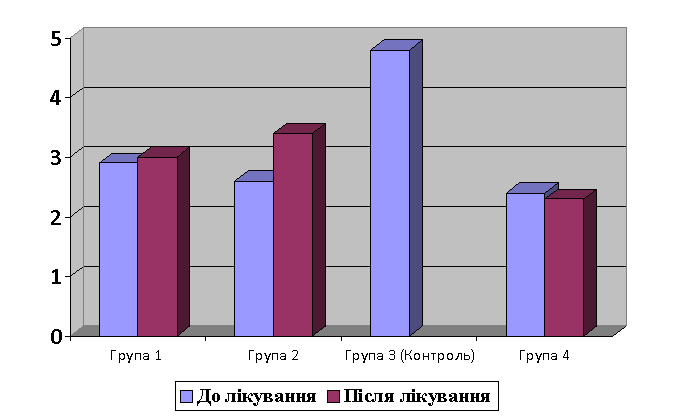
також вірогідно не відрізнялися (Рис. 1.).
 Примітка. * – різниця вірогідна
відносно показника групи контролю (р<0,05).
Примітка. * – різниця вірогідна
відносно показника групи контролю (р<0,05).
Рис. 1.
Динаміка змін товщин ендометрію в
процесі лікування, мм.
У 2 групі
динаміка змін товщини ендометрію була наступна - на початку лікування, протягом
маткового циклу, товщина ендометрію збільшилася на (2,6±0,5) мм, проте через 3 місяці вона відмічалася в
межах (3,4±1,1) мм, що становило зростання цього показника на 30,8 %. Як
і у
1 групі, ці показники вірогідно не відрізнялися від групи контролю.
Аналіз динаміки зміни товщини ендометрію 4 групи показав, достовірні
(р<0,05) відмінності зростання товщини ендометрію протягом маткового циклу
від аналогічних показників групи контрою. Також не відмічено ніякої динаміки
змін товщин ендометрію протягом маткового циклу між початком та кінцем лікування з використанням монотерапії левотироксином. Більше того, нами було
виявлено негативну (хоча і недостовірну) динаміку з (2,4±0,5) мм до (2,3±0,5) мм, що говорить
про недостаню ефективність монотерапії для відновлення репродуктивної функції
жінки. Динаміка збільшення ендометрію у жінок, які використовували
запропонований нами комплекс, була ж суттєво більшою, ніж у тих, хто використовував традиційну
монотерапію левотироксином.
При
встановленні групових даних перифолікулярного кровотоку було встановлено
незначне зниження показників індексу резистентності в ранню фолікулінову фазу
циклу (таб. 2) з 0,55±0,07 до 0,52±0,08
у жінок 1 групи. У жінок 2 групи встановлено достовірне зниження цього ж
показника з 0,75±0,02 до 0,51±0,02 (р<0,05). У групі порівняння (4 група)
цей показник знизився з 0,76±0,03 до 0,64±0,05, що
також мало ознаки достовірної відмінності (р<0,05). Крім того, у І фазу циклу індекс резистентності в цій
групі до початку лікування мав достовірні відмінності від аналогічного
показника групи контролю. Проте наприкінці обстеження та лікування цей показник у І фазі циклу, від групи контрою (3 група) уже достовірно не відрізнявся.
Дослідження
максимальної швидкості кровотоку в інтраоваріальних судинах під впливом терапії
показало, що даний показник у І фазу оваріального циклу зазнав достовірного (р<0,05)
збільшення у всіх досліджуваних групах. Встановлено, що підйом значення цього
показника відбувся з (11,23±0,43) см/с до (13,46±0,44) см/с у жінок 1 групи; з (9,14±0,52) см/с до (13,14±1,02) см/с у жінок 2 групи та
з (9,34±0,57) см/с до (12,28±0,53) см/с у 4 групі.
Таблиця
1
Характеристики яєчникового кровотоку в
процесі лікування, M±m
|
Фази циклу |
І фаза циклу |
ІІ фаза циклу |
|||
|
|
|
МСШ (см/с) |
ІР |
МСШ (см/с) |
ІР |
|
Група 1 (n=28) |
До лікування |
11,23±0,43 |
0,55±0,07 |
10,97±0,48 |
0,56±0,09 |
|
Після лікування |
13,46±0,44* |
0,52±0,08 |
16,95±0,45•* |
0,50±0,08 |
|
|
Група 2 (n=30) |
До лікування |
9,14±0,52• |
0,75±0,02• |
10,07±0,51• |
0,77±0,07• |
|
Після лікування |
13,14±0,52* |
0,51±0,02* |
15,70±0,65•* |
0,51±0,08* |
|
|
Група 3 (n=38) |
12,54±0,54 |
0,53±0,02 |
18,27±0,66 |
0,48±0,03 |
|
|
Група 4 (n=30) |
До лікування |
9,34±0,57• |
0,76±0,03• |
10,30±0,56 |
0,71±0,03 |
|
Після лікування |
12,28±0,53* |
0,64±0,05* |
12,35±0,94•* |
0,61±0,04•* |
|
Примітка: 1. * – різниця
вірогідна відносно показника до лікування, р<0,05;.
2. • – різниця вірогідна відносно показника групи контролю, р<0,05.
При
порівнянні аналогічних показників максимальної систолічної швидкості та індексу
резистентності в судинах яєчника в ІІ фазу циклу були встановлені показники, які
показували достовірне збільшення в процесі лікування максимальної систолічної
швидкості у 1, 2 та 4 групах
(р<0,05), а ІР зазнав достовірних
змін (р<0,05) лише у жінок, які приймали лікувальний комплекс (1 та 2
група), У жінок, шо отримували традиційну терапію левотироксином достовірних
змін ІР не відбулося (р>0,05).
Висновок
Виявлені
факти говорять про значне покращення кровообігу в яєчникових судинах у всіх
жінок, які приймали замісну гормональну терапію левотироксином проте зміни
еластичності стінок судин відмічали у тих пацієнток, котрі використовували
запропонований нами комплекс. Зміни
кровотоку свідчать про встановлення
балансу тироїдних гормонів, гармонійного співвідношення гормональних
фракцій гонадотропінів та оваріальних стероїдів, шо призводить до відновлення
репродуктивної функції жінки у вигляді повноцінних оваріальних циклів.
Література
1. Александрова Н. В.
Современные подходы к оценке овариального резерва у женщин с преждевременной
недостаточностью яичников (обзор литературы) / Н. В. Александрова, Л. А. Марченко // Проблемы
репродукции. — 2007. — № 2. — С. 25—28.
2. Демина Т.Н. Состояние
репродуктивной системы у больных с нарушением функции щитовидной железы/ Т.Н.
Демина // Вестник новых медицинских технологий. — 1998 — Т. 5, № 2. — С. 45—47.
3. Мартинишин О.Б.
Роль доплерометрії оваріальних артерій при різних формах акваріальної
недостатності / О. Б.
Мартинишин, Г. В. Чайка, А. Л. Костюк // Таврический
медико-биологический вестник. — 2012, —Т. 15, №2. — С. 264—266
4. Мишиева
Н. Г. Оценка овариального резерва у женщин репродуктивного возраста и его
значение в прогнозировании успеха лечения бесплодия / Н. Г. Мишиева, Т. А.
Назаренко // Проблемы репродукции. — 2008. — № 4. — С. 62—65.
5. Оксюта В.М. Стан менструальної
функції у жінок з безпліддям на фоні гіпотиреозу / В. М. Оксюта, Б. Ф.
Мазорчук, А. П. Дністрнська // Вісник
Вінницького національного медичного університету. — 2011. — № 2, Т15. — С.
282—284.
6 Попов А. А. Эндоскопическая хирургия в подготовке к ЭКО / А. А.
Попов // В сб. современные технологии в профилактике перинатальной и материнской смертности. –
Новосибирск, 2001. — С. 221—222.
7. Gougeon A.
Age-related changes of the population of human ovarian follicles: Increase in
the disappearance rate of non-growing and early-growing follicles in aging
women / A. Gougeon, R. Echochard, J. C. Thalabard // Biol Reprod. — 1994. —
Vol. 50. — P. 653—663.
8. Redmond G.P. Hypothyroidism and women's
health. / Redmond G.P. // International Journal of Fertility and Women's
Medicine. — 2002. — May-Jun — Vol. 47(3).
— P. 123-127.
9. Sherman B. M. The menopausal transition: analysis of LH, FSH,
estradiol and progesterone concentration during menstrual cycles of older women
/ B. M. Sherman, S. G. Korenman // J. Clin. Endocrinol. Metab. — 1976. — Vol.
42, № 4. — Р. 629—636.