Вдовина Е.Е., Плешкова
О.Г., Шипунов Б.П.
Алтайский государственный университет,
Россия
Влияние ВЧ поля на кристаллизацию
аквакомплексов NiSO4×7H2O и CuSO4×5H2O
Вода с измененной структурой обладает
уникальными свойствами, аномальность которых остается одной из неразрешенных
задач. Изучение влияния физических полей различной природы на водные растворы
становится все актуальнее. В частности, много исследований посвящено влиянию
магнитного поля на свойства водных растворов, которые уже достигли определенных
выводов, таких как увеличение скорости кристаллизации и уменьшении
кристаллической фазы [1]. Исследования, касающиеся влияния высокочастотного
поля на структуру воды, а в особенности на изменение свойств водных растворов,
только набирают ход. [2]Именно этим обусловлена актуальность данной работы по
изучению влияния ВЧ-поля на аквакомплексы NiSO4·7H2O
и CuSO4×5H2O.
До сих пор остается не ясным воздействие измененной воды на структуру
кристаллогидратов. Для изучения свойств облученной воды были выбраны два аквакомплекса,
отличающиеся по своим свойствам. Для начала рассмотрим их структуру.
Пентагидрат сульфата меди (II)
содержит аквакомплексы – катион тетрааквамеди (II) и слабо
связанную внешнесферную молекулу воды, которая объединяет катионы и
анионы посредством водородных связей.
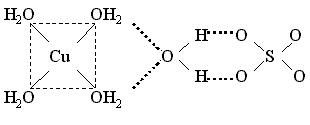
Рисунок 1 – Структура сульфата меди пятиводного
Координационная формула указанного соединения, учитывающая состав внутренней и
внешней сферы, такова: [Cu(H2O)4]SO4 . H2O.
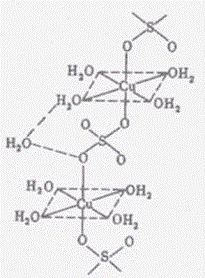
Рисунок 2 – Пространственная структура сульфата меди пятиводного
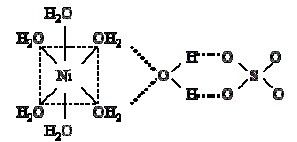
Рисунок 3 – Структура сульфата никеля семиводного
Координационная
формула
сульфата никеля семиводного, учитывающая состав внутренней и внешней сферы,
такова: [Ni(H2O)6]SO4 . H2O.
Структура никелевого купороса состоит из
сульфатных групп, шести молекул воды вокруг никеля и седьмой молекулы воды.
Расстояние Ni – H2O равно 2,03
Å, H2O - H2O
2,86 Å. Сульфатная
тетраэдрическая группа характеризуется расстояниями S – O 1,52 Å, O – O 2,48 Å [5].
Ионы никеля(II) и меди(II)
отличаются также гидратацией. Известно, что по действию на структуру воды ионы
разделяются на положительно и отрицательно гидратированные [6]. Молекулы воды
вблизи Cu2+ становятся подвижнее, чем в чистой воде, то
есть вокруг ионов меди в растворе молекулы воды обмениваются чаще, чем такой
обмен происходит вокруг молекулы воды в воде. Это явление и называется
отрицательной гидратацией. Связывание ионом Ni2+ близлежащих молекул
воды раствора есть проявление положительной гидратации иона. Таким образом,
положительно гидратированные являются структуроупрочняющими, в этом случае происходит некоторое эффективное связывание
ионами ближайших молекул воды. Отрицательно гидратированные оказывают
разрушающее действие на структуру воды.
Методика эксперимента
В работе использовалась деионизированная вода с
электропроводностью 2,3 мкСм/см. Вода хранилась в герметически закрытых
полиэтиленовых бутылях. Измерение электропроводности проводилось на
кондуктометре ОК-102/1. Источником ВЧ поля служил генератор Г4-119А, выходная
мощность которого составляла 1 Вт, выходное напряжение порядка 12-14 В, рабочий
диапазон частот от 30 до200 МГц. Ячейка, в которой исследуемая вода
подвергалась электромагнитному воздействию, представляла собой тефлоновый
стаканчик объемом 20 мл, в центре которого располагался внутренний ВЧ электрод,
представляющий собой латунный стержень, помещенный в тефлоновую трубку. Вторым
ВЧ электродом служила медная фольга, плотно прилегающая к внешней части ячейки.
Вывод ВЧ электродов производился через дно ячейки. ВЧ электроды соединялись с
ВЧ генератором кабелем длинной 10 см, заканчивающимся разъемом, который
подключали к генератору. Облучение воды осуществлялось непрерывно в течение 60
минут, после чего девять облученных образцов воды выдерживались трое суток с
десятым контрольным (необлученным). Взвешивание образцов осуществлялось на
весах модификации BM 153M – II№491113.
Семиводный сульфат никеля и пятиводный сульфат
меди отдельно друг от друга измельчались в фарфоровых ступках, помещались в
фарфоровые чашки и высушивались в сушильном шкафу при температуре обезвоживания
солей – 285 ˚C
для NiSO4 и 258 ˚C для CuSO4 [7].
Растворимость сульфата никеля – 39 г в 100 мл
воды, сульфата меди – 20,2 г [7]. Для первой серии опытов в химических стаканах
вместимостью 50 мл были приготовлены десять ненасыщенных растворов каждой соли
с использованием 50 мл уже облученной воды, 14 г обезвоженного сульфата никеля
или 9 г сульфата меди. Растворы подогревались на водяной бане, перемешивание
осуществлялось пластиковой палочкой до полного растворения соли, стаканы
накрывались бумажными фильтрами красная лента. Изменения, происходившие в
образцах до выпадения кристаллов, регулярно фиксировались. Параллельно
изучалась скорость испарения воды в растворах, облученных на разной частоте.
Для последующих двух серий опытов были
приготовлены растворы с содержанием воды 25 мл, а NiSO4 – 7 г и CuSO4
– 4,5
г.
Обсуждение результатов
На графике (рисунок 4) видно, что размер
кристалловNiSO4∙7H2O варьируется для растворов, приготовленных
из облученной воды на разной частоте. Увеличение размера кристаллов наблюдается
от контрольного до образцов, облученных на частотах 30 – 60 МГц. Для частот 90
– 150 МГц наблюдается уменьшение размеров, на частоте 170 МГц – резкое
увеличение размера, на частотах 190 – 200 МГц плавное уменьшение размеров
кристаллов. Данная тенденция прослеживается в трёх сериях опыта.
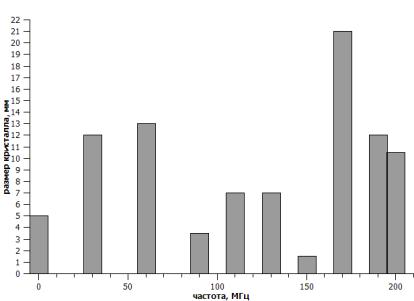
Рисунок
4 – Зависимость размера кристалла NiSO4∙7H2O от частоты облученной воды
Анализразмеров кристаллов пятиводного сульфата
меди выявил следующее: кристаллы, образовавшиеся в стаканах с частотами
облученной воды от 30 до 130 МГц, увеличиваются в размерах с увеличением
частоты. В целом, были проанализированы кристаллы трёх серий опытов, на
основании чего была выявлена тенденция к увеличению размера кристаллов с
увеличением частоты облучения раствора.
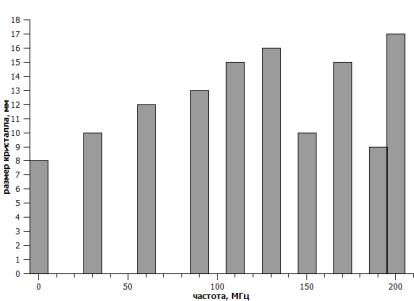
Рисунок 5 – Зависимость
размера кристалла CuSO4∙5H2O от частоты облученной
воды

Рисунок 6 – Кристалл NiSO4∙7H2O
(30 МГц; 170 МГц)

Рисунок 7 – Кристалл
CuSO4∙5H2O (150 МГц; 170 МГц)
Скорость испарения воды зависит от давления,
температуры и относительной влажности воздуха. Температура в лаборатории
величина постоянная 20 – 25 ˚C, влажность практически
не изменяется, так как работа выполняется в зимнее время года. Эксперимент по
измерению скорости испарения воды в образцах заключается в их регулярном
взвешивании, нахождении разницы в массах ∆m, расчета ∆t. А
также в построении зависимости скорости испарения воды от времени для каждого
образца.
![]() , г/ч (1)
, г/ч (1)
На кривой для NiSO4·7H2O
было выявлено, что скорость испарения воды из системы в контрольном
(необлученном) образце превышает скорости испарения облученных растворов. При
сравнении скоростей испарения облученных образцов между собой, были сделаны
выводы о том, что скорость испарения хаотично увеличивается, либо идет на спад.
Общая тенденция такова: после выпадения кристаллов, скорость испарения воды
увеличивается от 0,02 до 0,04 г/ч.
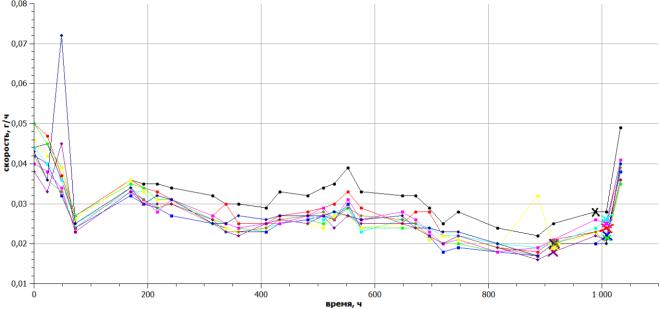
-●- – контроль; -●- –
30 МГц; -●-
– 60 МГц; -▪-
– 90 МГц; -▪-
– 110 МГц;
-▪- – 130 МГц; -▪- – 150 МГц; -♦-
– 170 МГц; -♦- – 190 МГц; -♦- – 200 МГц
Рисунок 8 –
Зависимость скорости испарения воды от времени для растворов NiSO4·7H2O
На кривой для CuSO4·5H2O
скорость испарения воды из системы в контрольном (необлученном) образце так же,
как и в случае с сульфатом никеля семиводным, превышает скорости испарения
облученных растворов. При сравнении скоростей испарения облученных образцов
между собой была выявленаобщая тенденция: после выпадения кристаллов скорость
испарения воды увеличивается на 0,005 – 0,01 г/ч для растворов, облученных на
частотах 150 – 200 МГц и необлученного образца. Для образцов, облученных на
частотах 30 – 130 МГц скорость испарения воды увеличивается на 0,035 г/ч.
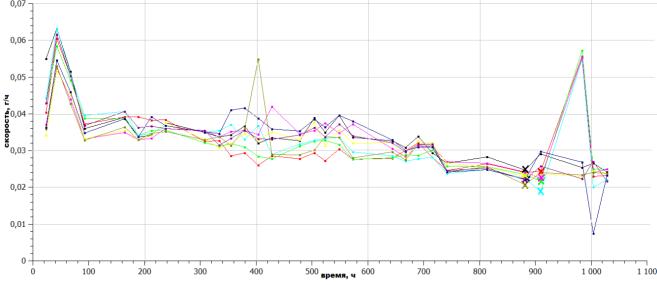
Рисунок 9 – Зависимость
скорости испарения воды от времени для растворов CuSO4∙5H2O
-●- –
контроль; -●- – 30 МГц; -●- – 60 МГц; -●-
– 90 МГц; -●- – 110 МГц;
-●-
– 130 МГц; -●- – 150 МГц; -●-
– 170 МГц; -●- – 190 МГц; -●- – 200 МГц
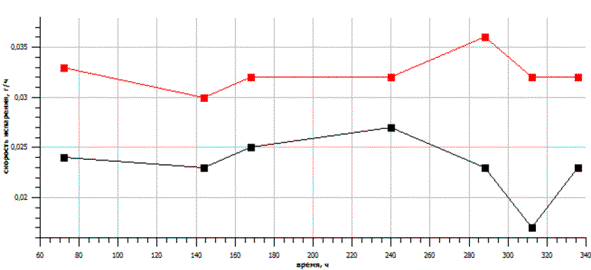
На скорость
испарения воды из растворов влияет также гидратация ионов. Для подтверждения
этого было проведено сравнение скоростей испарения воды из растворов
семиводного сульфата никеля и пятиводного сульфата меди во второй и третьей
сериях опыта.
Рисунок 10 – Скорости испарения воды из
контрольных растворов второй серии опыта-▪- – NiSO4·7H2O;
-▪- – CuSO4∙5H2O
Из-за положительной гидратации скорость
испарения воды из растворов сульфата никеля меньше, чем из растворов сульфата
меди пятиводного, что подтвердилось экспериментально. Данная зависимость
соблюдается также при сравнении скоростей испарения воды из облученных
растворов.
Выводы
Прежде всего, была выявлена тенденция к
увеличению размеров кристаллов пятиводного сульфата меди с увеличением частоты
воздействия электромагнитного поля. Для сульфата никеля семиводного наблюдается
иная закономерность: кристаллы, выращенные на облученной воде с частотами
полевого воздействия 90 – 150 МГц для трех серий опыта имеют малые размеры 1 –
7 мм.
Также была выявлена тенденция к уменьшению
скорости испарения воды из растворов NiSO4×7H2O и CuSO4∙5H2O
с ростом частоты полевого воздействия.
Также было экспериментально подтверждено влияние
гидратации ионов на скорости испарения воды из растворов NiSO4×7H2O и CuSO4∙5H2O.
В частности, отрицательная гидратация иона меди (II) способствует увеличению
скорости испарения воды по сравнению с раствором, содержащим положительно
гидратированные ионы никеля (II).
Список литературы
1.
Классен,
В.И. Омагничивание водных систем. / В.И. Классен. – М.: Химия, 1982. – 128 с.
2.
Бессонова
А.П. Влияние высокочастотного электромагнитного поля на физико-химические
свойства воды и ее спектральные характеристики / А.П. Бессонова, И.Е. Стась //
Ползуновский вестник. – 2008 – №3. – C. 305–309.
3.
Dr. Navid Qureshi Experiment M2.6
Electron Spin Resonance / Dr. Navid Qureshi // Advanced Experiments – II
Physikalisches Institut, Universitдt zu Köln
4.
Schlappa J.
Fortgeschrittenenpraktikum / J. Schlappa, R. Rückamp // Advanced
Experiments – II Physikalisches Institut, Universitдt zu Köln
5.
Beevers C.A. The Crystal Structure
of Nickel Sulphate Heptahydrate NiS04×7H20. / C.A. Beevers, C.M. Schwartz. – Manchester
6.
Самойлов
О.Я. Структура водных растворов электролитов и гидратация ионов. / О.Я.
Самойлов. – М.: Академия наук СССР, 1957. – 173с.
7.
Химическая
энциклопедия : в 5 т. / под ред. И.Л. Кнунянц. – М.: Советская энциклопедия.,
1990. – 2 т.
8.
Зацепина
Г.Н. Свойства и структура воды. / Г.Н. Зацепина. – М.: МГУ, 1974. – 168 с.
9.
Карякин
А.В. Состояние воды в органических и неорганических соединениях. / А.В.
Карякин, А.Г. Кривенцова. – М.: Наука, 1973. – 176 с.
10.
Кульский
Л.А. Вода знакомая и загадочная. / Л.А. Кульский, В.В. Даль, Л.Г. Ленчина. –
Радянська школа: Наука и техника, 1982
11.
Химия
и жизнь — XXI век: [Электронный ресурс]: Полнотекстовая база (электронный
журнал). – режим доступа к журн.:
http://wsyachina.narod.ru/physics/aqua_4.html
12.
Мокроусов
Г.М. Физико-химические процессы в
магнитном поле. / Г.М. Мокроусов. –
Томск: ТГУ, 1988. – 128 с.
13.
Lamb L., Turney А. Plastic yielding in ice single crystals / L. Lamb, A. Turney // Рrос. Phys.
Soc., 1999. – V. 62. – Р. 272–275.
14.
Леммлейн
Г. Г. Образование кристаллов. / Г.Г. Леммлейн – М.: Химия, 1994. – 432 c.
15.
Кульский
Л.А. Вода и ее использование в настоящем и будущем. / Л.А. Кульский. – К.:
Знание, 1977. – 48 с.
16.
Классен
В.И. Вода и магнит. / В.И. Классен. – М.: Наука, 1972. – 111 с.
17.
Hоrnig D. F. Advances in
molecular vibrations and collision dynamics // J. Chem. Phys. 1994. V. 40. Р. 3099–3108.
18.
Куртов
В.Д. Об удивительных свойствах электро-активированной воды. / В.Д. Куртов. – Киев, 2008. – 236 с.