Биологические науки/9. Биохимия
ибиофизика
Шевкун Н.А., Сяткин С.П. д.б.н., Демуров Е.А. д.м.н.
Российский
Университет Дружбы Народов (РУДН), Медицинский факультет.
117198
Россия, Москва, ул. Миклухо-Маклая, д. 8.
Цитотоксическое
действие модуляторов катаболизма полиаминов на клетки рака простаты.
Полиаминоксидазы
(ПАО) - это FAD-содержащие ферменты катаболизма полиаминов (ПА), осуществляющие
процесс окислительного дезаминирования с образованием цитотоксических продуктов
и индукторов апоптоза. Нарушения в метаболизме ПА, приводящие к повышению их
уровня и ускоренной пролиферации клеток, свойственны множеству раковых
заболеваний, в том числе раку простаты. Возрастание количества ПА в клетке при
канцерогенезе происходит преимущественно за счет снижения или практического
подавления катаболизма ПА путем окислительного дезаминирования, а не в
результате значительного возрастания синтетической активности. Таким образом,
активаторы катаболизма ПА – это потенциальные противоопухолевые агенты.
Перспективной задачей в разработке новых препаратов является направленный поиск
синтетических аналогов ПА, действующих на ключевые ферменты обмена таким
образом, чтобы скорость распада
превышала скорость синтеза, образовывались цитотоксические агенты и, в конечном
итоге, замедлялась злокачественная пролиферация.
Цель данной работы - провести скрининг
синтетических гетероциклических азотсодержащих соединений как потенциальных
модуляторов обмена полиаминов и противоопухолевых агентов. Изучаемые
оригинальные соединения относятся к группам: А – производные анилина (Таблица
1) ; Б – производные азакраун-эфиров (Таблица 2).
Определение
активности ди- и полиаминоксидаз in vitro проводили модифицированным спектрофотометрическим
методом в бесклеточной тест-системе из гомогената печени крыс линии Sprague
Dawley. Супернатант 10% гомогената печени в Tris-буфере (10000g 20 мин)
инкубировали в 96-луночных плашках 1ч при 37°С с субстратами Путресцин-2НС1,
Спермидин-3HCI или Спермин-4HCI в присутствии 100 мкМ тестируемых соединений.
Затем добавляли о-дианизидин и пероксидазу, инкубировали еще 30 мин и при 450
нм измеряли поглощение окрашенного продукта, который образуется при окислении
о-дианизидина перекисью водорода, выделяющейся в аминоксидазной реакции.
Таблица
1. Производные анилина (группа А).
|
Код |
Химическое
название |
Код |
Химическое название |
|
В1 |
3-анилино-1-фенил-пропанон-1 |
В8 |
3-(1-фенил-2-фторанилино)-пропанон-1 |
|
В2 |
1-фенил-3-(4-толуидино)-пропанон-1 |
В9 |
3-(3-трифторметиланилино)-1-фенилпропанон-1 |
|
В3 |
3-(4-этиланилино)-1-фенилпропанон-1 |
В10 |
3-(3-хлоранилино)-1-фенилпропанон-1 |
|
В4 |
3-(4-изопропиланилино)-1-фенилпропанон-1 |
В11 |
3-(3-нитроанилино)-1-фенилпропанон-1 |
|
В5 |
3-(4-хлоранилино)-1-фенилпропанон-1 |
В12 |
Этиловый эфир
4-(3-оксо-3-фенилпропиламино) бензойной кислоты |
|
В6 |
3-(4-броманилино)-1-фенилпропанон-1 |
В13 |
3-(3-ацетиланилино)-1-фенилпропанон-1 |
|
В7 |
3-(4-иоданилино)-1фенилпропанон-1 |
В14 |
3-(2-хлоранилино)-1-фенилпропанон-1-гидразон |
Таблица
2. Производные азакраун-эфиров (группа Б).
|
Код
|
Химическое
название |
Код |
Химическое название |
|
Х1 |
23-Аллил-8,11,14-триокса-25-азатетрацикло[19.3.1.02,7.015,20]пентакоза-2,4,6,15(20),16,18-гексаен-23-тион |
Х11 |
1,4-бис(-8,11,14-триокса-25-азатетрацикло [19.3.02,7.015,20]пентакоза-1(25),2,4,6,15(20),16,18,21,23-нонаен-23-ил)
бензол |
|
Х2 |
23-Метил-8,11,14-триокса-25-азатетрацикло[19.3.1.02,7.015,20]пентакоза-2,4,6,15(20),16,18-гексаен-23-тион |
Х13 |
7-(2-гидроксифенил)-1-(2-гидроксифенилметиленимино)-8,9-дифенил-2-окса-6-аза-3,4-бензобицикло[3.3.11,5]нонан |
|
Х3 |
23-циано-8,11,14-триокса-22,24,25-триазатетрацикло[19.3.1.02,7.015,20]пентакоза-2,4,6,15(20),16,18-гексаен-23-он |
Х14 |
22,24-дифенил-8,11,14-триокса-25-азатетрацикло[19.3.1.02,7.015,20]пентакоза-2,4,6,15(20),16,18-гексаен-23-ол |
|
Х4 |
8,11,14-Триокса-25-азатетрацикло
[19.3.1.02,7.015,20]
пентакоза-2,4,6,15(20),16,18-гексаен-23-тион |
Х15 |
2,6-Ди(2-гидроксифенил-3,5-дифенилпиперидин-4-ол |
|
Х5 |
23-Имино-8,11,14-триокса-25-азатетрацикло[19.3.1.02,7.015,20]пентакоза-2,4,6,16,18-гексаен |
Х16 |
2,6-Ди(4-гидроксифенил)-3,5-дифенилпиперидин-4-он |
|
Х6 |
23-оксо-8,11,14-триокса-22,25-диазатетрацикло[19.3.1.02,7.015,20]пентакоза-2,4,6,15(20),16,18-гексаен-24-карбокcамид |
Х17 |
23-β-Пиридин-8,11,14-триокса-25-азатетрацикло [19.3.02,7.015,20]пентакоза-1(25),2,4,6,15(20),16,18,21,23-нонаен |
|
Х7 |
2,6-Ди(4-гидрокси-5-нитрофенил)-3,5-дифенилпиперидин-4-он |
Х18 |
2,6-Ди(2-гидроксифенил-3,5-дифенилпиперидин-4-он |
|
Х9 |
7-(2-гидроксифенил)-1-(2-гидроксифенилметиленимино)-8-(4-гидрокси)фенил-2-окса-6-аза-3,4-бензобицикло[3.3.11,5]нонан |
Х19 |
16,20-Имино-16H-дибензо[h,o][1,4,7]триоксациклогексадецин-17,19-дикарбоновой
кислоты-6,7,9,10,17,18,19,20-октагидро-8-оксо-диметиловый эфир |
|
Х10 |
(2E,25E)-11,14,17,33,36,39-гексаоксапентацикло[38.4.0.0^{5,10}.0^{18,23}.0^{27,32}]тетратетраконта-1(40),2,5(10),6,8,18,19,21,25,27,28,30,41,42-тетрадекаен-4,24-дион |
Х20 |
Этил
23-оксо-8,11,14-триокса-25-азатетрациклопентакозагексаен-22-карбоксилат |
Производные
анилина (группа А), активизирующие окислительное дезаминирование сразу по трем
субстратам (Пут, Сд, См): В4, В5, В6, В8, В9 и В14. При этом наибольший эффект
получен для См – среднее превышение над контролем в 2.3 раза (Рис.1).
*



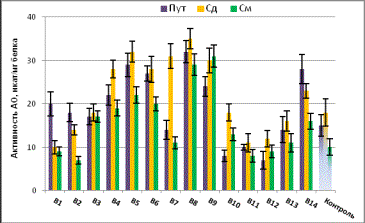
Рис.1 Влияние
производных анилина на аминоксидазную активность.

 Производные
азакраун-эфиров проявили себя как активаторы и ингибиторы аминоксидазной
активности. Окислительное дезаминирование увеличивается при действии Х9, Х13,
Х15, Х18 и Х20. При этом наибольшая активность отмечается в отношении См.
Активность аминоксидаз значительно ингибируется веществами Х1, Х2, Х4, Х10, Х11
(Рис.2).
Производные
азакраун-эфиров проявили себя как активаторы и ингибиторы аминоксидазной
активности. Окислительное дезаминирование увеличивается при действии Х9, Х13,
Х15, Х18 и Х20. При этом наибольшая активность отмечается в отношении См.
Активность аминоксидаз значительно ингибируется веществами Х1, Х2, Х4, Х10, Х11
(Рис.2).

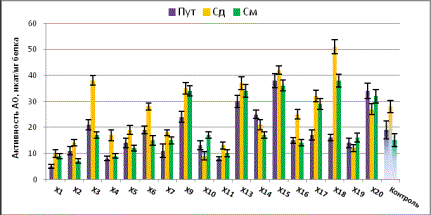
Рис.2 Влияние
производных азакраун-эфиров на аминоксидазы.
Для
оценки влияния тестируемых веществ на пролиферацию клеток рака простаты линии
PC-3 клетки за 24 ч до добавления веществ были посажены в 96-луночные плашки в
концентрации 5 тыс. на лунку. Инкубировались 72 ч с изучаемыми веществами в
среде DMEM. Контрольные лунки содержали 0,5% ДМСО. Количество живых клеток
определяли после 5 ч инкубации с 50 мкМ нефлуоресцентным красителем Аламар Блю
(резаруцин), который при восстановлении в метаболически-активных клетках
превращается во флуоресцентный продукт резоруфин. Уменьшение флуоресценции
(Ex535/Em585 нм) в присутствии тестируемого вещества пропорционально количеству
живых клеток и использовалось для измерения цитотоксичности.
По
результатам скрининга найдены ингибиторы пролиферации раковых клеток. Вещества
с более чем 30%-м подавлением роста клеток рака простаты РС-3: В1, В8, В13, В14
из группы А; Х1, Х13, Х14, Х19 из
группы Б.
Литература:
1.
Сяткин С.П., Березов Т.Т., Фролов В.А., Голомазова
К.А., Левов А.Н., Шевченко А.А., Федорончук Т.В. Прогноз канцерогенных и
противоопухолевых свойств производных бензимидазола и азафлуорена // Вестник
РУДН. – 2007, 6:70-73.
2.
McCloskey D., Woster
P., Casero, Jr R. et al. Effects of the polyamine analogues
N1-Ethyl-N11-((cyclopropyl)methyl)-4,8-diazaundecane and
N1--Ethyl-N11-((cycloheptyl)methyl)-4,8-diazaundecane in human prostate cancer
cells // Clin Cancer Res. – 2000.
– №6. – p. 17-23.