Д.с.-х.н,
к.т.н., профессор Иванова Т.А.,
Великолукская
государственная сельскохозяйственная академия Россия;
К.с.-х.н.,
доцент Керечанина Е.Д.,
Великолукский
филиал Петербургского государственного
университета путей сообщения, Россия
Экстракция
Жидкостную экстракцию применяют для
очистки сточных вод, содержащих фенолы, масла, органические кислоты, ионы
металлов и др. Экстракция может быть экономически выгодным процессом, если
стоимость извлекаемых веществ компенсирует все затраты на его проведение. В
общем случае для большинства веществ можно считать, что при концентрации выше
3-4 г/л их рациональнее извлекать экстракцией, чем адсорбцией. При концентрации
меньше 1 г/л экстракцию следует применять только в особых случаях. Очистка
сточных вод экстракцией состоит из трех стадий. Первая стадия – интенсивное
смешение сточной воды с экстрагентом (органическим растворителем).
В условиях развитой поверхности контакта
между жидкостями образуются две жидкие фазы. Одна фаза ‒ экстракт
содержит извлекаемое вещество и экстрагент, другая ‒ рафинат содержит
сточную воду и экстрагент. Вторая стадия - разделение экстракта и рафината;
третья стадия ‒ регенерация экстрагента из экстракта и рафината.
Экстрагент должен отвечать следующим требованиям: 1) растворять извлекаемое
вещество значительно лучше, чем вода, т. е. обладать высоким коэффициентом
распределения; 2) обладать большой селективностью растворения; 3) иметь низкую
растворимость в сточной воде и не образовывать устойчивых эмульсий; 4)
значительно отличаться по плотности от сточной воды (обычно она меньше),
поскольку только достаточная разность плотностей обеспечивает быстрое и полное
разделение фаз; 5) обладать большим коэффициентом диффузии; 6) регенерироваться
простым и дешевым способом; 7) иметь небольшую теплоту испарения и небольшую
теплоемкость; 8) не взаимодействовать с извлекаемым веществом; 9) по возможности
не быть вредным, взрыво- и огнеопасным, не вызывать коррозию аппаратов; 10)
иметь небольшую стоимость.
Экстрагент должен равномерно
распределяться в объеме сточной воды. Скорость подачи экстрагента в сточную
воду должна быть минимальной. Она зависит от степени очистки и коэффициента
распределения, который выражается отношением растворенного вещества в
экстрагенте и в воде. Коэффициент распределения зависит от природы компонентов
системы, содержания примесей в воде и экстрагенте, температуры. Это соотношение
справедливо, если экстрагент совершенно нерастворим в сточной воде. Однако
экстрагент частично растворим в сточной воде, поэтому коэффициент распределения
будет зависеть не только от температуры, но и от концентрации извлекаемого
вещества в рафинате.
При содержании в сточной воде нескольких
примесей целесообразно извлекать экстракцией сначала один из компонентов –
наиболее ценный или токсичный, а затем, если это необходимо, другой и т. д. При
этом для каждого компонента может быть разный экстрагент. Необходимость
извлечения экстрагента из экстракта связана с тем, что его надо вновь вернуть в
процесс экстракции. Регенерация может быть проведена с применением вторичной
экстракции с другим растворителем, а также выпариванием, дистилляцией, осаждением.
Не проводить регенерацию экстрагента можно в случае, если нет необходимости
возвращать его в цикл. Так как совершенно нерастворимых в воде жидкостей нет,
то в процессе экстракции часть экстрагента растворяется в сточной воде,
становится новым ее загрязнителем, поэтому необходимо удалять экстрагент из
рафината. Наиболее распространенным способом извлечения растворителя из
рафината является адсорбция или отгонка паром (газом). Для этой цели
целесообразно использовать отработанный пар или отходящие дымовые газы. Для
очистки сточных вод наиболее часто применяют процессы противоточной
многоступенчатой экстракции и непрерывной противоточной экстракции.
Схема многоступенчатой экстракционной
установки представляет собой батарею смесителей и отстойников (рис.). Каждая
ступень состоит из смесителя воды с экстрагентом и отстойника. Свежий
экстрагент и сточная вода поступают с противоположных сторон. В первой ступени
сточная вода с небольшим содержанием примесей перемешивается со свежим
экстрагентом, а в последней ступени исходная сточная вода смешивается с экстрагентом,
который уже содержит значительное количество извлекаемого вещества. Такое
движение потоков способствует созданию большой движущей силы процесса
экстракции и эффективной очистке сточных вод.
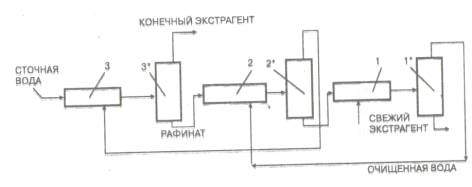
Рис. Схема многоступенчатой
противоточной экстракции:
1-3 - смесители; 1* - 3* - отстойники
Для экстракции фенолов из сточных вод
применяют простые и сложные эфиры. Простые эфиры: диэтиловый, дибутиловый,
диизо-проловый; сложные эфиры: этилацетат, н-амилацетат, изо-бутилацетат;
изо-амилацетат. Подсмольные воды полукоксования бурых углей очищаются
экстракцией фенсольваном, либо трикрезилфосфатом. Фенсольван ‒ смесь
сложных алифатических эфиров, трудно растворим в воде, но обладает высокой
растворяющей способностью по отношению к фенолам. После регенерации экстракционная
способность фенсольвана восстанавливается полностью. Нитропродукты экстрагируют
бензолом. В процессе экстракции азотная кислота нитрует бензол и ее
концентрация в сточных водах снижается до 0,01-0,03%. Экстракцию проводят в
двухступенчатой установке. Экстракт идет на ректификацию. После ректификации
бензол возвращают на повторное использование, а выделенные нитропродукты
(кубовый остаток) перерабатывают в готовую продукцию.
Жидкостная экстракция используется для
извлечения металлов из
сточных вод. В процессе жидкостной экстракции извлекаемые из сточной воды
металлы переходят в органическую фазу, затем в результате реэкстракции ‒
из органической фазы в водный раствор. Таким образом, достигается очистка
сточных вод и концентрирование металла, т.е. создаются условия для его
рекуперации. Органическая фаза содержит экстрагент и органическую жидкость
‒ растворитель экстрагента (керосин, бензол, хлороформ, толуол). В
качестве экстрагентов используют органические кислоты, эфиры, спирты, кетоны,
амины, а реэкстрагентов ‒ водные растворы кислот и оснований.
Извлечение металлов из водной в
органическую фазу проводят тремя способами: 1) катионообменной экстракцией, т.
е. обменом экстрагирующегося катиона металла на катион экстрагента; 2)
анионообменной экстракцией, т. е. обменом металлосодержащегося в воде аниона на
анион экстрагента; 3) координационной экстракцией, при которой экстрагируемое
соединение образуется за счет донорно-акцепторной связи между молекулой или
ионом экстрагента и атомом (ионом) экстрагируемого металла.
Катионообменная экстракция в общем виде
описывается уравнением
![]()
![]() МеZвод +zHRорг
МеRz орг + zH+
МеZвод +zHRорг
МеRz орг + zH+
где Me
‒ металл валентностью z; R —
кислотный остаток органической кислоты.
Катионообменными экстрагентами являются
кислоты жирного ряда типа RCOOH (например, карбоновые кислоты) с числом углеродных атомов в
радикале от 7 до 9 (С7 ‒ С9) и нафтеновые кислоты,
которые получают из сырой нефти.
Разновидностью катионообменной экстракции
является экстракция комплесксообразуюшими (хелатообразующими) экстрагентами. В
этом случае экстракция происходит в результате ионного обмена и координации
экстрагента с атомом (ионом) экстрагируемого металла с образованием
внутрикомплексных соединений.
В процессах анионообменной экстракции в
качестве экстрагентов используют амины первичные RNH2; вторичные R2NH и третичные R3N (R
‒ С7 ‒ С9). В аминах азот имеет неподеленную пару электронов, что дает
возможность образовывать координационные соединения:
R3N + HCI → [R3NH]CI
образующиеся при обработке кислотой соли аминов могут
обменивать анион кислоты на металлсодержащие анионы, например
![]()
![]() 2[R3NH]Cl
+ MeCl62- [R3NH]2 MeCl6
+ 2Cl-
2[R3NH]Cl
+ MeCl62- [R3NH]2 MeCl6
+ 2Cl-
В щелочной среде амины могут находиться не
в виде солей, способных обменивать анион, а в виде нейтральных молекул, поэтому
их применяют только в кислых средах.
Еще одним классом анионообменных
экстрагентов являются четвертичные аммониевые основания (ЧАО) и их соли (ЧАС).
ЧАО являются производными иона аммония (NH4) +: R4NOH.
Наиболее употребимы такие ЧАС, как
триалкилбензиламмонийхлорид (C6H5CH2R3N)Cl
(сокращенно «табах»); триалкилметиламмонийхлорид (CH3R3N)Cl
(«тамах»); тетраалкиламмонийхлорид (R4N)Cl
(«таах»), где R – СnН2n+1, n = 8 – 10.
ЧАС экстрагируют металлы только по типу реакции анионного
обмена:
![]()
![]() mMeXz + z[R4N]mY m [R4N]x
MeX + zYm–
mMeXz + z[R4N]mY m [R4N]x
MeX + zYm–
где
z
– заряд металлсодержащего аниона МеХ; т –
заряд аниона ЧАС; Y – анион ЧАС.
ЧАС способны экстрагировать металлсодержащие соли из кислых
и щелочных растворов.
К нейтральным экстрагентам относятся: 1) органические спирты
общей формулы ROH (в углеродном радикале от 7 до 9
атомов углерода); 2) кетоны R2CO,
из которых наиболее широко используют метилизобутилкетон (гексон) СН3СОС4Н9;
3) простые эфиры R2О
[диэтиловый эфир (С2Н5)2О]; 4) сложные эфиры,
образующиеся при взаимодействии спиртов с неорганическими кислотами, например,
трибутилфосфат –ТБФ (С4Н9О)3РО; 5)
триалкилфосфиноксид R3PO; 6) сульфоксид R2SO.
Все эти экстрагенты имеют группы, содержащие кислород и
являются полярными. Экстракция диэтиловым эфиром проходит по оксониевому типу.
Сущность подобных реакций состоит в том, что ион водорода в водных
сильнокислотных растворах образует комплексный устойчивый ион – оксоний Н3О+:
Н2О + Н+ = [Н2О
→ H] +
Стрелкой обозначена координационная связь.
Такие же комплексные положительно заряженные ионы образует
ион водорода с органическими веществами, содержащими кислород:
R2O + H+ = [R2O → H]+.
Металл экстрагируется в виде комплексного аниона, например
H[FeCl4] + R2O = [R20 → H] [FеCl4].
Нейтральные экстрагенты могут экстрагировать и катионы
металлов в случае непосредственного
присоединения полярной группы молекулы экстрагента к катиону (сольватный тип
взаимодействия), например, экстракция трибутилфосфатом (ТБФ):
![]()
![]() Ме2+ + 2NO3– + 2ТБФ 2ТБФ · Мe(NO3)2.
Ме2+ + 2NO3– + 2ТБФ 2ТБФ · Мe(NO3)2.
Коэффициент распределения определяется по соотношению
Кр = сMe орг /сMe вод,
где сMe орг и сMe вод – равновесные
концентрации металла соответственно в
органической и водной фазах. На
практике Кр ≥ 0,3 – 0,5.
Селективность (избирательность) экстрагента по отношению к
целевому металлу для данной пары металлов является коэффициентом разделения:
βМе1 / Ме2 = Кр1 / Кр2.
На практике используют экстракционные системы с β > 2. При
меньших значениях β возрастает
число ступеней экстракции.
В таблице указаны экстрагенты, которые
можно применять для извлечения цветных, редких и благородных металлов.
Таблица. Экстрагенты для извлечения
металлов.
|
Экстрагент |
Группы
периодической системы элементов |
|||||||
|
I |
II |
III |
IV |
V |
VI |
VII |
VIII |
|
|
ТБФ |
Au |
Ca, Sr, Ba Cd, Hg |
Sr, V, Ga, In |
Zr, Hf |
– |
Se, Te |
– |
Fe, Pt-эле- менты |
|
Алкилфосфор- ные кислоты |
Cu, Na, Cs |
Mg, Ba |
Sc,V, La, In |
Zr, Hf |
As, Sb |
Mo |
– |
Co, Ni |
|
Жирные и нафтеновые кислоты |
Cu, Ag |
Mg, Ca, Zn, Cd, Hg |
Al, Ga |
Pb |
Bi |
– |
– |
Fe, Ni |
|
Пиридиноксиды, оксиды аминов |
Ag |
Zn |
– |
Zr, Hf |
Nb,Ta |
Mo,W |
– |
Fe, Co, Ni |
|
Хлорекс |
Au |
Zn |
Ga, Ti |
Ge |
– |
– |
– |
Pd |
|
Амины |
Au |
Be, Zn, Cd |
– |
– |
V |
Mo,W, Se |
Mn, Re |
Fe, Co,Ni, Pt-элементы |
Таким образом, природа ‒ целостная
система с множеством сбалансированных связей. Нарушение этих связей приводит к
изменениям в установившихся в природе круговоротах веществ и энергии.
Литература:
1. Иванова Т.А., Воскресенский А.М., Кучинская
Е.А. Базовые модели переработки
полимерных и природных высокомолекулярных материалов. – СПб, В.Луки, 2003. –
192 с.
2. Иванова Т.А. Химия. Окружающая среда и техника ее
защиты. В.Луки, 1999. – 228 с.