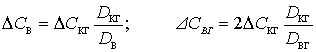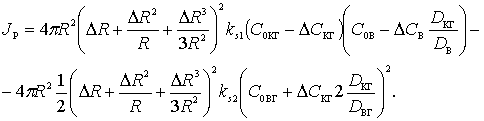к.ф-м.н. Козенков О.Д., аспирант Косырева Л.Г.
Воронежский государственный технический университет,
Воронежский государственный университет инженерных
технологий.
МОДЕЛЬ РОСТА НИТЕВИДНОГО КРИСТАЛЛА
ЛИМИТИРУЕМОГО ОБРАТИМОЙ ГЕТЕРОГЕННОЙ
ХИМИЧЕСКОЙ РЕАКЦИЕЙ НА ГРАНИЦЕ
ЖИДКОСТЬ-ГАЗ
Скорость роста нитевидного кристалла (НК)
определяется скоростью доставки кристаллизующегося вещества. Обычно процесс
роста включает стадию химической реакции. Скорость гетерогенной химической
реакции определяется диффузионной доставкой исходных веществ, отводом продуктов
реакции и химической реакцией на границе раздела фаз, проходящей по схеме [1]:
|
КГ2(Г) +
В2(Г)
↔ 2ВГ(Г) +
К(Ж) |
(1) |
КГ – химическое соединение кристаллизующегося вещества;
В – восстановитель; ВГ – продукт реакции; К – кристаллизующееся вещество.
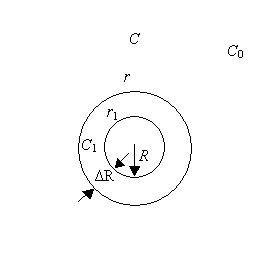
Для случая роста лимитируемого обратимой
гетерогенной химической реакцией на границе жидкость-газ предложена следующая модель
(рисунок1).
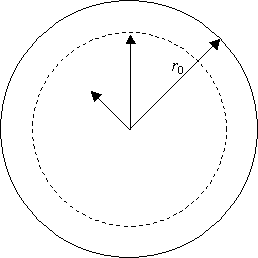
Предположим, что поверхность жидкой фазы
сферическая. Тогда вокруг жидкости в газовом потоке формируется пограничный
слой размером r0 за пределами
которого концентрация реагентов (1) равна их концентрации в объеме С0. В пределах пограничного
слоя от r0 до r1 происходит диффузионная доставка исходных веществ и
отвод продуктов реакции. Предположим, что в пределах шарового слоя толщиной
ΔR концентрация реагентов в газовой фазе постоянна и
определяется с одной стороны скоростью диффузионных процессов, а с другой
стороны скоростью химической реакции. При этом должно выполняться условие равенства
суммы диффузионных потоков исходных веществ сумме диффузионных потоков
продуктов реакции [2], которые связаны между собой условием стехиометрии реакции
(1).
|
|
(2) |
где JКГ – поток
химического соединения кристаллизующегося вещества, JВ – поток
восстановителя, JВГ – поток
кристаллизующегося вещества.
|
|
|
Рисунок 1 – Схема модели роста НК |
В стационарном режиме устанавливаются
некоторые постоянные значения концентраций реагентов в слое ΔR (С1КГ, С1В, С1ВГ), как
результат равенства диффузионных потоков (2) потоку химической реакции (1), который
приводит к изменению концентраций реагентов и к росту НК.
Обозначим: С0КГ – С1КГ =
ΔСКГ – убыль
концентрации химического соединения кристаллизующегося вещества в процессе
диффузии от границы r0 до
границы r1; С0В – С1В = ΔСВ – убыль концентрации восстановителя
в процессе диффузии от границы r0 до
границы r1; С0ВГ – С1ВГ = –
2ΔСВГ – убыль
концентрации продуктов реакции в процессе диффузии от границы r1 до границы r2.
Диффузионный поток определяется только величиной
ΔС, следовательно:
|
|
(3) |
где DКГ, DВ, DВГ – соответствующие коэффициенты диффузии.
Поток кристаллизующегося вещества, запишем
в виде разности потоков прямой и обратной химической реакции:
|
|
(4) |
Из стехиометрии реакции (1) следует связь
потока JР с
диффузионными потоками:
|
|
(5) |
Следовательно, можно определить ΔСКГ, ΔСВ и ΔСВГ и скорость роста НК.
Литература
1. Гиваргизов Е.И. Рост нитевидных и
пластинчатых кристаллов из пара / Е.И. Гиваргизов. – М.: Наука, 1977. – 304с.
2. Поляков Ю.И. Кинетика пиролиза летучих
соединений металлов при нанесении покрытий в вакууме / Ю.И. Поляков, Г.Н.
Картмазов, Ю.В. Лукирский, С.Г. Руденький, Л.А. Ферлий // Вопросы атомной науки
и техники. Серия: Физика радиационных повреждений и радиационное материаловедение.
2011. - № 2. – С. 163 – 167.