Медицина/6. Экспериментальная и клиническая фармакология
Политкина С.Н., д.ф.н.
Кондратенко С.Н., д.м.н. Стародубцев А.К.,
к.м.н. Сеник Е.А.
ГБОУ ВПО Первый
Московский государственный медицинский университет им. И.М. Сеченова, г. Москва,
Россия
Динамика распределения
левофлоксацина
в
слюне здоровых добровольцев
Группа фторхинолонов – антибиотики широкого спектра активности на
грамположительные, грамотрицательные, аэробные и внутриклеточные бактерии. Для
препаратов группы фторхинолонов характерна высокая абсолютная биодоступность,
которая достигает 80–100%. Фторхинолоны
хорошо проникают в биологические ткани и жидкости, в том числе и в слюну. Степень
проникновения фторхинолонов в слюну зависит от различных факторов: физико-химических
свойств лекарственного средства (показатель кислотности Рка, степень
ионизации молекулы, липофильность), индивидуальных особенностей больных
(например, наличие хронических респираторных заболеваний) и способа отбора проб
слюны [1, 5, 6]. Для некоторых фторхинолонов доказана возможность проведения
лекарственного мониторинга и изучения их фармакокинетики по динамике
распределения в слюне [2, 5, 6]. Однако
особенности распределения левофлоксацина в слюне пациентов не исследованы.
Поэтому представлялось актуальным изучить динамику распределения левофлоксацина
в слюне здоровых добровольцев после однократного перорального приема.
Материалы и методы исследования
В фармакокинетическое исследование были включены 6 здоровых
добровольцев-мужчин, средний возраст
составил 21,3 лет; рост 175,5 см; вес 70,5 кг.
Добровольцы принимали однократно препарат Таваник® («Санофи
Винтроп Индустрия», Франция) в дозе
500 мг внутрь натощак.
Стандартный завтрак разрешался
через 3 часа после приема препарата.
После приема препарата, пищи и напитков добровольцы тщательно прополаскивали
рот водой. Отбор проб слюны осуществлялся без стимуляции слюноотделения в пластиковые пробирки в количестве 2–3
мл до и через 0.25, 0.5, 1.0, 1.5, 2.0, 3.0, 4.0, 5.0, 6.0, 8.0, 10.0, 12.0 и
24.0 часа после приема препарата.
Количественное определение левофлоксацина в
слюне проводили методом ВЭЖХ. За основу была
выбрана методика количественного определения офлоксацина в плазме крови
человека Soledad С. Flor с соавторами [4], которая была модифицирована. Левофлоксацин из слюны
(0,5 мл) экстрагировали хлороформом (5 мл) при рН=7 (0,5 мл фосфатного буфера).
После центрифугирования водный слой отбрасывали, а органическую фазу упаривали
досуха на роторном испарителе под вакуумом. Сухой остаток растворяли в элюенте,
аликвоту (50 мкл) наносили на колонку.
Анализ проводили на
высокоэффективном жидкостном хроматографе "Hewlett-Packard" (США) с УФ-фотометрическим детектором с переменной длиной
волны Series 1050 при длине волны 310 нм и аттенюации 4.
Использовалась хроматографическая колонка µBondapakТМ С18, 10 µm, 3,9x150 mm («Waters»,
США). Элюирование проводили мобильной фазой, состоящей из ацетонитрила и фосфатного
буферного раствора в объёмном соотношении 19:81, доведенной до рН=3 орто-фосфорной
кислотой. Разделение проводили при комнатной температуре, скорость элюирования
составляла 1 мл/мин, время удерживания левофлоксацина – 5,9 ± 0,2 мин. Количественное определение левофлоксацина
в слюне проводили методом абсолютной калибровки.
Статистическая
обработка полученных результатов проводилась с помощью программы EXCEL. Рассчитывались следующие статистические
параметры: среднее арифметическое значение (Mean), стандартное отклонение среднего результата (S.D.), стандартная ошибка (S.E.), коэффициент вариации (C.V.).
Результаты и обсуждение
Динамика
индивидуальных значений концентрации левофлоксацина в слюне здоровых
добровольцев после однократного перорального приема препарата Таваник® в дозе
500 мг представлена на рис. 1, динамика усредненных значений концентрации
левофлоксацина в слюне добровольцев – на рис. 2 и в таблице.
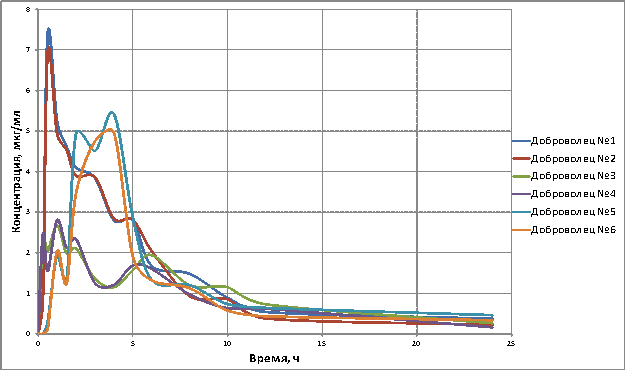
Рис. 1. Динамика
индивидуальных концентрации левофлоксацина в слюне здоровых добровольцев после однократного приема препарата Таваник®
Профили
индивидуальных фармакокинетических кривых существенно различаются: у добровольца под № 1 регистрируется один
пик концентрации левофлоксацина в слюне, добровольца под № 6 – два пика
концентрации, у добровольцев под № 2 и 5 – три подъема концентрации, у добровольцев
под № 3 и 4 – четыре пика концентрации. При этом время достижения максимальной
концентрации в слюне варьирует от 0,5 до 4 ч, а ее значение – от 2,68 до 7,40
мкг/мл. Через 24 ч после приема препарата левофлоксацин еще регистрировался в
слюне добровольцев в количестве 0,16–0,46 мкг/мл. На протяжении всего исследования наблюдался умеренный
разброс индивидуальных значений концентрации левофлоксацина в слюне
добровольцев (C.V.=17,2–58,4%), за
исключением временных точек 0,25–0,5 ч, когда коэффициент вариации был
значительно выше (98,2–107,0%).
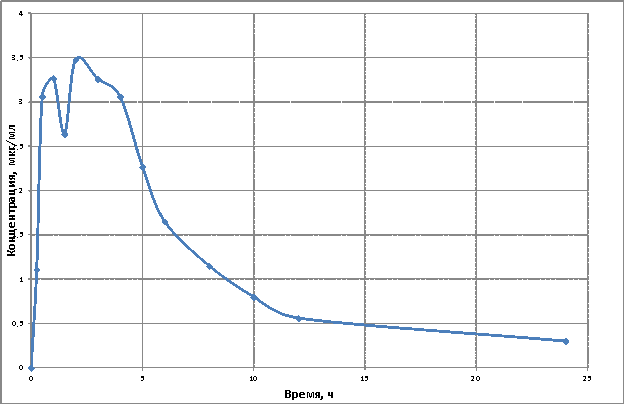
Рис. 2.
Динамика усредненных значений концентрации левофлоксацина в слюне здоровых
добровольцев после однократного приема препарата Таваник®
На усредненной фармакокинетической кривой наблюдаются два пика концентрации левофлоксацина в слюне:
через 1 и 2 ч после приема препарата (3,27±0,65 мкг/мл и 3,48±0,49 мкг/мл
соответственно). Затем наблюдается постепенное снижение уровня левофлоксацина и
через 24 ч его концентрация в слюне добровольцев составляет 0,30±0,05 мкг/мл.
Таким образом, левофлоксацин хорошо проникает в слюну: уже через 15 мин
после приема он регистрируется в слюне добровольцев в количестве 1,11±0,49 мкг/мл, максимальная концентрация в слюне достигается в
среднем через 1–2 ч после приема и составляет
3,48±0,49 мкг/мл с индивидуальным разбросом от 2,68 до 7,40 мкг/мл. Полученные результаты
согласуются с литературными данными по распределению левофлоксацина в плазме
крови добровольцев [3, 7]. Представленные
данные свидетельствуют о возможности проведения лекарственного терапевтического
мониторинга и фармакокинетических исследований левофлоксацина по динамике его
концентрации в слюне, однако необходима надежная методика, позволяющая
исключить статистически значимые ошибки, обусловленные использованием этой
биожидкости.
Таблица –
Статистические параметры, рассчитанные по индивидуальным значениям
концентрации левофлоксацина в слюне здоровых добровольцев после
однократного приема препарата Таваник® в
дозе 500 мг
|
Время, ч |
Статистические параметры |
|||
|
Mean |
S.D. |
S.E. |
C.V. |
|
|
0,25 |
1,11 |
1,09 |
0,49 |
98,2 |
|
0,5 |
3,06 |
3,28 |
1,47 |
107,0 |
|
1 |
3,27 |
1,44 |
0,65 |
44,19 |
|
1,5 |
2,64 |
1,54 |
0,69 |
58,41 |
|
2 |
3,48 |
1,09 |
0,49 |
31,21 |
|
3 |
3,26 |
1,56 |
0,70 |
47,78 |
|
4 |
3,06 |
1,81 |
0,81 |
59,12 |
|
5 |
2,27 |
0,61 |
0,28 |
27,11 |
|
6 |
1,65 |
0,30 |
0,14 |
18,33 |
|
8 |
1,15 |
0,20 |
0,09 |
17,20 |
|
10 |
0,80 |
0,21 |
0,09 |
18,23 |
|
12 |
0,56 |
0,13 |
0,06 |
23,77 |
|
24 |
0,30 |
0,11 |
0,05 |
36,20 |
Литература:
1.
Глущенко
И.А., Кондратенко С.Н., Стародубцев А.К. Сравнительная фармакокинетика
фторхинолонов и особенности их распределения в слюне. // Клиническая
фармакология и терапия. 2011. Т. 20, № 2. С. 53–58.
2.
Золкина
И.В., Кондратенко С.Н., Кабанова И.А., Стародубцев А.К. Сравнительная
фармакокинетика препаратов моксифлоксацина по динамике его распределения в
плазме крови и слюне. // Фармация. 2007. № 8. С. 30–33.
3.
Падейская Е.И.,
Яковлев В.П. Антимикробные препараты группы фторхинолонов в клинической
практике. М.: Логата, 1998. 351 с.
4. Flor S.C., Rogge M.C., Chow A.T. Bioequivalence of oral and intravenous
ofloxacin after multiple-dose administration to healthy male volunteers. //
Antimicrobial Agents and Chemotherapy. 1993. V. 37, N 7. P. 1468–1472.
5. Koizumi F. et al. Effective monitoring of concentration of ofloxacin in saliva of patients with chronic respiratory
tract infections. // Antimicrobial Agents and
Chemotherapy. 1994. V. 38, N 5. P. 1140–1143.
6.
Kozjek F., Šuturcova L.J., Antolič G.
et al. Kinetics of 4-fluoroquinolones permeation into saliva. //
Biopharmaceutical and Drug Disposition. 1999. V. 20. P. 183–191.
7. Lubasch A.,
Keller I., Borner K. et al. et al. Comparative pharmacokinetics of ciprofloxacin, gatifloxacin, grepafloxacin, levofloxacin, trovafloxacin, and
moxifloxacin after single oral administration in healthy volunteers. //
Antimicrobial Agents and Chemotherapy. 2000. V. 44, N 10. P. 2600–2603.