Медицина/14. Анастезиология и реанимация
Д.б.н.
Лескова Г.Ф.
НИИ общей патологии
и патофизиологии РАМН, Россия
МЕМБРАННЫЕ ФОСФОЛИПИДЫ В ПАТОГЕНЕЗЕ ГЕМОРРАГИЧЕСКОГО ШОКА И ЗАЩИТНЫЙ
ЭФФЕКТ ЛИПОСОМ
Коррекция клеточных повреждений является
одной из наиболее трудно решаемых проблем шоковых состояний, что создает
необходимость изучения механизмов таких повреждений с перспективой
теоретического обоснования подходов к восстановлению структуры и функций
органов-мишеней. С учетом того, что существенную роль в биохимических и физиологических процессах играют мембранные фосфолипиды (ФЛ), изучали
особенности модификации ФЛ-состава клеточных мембран при развитии
геморрагического шока (ГШ).
Исследования проведены на кошках.
Установлено, что через 30 мин от начала
кровопотери изменение ФЛ-состава синаптических мембран продолговатого мозга, лобного
отдела головного мозга и плазмалеммы клеток печени связано с падением уровня
фосфатидилинозитола (ФИ) (рис.1). Известно, что гидролиз содержащих инозитол ФЛ
тесно связан с активацией большого количества рецепторов, использующих Са2+-зависимые
пути внутриклеточной сигнализации. Полученные данные дают основание полагать,
что одним из факторов усиления компенсаторных механизмов в изученных органах на
начальном этапе развития ГШ является увеличение степени гидролиза ФИ в
синаптических мембранах и в плазмалемме клеток печени, что несомненно связано с
гиперактивацией центральной нервной системы, поскольку известно, что
ацетилхолин, норадреналин, а также вазопрессин являются активаторами обмена ФИ.
Длительное воздействие медиаторов на
постсинаптическую мембрану приводит к ослаблению чувствительности ее
рецептивных участков – десенситизации. На существование сходного механизма
ослабления чувствительности холино- и адренорецептивных участков синаптических
мембран лобных долей головного мозга на стадии развитого ГШ указывает
обогащение этих мембран ФИ, среди активаторов которого, как уже отмечалось,
рассматривают ацетилхолин и норадреналин. Накопление ФИ в плазмалемме клеток
печени в отдаленные периоды развития ГШ оказалось наиболее выраженным, свидетельствуя о глубоком повреждении
механизмов взаимодействия агонистов, стимулирующих распад ФИ, с мембранными
рецепторами клеток печени и нарушении трансмембранной сигнализации.
Рис.1.
ИЗМЕНЕНИЕ СОДЕРЖАНИЯ
ФОСФАТИДИЛИНОЗИТОЛА В СИНАПТИЧЕСКИХ МЕМБРАНАХ ГОЛОВНОГО МОЗГА ПРИ РАЗВИТИИ
ГЕМОРРАГИЧЕСКОГО ШОКА
ПРОДОЛГОВАТЫЙ МОЗГ
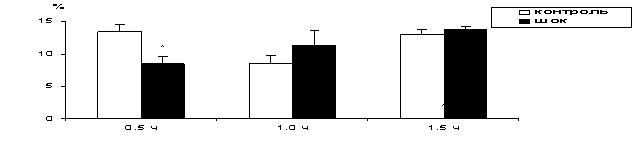
ЛОБНЫЙ ОТДЕЛ
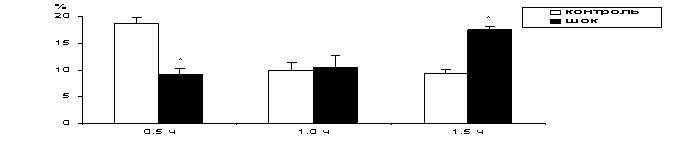
ИЗМЕНЕНИЕ СОДЕРЖАНИЯ
ФОСФАТИДИЛИНОЗИТОЛА В ПЛАЗМАТИЧЕСКИХ МЕМБРАНАХ КЛЕТОК ПЕЧЕНИ ПРИ РАЗВИТИИ
ГЕМОРРАГИЧЕСКОГО ШОКА
Здесь и на рисунках 2-4: * - P<0,05 по сравнению с контрольными показателями
Вклад в увеличение уровня мембранного
фосфатидилэтаноламина (ФЭ) на ранних
стадиях ГШ (рис. 2) может вносить усиление его обмена в связи с активным
выбросом в кровь катехоламинов и вазопрессина, являющихся активаторами синтеза
этого ФЛ. Известно, что увеличение в мембранах концентрации ФЛ, содержащих
этаноламин, сопровождается повышением активности Са2+-АТФазы. Таким
образом, накопление ФЭ в плазматических мембранах клеток печени, а также в
синаптических мембранах лобного отдела головного мозга на ранней стадии ГШ
можно оценить как компенсаторный механизм, направленный на освобождение клеток
от избытка кальция.
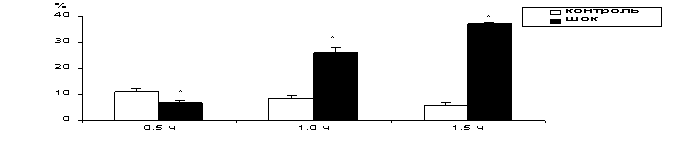
Рис. 2.
ИЗМЕНЕНИЕ СОДЕРЖАНИЯ ФОСФАТИДИЛЭТАНОЛАМИНА В ПЛАЗМАТИЧЕСКИХ МЕМБРАНАХ
КЛЕТОК ПЕЧЕНИ ПРИ РАЗВИТИИ ГЕМОРРАГИЧЕСКОГО ШОКА
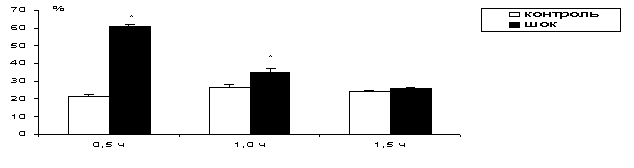
ИЗМЕНЕНИЕ СОДЕРЖАНИЯ
ФОСФАТИДИЛЭТАНОЛАМИНА В СИНАПТИЧЕСКИХ МЕМБРАНАХ ГОЛОВНОГО МОЗГА ПРИ РАЗВИТИИ
ГЕМОРРАГИЧЕСКОГО ШОКА
ЛОБНЫЙ ОТДЕЛ
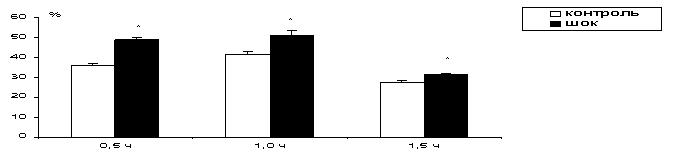
ПРОДОЛГОВАТЫЙ МОЗГ
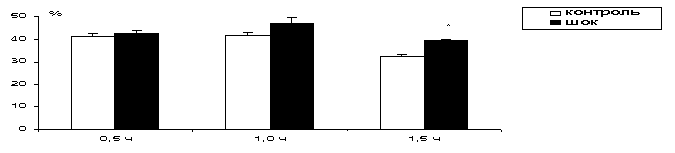
Высокий уровень мембранного ФЭ на
отдаленных стадиях ГШ не исключает возможности снижения уровня его
метилирования. Следует отметить, что процессам метилирования в ЦНС придается особое значение как важному
механизму передачи нервных импульсов, опосредованному через аминокислоты. Существует
мнение, что метилирование ФЛ является одним из инструментов, посредством
которого нервные клетки регулируют концентрацию аминокислот в синаптической
щели. Установлено, что высокий уровень метилирования ФЛ синаптических мембран
сопровождается снижением захвата возбуждающих аминокилот (ВАК) нервными
окончаниями, в то время как при низком уровне метилирования ФЛ ингибирование
захвата ВАК уменьшается, причем, имеет важность окружения молекулы-переносчика
мембраны метаболитами ФЭ для нормального функционирования системы
высокоаффинного захвата медиаторных аминокислот. Таким образом, накопление ФЭ в
синаптических мембранах головного мозга на отдаленных стадиях геморрагического
шока не исключает возможности замедления его метилирования и, как следствие, усиления
нейротоксического действия ВАК.
Следующая важная особенность модификации
ФЛ-состава изученных мембран при развитии ГШ
- истощение фосфатидилхолина (ФХ) (рис.3). Снижение содержания ФХ в
плазмалемме клеток печени наиболее выражено. На начальном этапе массивной
кровопотери это, вероятно, связано в основном с выбросом в кровь
«стресс-гормонов», являющихся агонистами, стимулируюшими распад
фосфатидилхолина, а в более позднем периоде особую значимость может приобретать
дефицит холина, приводящий к нарушению синтеза ФХ в печени.
Взаимодействие ацетилхолина с
мускариновыми рецепторами, стимуляция метаботропных глутаматных и α1-адренорецепторов
активируют фосфолипазу D – фосфодиэстеразу, гидролизующую ФХ с образованием
фосфатидной кислоты и предшественника ацетилхолина – холина. Освобождение
холина из ФХ клеточных мембран является важным для синтеза ацетилхолина в
холинергических нейронах при усилении
освобождения этого медиатора. Вместе с тем, интенсивное использование
холин-содержащих мембранных ФЛ приводит к повреждению клеточных мембран,
нарушению функций клеток и их гибели. Следовательно, специфичность изменения
структуры синаптических мембран, связанная с исчезновением ФХ, в значительной
степени определяется усилением синтеза
ацетилхолина в холинергических нейронах на фоне холинергической гиперактивации,
сопровождающей массивную кровопотерю. На стадии развитого ГШ определенное
значение может иметь нарушение синтеза этого ФЛ на фоне дефицита его деривата –
холина.
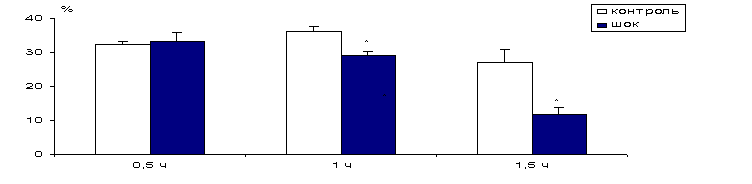
Рис.
3.
ИЗМЕНЕНИЕ
СОДЕРЖАНИЯ ФОСФАТИДИЛХОЛИНА В ПЛАЗМАТИЧЕСКИХ МЕМБРАНАХ КЛЕТОК ПЕЧЕНИ ПРИ
РАЗВИТИИ ГЕМОРРАГИЧЕСКОГО ШОКА
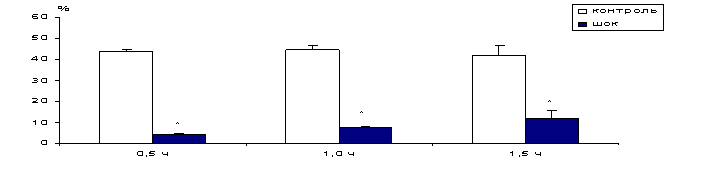
ИЗМЕНЕНИЕ
СОДЕРЖАНИЯ ФОСФАТИДИЛХОЛИНА В СИНАПТИЧЕСКИХ МЕМБРАНАХ ГОЛОВНОГО МОЗГА ПРИ
РАЗВИТИИ ГЕМОРРАГИЧЕСКОГО ШОКА
ЛОБНЫЙ ОТДЕЛ
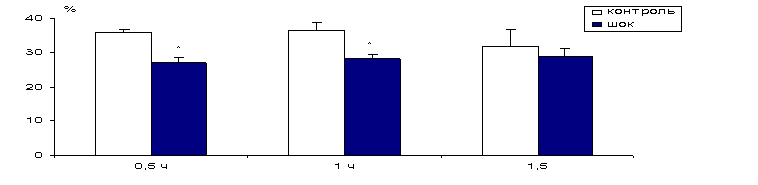
ПРОДОЛГОВАТЫЙ МОЗГ
Ацетилхолин играет исключительно важную роль
в организме, поскольку помимо воздействия на нейроны существует его прямой или
опосредованный эффект на клетки ненейронального происхождения. Считают, что
ацетилхолин может быть вовлечен в регуляцию основных клеточных функций, таких
как экспрессия генов, пролиферация, дифферентация, цитоскелетная
организация, взаимодействие клетка-клетка, капиллярная и электрическая
активность, секреция и абсорбция. Ацетилхолин контролирует неспецифические и
специфические иммунные реакции. Таким образом, повышенный уровень ацетилхолина
в крови при ГШ можно рассматривать как важный компенсаторный механизм,
направленный на устранение вызванных массивной кровопотерей повреждений. Вместе
с тем на поздних стадиях ГШ – в связи со значительным разрушением мембран, набуханием – клетки в значительной
степени теряют способность взаимодействовать с биологически активными
веществами, в том числе с ацетилхолином.
В целях коррекции структуры клеточных
мембран и нормализации холинергических воздействий на фоне ГШ животным вводили
липосомы, приготовленные из ФХ, истощение которого в клеточных мембранах
является одним из основных факторов клеточного повреждения. Липосомальная
терапия приводила к нормализации ФЛ-состава клеточных мембран печени и
головного мозга (рис. 4). Введение липосом животным в поздней стадии ГШ
повысило системное артериальное давление в среднем в течение 30 мин до 70 мм
рт.ст. (до уровня, при котором клетки
перестают разрушаться) (рис. 5). Стабилизация артериального давления на
субнормальном уровне поддерживалась в среднем в течение 4-х часов.
Продолжительность жизни таких животных в среднем составляла 8 ч, в то время как
нелеченые животные погибали в среднем в течение 80 мин.
Гистологические исследования показали
существенное облегчение патологии ряда органов. Наиболее выраженным оно
оказалось в печени (рис 6). На фоне действия липосом снизился отек легких.
В препаратах селезенки выявили
отчетливое увеличение красной пульпы, характерное для синдрома усиления
утилизационной функции этого органа. Уменьшились деструктивные изменения
нейронов коры головного мозга, сократилось количество безъядерных клеток.
Следует отметить, что липосомальный
препарат применяется в небольшом объеме и в перспективе может быть использован
для оказания первой медицинской помощи при массивной кровопотере. Его
корректирующее действие на уровне
клеточных мембран несомненно будет способствовать существенному повышению
эффективности комплексной терапии ГШ и, как следствие, снижению смертности и
инвалидности.
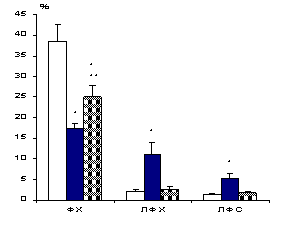
Рис. 4.
ВОЗДЕЙСТВИЕ ЛИПОСОМ НА ФОНЕ ГЕМОРРАГИЧЕСКОГО ШОКА
ВОССТАНОВЛЕНИЕ
СОСТАВА ФОСФОЛИПИДОВ ПЛАЗМАТИЧЕСКИХ МЕМБРАН КЛЕТОК ПЕЧЕНИ
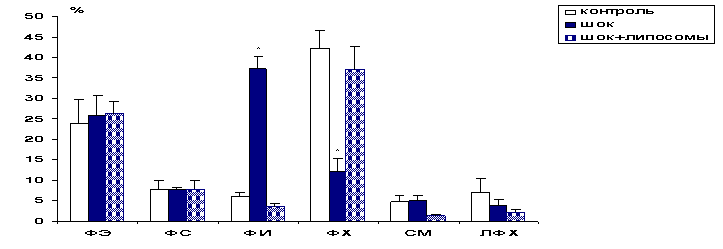
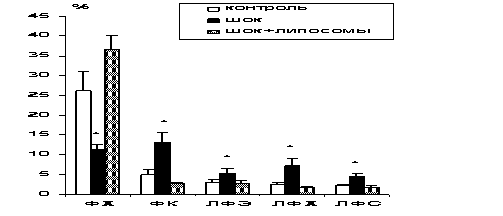
ВОССТАНОВЛЕНИЕ
СОСТАВА ФОСФОЛИПИДОВ МЕМБРАН МИТОХОНДРИЙ ЛОБНОГО ОТДЕЛА ГОЛОВНОГО МОЗГА
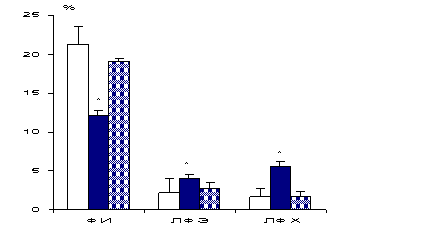
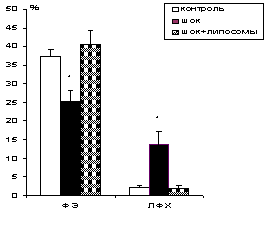
Внешние мембраны Внутренние мембраны
КОРРЕКЦИЯ
СОСТАВА ФОСФОЛИПИДОВ МЕМБРАН МИТОХОНДРИЙ ПРОДОЛГОВАТОГО МОЗГА
Внешние мембраны Внутренние мембраны
ФЭ-фосфатидилэтаноламин; ФС-фосфатидилсерин;
ФИ-фосфатидилинозитол; ФХ-фосфатидилхолин; СМ-сфингомиелин; ФК-фосфатидная
кислота; ЛФХ-лизофосфатидилхолин; ЛФЭ-лизофосфатидилэтаноламин;
ЛФС-лизофосфатидилсерин. ** -
Р<0,05 по сравнению с показателями у
нелеченых животных.
Рис.
5.
ВОЗДЕЙСТВИЕ ЛИПОСОМ СИСТЕМНОЕ АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ
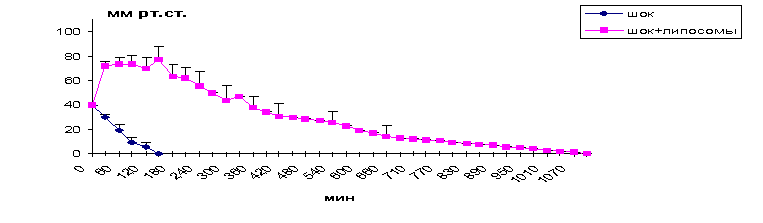
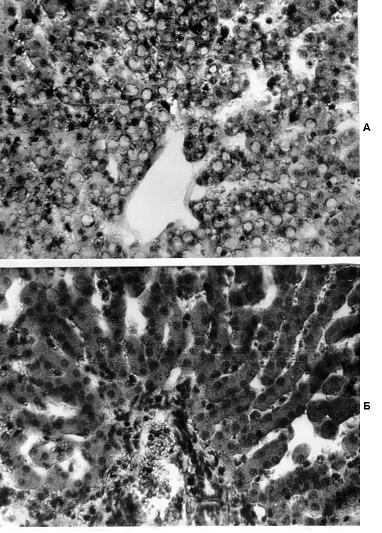
Рис. 6. Структурные изменения в печени у кошек при
геморрагическом шоке и их
коррекция липосомами
А – печень кощки. Геморрагический шок. Жировая и вакуольная
дистрофия, запустение центральных вен и синусоидов.
Б – печень кошки. Геморрагический шок + липосомы через 70 мин после
инокуляции. Отсутствие проявлений жировой и вакуольной дистрофии; уменьшение
признаков отека; в просвете синусоидов встречаются форменные элементы крови.