1Оналбаева Ж.С., 2Рыспаев Т.А., 1Самойлов
В.И., 1Хлебникова Е.Н.,
1Восточно-Казахстанский государственный технический
университет
им. Д. Серикбаева, г.
Усть-Каменогорск, Казахстан
2TU Clausthal, Clausthal-Zellerfeld, Германия
Современное состояние сернокислотной
технологии производства карбоната лития из минерального сырья
Известны сотни патентов и научных работ,
посвящённых технологии производства соединений лития. В этом объёме
исследований легко заметить желание исследователей найти новые приёмы разложения
исходного сырья наиболее дешёвыми реагентами, обеспечивающие полноту разложения
без разубоживания бедного исходного концентрата и позволяющие применять простую
и устойчивую аппаратуру. Окончательный выбор тех или иных методов переработки
литиевого сырья значительно зависит от
состава конечного товарного продукта. Например, способы, которые
наиболее простым путём приводят к получению хлорида лития, применяются в том
случае, если нужно из него получить металл; LiOH целесообразно получать
при непосредственном использовании её в промышленности, а способ, связанный с
получением сульфата лития, эффективнее, если в дальнейшем желательно иметь Li2CO3, из которого легко
получать любые соли.
Для переработки сподуменового концентрата,
который в настоящее время занимает основное место среди литиевых концентратов,
известно четыре способа: сульфатный, известковый, сернокислотный и хлорирующий
обжиг. Все они применяются в промышленности; целесообразность применения
каждого определяется экономическими соображениями [1-12].
Ориентировочный
термодинамический расчёт реакции вскрытия сподумена серной кислотой выполнен
Г.А. Ягодиным и др. [12] по этим данным, реакция разложения сподумена серной
кислотой с образованием сульфата лития:
|
Li2O·Al2O3·4SiO2
+ H2SO4 = Li2SO4 + H2O·Al2O3·4SiO2 |
(1) |
термодинамически вероятна. Разложение
концентратов путем нагревания их с концентрированной серной кислотой основано
на топохимических реакциях. Кинетика процесса определяется диффузионными
процессами подвода серной кислотой к непрореагировавшей поверхности минерала
через слой продукта реакции.
Перед реакцией с серной кислотой рудный
концентрат подвергают специальной термической обработке для перевода минералов
в более реакционную форму. При этом изменяется термодинамическая характеристика
вскрываемого материала и увеличивается его поверхность. Сподуменовый концентрат
перед сульфатизацией подвергают декрипитации. Сернокислотный способ разложения
α-сподумена без предварительной подготовки минерала не даёт хороших
результатов; извлечение лития достигает 4–5
%. Однако при обработке β-сподумена серной кислотой в количестве 130–140 % от стехиометрического при 250 °С
происходит замещение ионов лития водородом. Впервые этот способ был предложен в
1950 г. Эллестедом и Льюте. Источником ионов водорода является серная кислота.
Считают, что происходит ионный обмен между алюмосиликатным ядром сподумена и
серной кислотой.
В результате обработки реакционной массы водой
образуется раствор сульфата лития, β-сподумен переходит в вещество, структура
которого фактически не изменяется. В трудах [7] подтверждены эти положения.
Полнота реакции сульфатизации, видимо, связана с повышением активности
сподумена при переходе его из α- в β-модификации.
Технологическая схема сернокислотного способа
разложения сподуменового концентрата
представлена на рисунке 1. В таком варианте она используется в США.
Исходным сырьём является обогащённый сподуменовый концентрат, содержащий 3–5 % масс. оксида лития. Для получения
β-сподумена исходный концентрат
обжигают во вращающейся печи при 1100 °С. Длина печи 12,2 метра; диаметр
1,2 метра; скорость вращения 1 об/мин; производительность 1–2 т/ч. При нагревании сподумена происходит
резкое изменение свойств кристаллов исчезает
двойное лучепреломление, показатель преломления падает с 1,66 до
1,52 и происходит полный переход α-формы в β-форму.
Декрипитированный
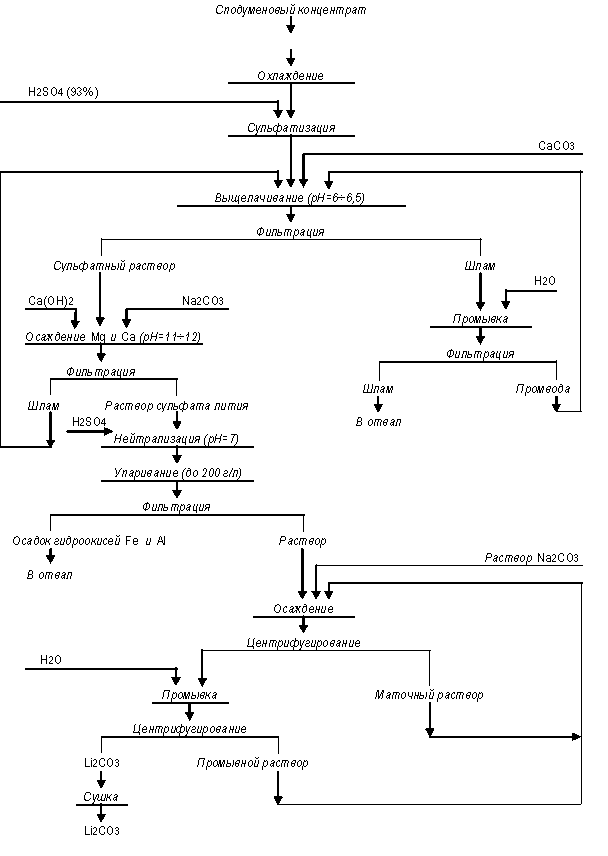
Рисунок
1 – Технологическая схема сернокислотного способа разложения сподуменового концентрата
охлажденный продукт измельчают на валковой
мельнице до -0,074 мм и смешивают измельченный концентрат с 93 % серной
кислотой на горизонтальном шнековом транспортёре. Под действием кислоты
происходит полное разложение концентрата. Сульфатизацию концентрата проводят
также во вращающейся печи, обогреваемой газом, при 250 °С. Для растворения
сульфата лития просульфатизированный продукт выщелачивают водой при перемешивании.
В этот же реактор добавляют углекислый кальций для нейтрализации избыточной
серной кислоты до рН=6,0–6,5.
Отделение нерастворимого остатка и промывки его водой проводят на барабанном
фильтре. Промывную воду возвращают на выщелачивание сульфатного продукта.
Извлечение лития на этой стадии составляет 99 %.
Чистый концентрированный раствор сульфата лития
перекачивают в реактор, где производят осаждение карбоната лития раствором соды
концентрацией 330 г/дм3 карбоната натрия при нагревании до 90 °С.
При этом происходит обменная реакция, и в твердую фазу выпадает мелкокристаллический
осадок карбоната лития, который отделяют от маточника на центрифуге и там же промывают водой. Отмытый
продукт, содержащий до 10 %
масс. влаги, сушат в вакууме в течение четырёх часов.
Как показала промышленная практика,
сернокислотным способом можно перерабатывать не только концентрат, но и
литиевые руды без предварительного обогащения. При этом извлечение соли из
воды значительно повышается.
Основные преимущества сернокислотной технологии:
1) отсутствие необходимости в измельчении руды,
так как предварительная декрипитация обеспечивает разрыхление руды, и
сульфатизация серной кислотой протекает успешно даже при крупных кусках руды;
2) нет передела смешения руды с твёрдыми
реагентами, а смешивать руду с серной кислотой значительно легче;
3)
отсутствуют длительные высокотемпературные процессы;
4)
получается карбонат, который легко может быть переведён в любую нужную литиевую
соль.
В настоящее время работают
над усовершенствованием сернокислотного способа переработки литиевых руд.
Известны исследования по переработке измельчённого сподуменового концентрата
путём длительной обработке его концентрированной серной кислотой при 250–400 °С
в автоклавах. Цель исследований – исключить предел декрипитации. Ведутся
исследования по вскрытию концентрата расплавленным гидросульфатом аммония при
290 °С [7].
Литература:
1. Самойлов В.И. Экспериментальная разработка перспективных
химических методов извлечения бериллия и лития из минерального сырья. –
Усть-Каменогорск: Медиа-Альянс, 2006. – 551 с.
2. Плющев В.Е., Cтёпин
Б.Д. Химия и технология соединений лития, рубидия
и цезия. – М.: Химия,
1970. – 408 с.
3. Остроушко Ю.И.,
Бучихин П.И., Алексеева В.В. и др. Литий, его химия и
технология. – М.:
Атомиздат, 1960. – 200 c.
4. Хлебникова Е.Н. Определение физико-химических характеристик минералов бериллия и лития, и
выбор оптимальных условий их вскрытия в гидрометаллургии: Дис. … магистра техн. наук. Усть-Каменогорск, 2013. – 87 с.
5. Зеликман А.Н.,
Меерсон Г.А. Металлургия редких металлов. – М.: Металлургия, 1973. – 608 c.
6. Зеликман А.Н.,
Коршунов Б.Г. Металлургия редких металлов. – М.: Металлургия, 1991. – 432 с.
7. Самойлов В.И.
Исследование современных и разработка перспективных методов извлечения лития из
минерального сырья в технические соединения. – Усть-Каменогорск: Медиа-Альянс,
2005. – 276 с.
8. Коленкова М.А., Крейн О.Е. Металлургия рассеяных и легких
редких металлов. – М.: Металлургия, 1977. – 360 с.
9. Химия и технология редких и рассеянных
элементов: В 2 т. / Под ред. К.А. Большакова. – Т. 2: Технология редких и рассеянных
элементов. – М.: Высшая школа, 1969. – 640 c.
10. Литий // Редкие
металлы / Под ред. О.С. Сергеевой: Сб. стат. – М.: ИЛ, 1954. – 105 с.
11. Плющев В.Е. Редкие
щелочные элементы. – Пермь, Издательство Пермского Политехнического Института,
1969. – 271-280 с.
12. Ягодин Г.А., Синегрибов
О.А., Чекмарев А.М. Технология редких металлов в атомной технике. – М.:
Атомиздат, 1974. – 343 с.