Экология / Экологические и метеорологические проблемы
больших городов и промышленных зон
д. т. н.,
профессор Краснова Т. А., аспирант Жулина К. В.,
студент
Хлопова А. В.
Кемеровский
технологический институт пищевой промышленности (университет)
Исследование адсорбции меланоидина на углеродных сорбентах
Основной причиной попадания меланоидинов в
водоемы является их поступление со сточными водами. Меланоидины широко используются
в пивоваренном производстве и являются составной частью сточных вод пищевых
предприятий. Меланоидины, образующиеся как отходы пищевого производства, могут
приводить к серьёзному загрязнению. В частности, из-за их тёмной окраски, они
блокируют прохождение солнечного света и снижают фотосинтез и
уровень кислорода в реках. Это требует особой обработки отходов перед сливом
производственных вод.
Наиболее перспективными методами очистки
сточных вод с низким содержанием органических веществ являются сорбционные
методы. Активные угли – широко использующиеся пористые сорбенты, известные как
эффективные поглотители растворенных веществ. В настоящее время на рынке
активных углей появились полукоксы – углеродные сорбенты, произведенные по
новой технологии, позволяющей снизить конечную цену активного угля.
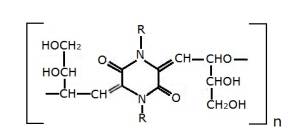
Рисунок 1 – Структурная
формула меланоидина
Целью работы было исследование возможности
использования активных углей (АУ) для адсорбционного извлечения меланоидинов.
Объектами исследования являлись модельные
растворы меланоидина и активные угли марок АГ-ОВ-1 и «Пуролат-Стандарт»,
отличающиеся способом получения, сырьем, структурой и химическим состоянием
поверхности. Более часто в практике используются гранулированный уголь
АГ-ОВ-1, «Пуролат-Стандарт» относится к
новым дешевым сорбентам (полукоксам). Меланоидин получали путем термической
обработки смеси чистых аминокислоты и глюкозы по стандартной методике.
Содержание меланоидинов определялось фотоколориметрическим методом при длине
волны 400 нм и толщине слоя 10 мм [1].
Адсорбция из водного раствора меланоидина
исследовалась при комнатной температуре из ограниченного объема при непрерывном
перемешивании в течение 8 часов в равновесных условиях в диапазоне концентраций
от 20 до 300 мг/дм3.
Изотермы адсорбции меланоидина относятся к
изотермам Н-типа, для которых характерно наличие специфического взаимодействия
сорбент – сорбат. Потенциометрическим титрованием определили состояние
поверхности углеродных сорбентов, свидетельствующее о наличии у обоих сорбентов
фенольных и карбоксильных групп. Исходя из структуры меланоидина (рис. 1) и
характеристик поверхности АУ можно предположить образование водородных связей
различной силы между кислородсодержащими функциональными группами (КФГ)
кислотного типа (фенольные и карбоксильные) [2, 3].
Для расчета адсорбционных параметров были
использованы теории мономолекулярной (Легмюр, Фрейдлих) и полимолекулярной
(БЭТ) адсорбции, а также теория объемного заполнения микропор (Дубинин –
Рудушкевич). Установлено, что адсорбционная емкость АГ-ОВ-1 выше в 2 раза, чем
емкость АУ «Пуролат-Стандарт», что связано с пористой структурой углей. Уголь
АГ-ОВ-1 имеет микро-, мезо- и макропоры. «Пуролат-Стандарт» имеет
преимущественно макропоры, причем объем макропор у него меньше суммарного
объема мезо- и микропор, чем у АУ АГ-ОА-1. Размер молекулы меланоидина исключает
адсорбцию меланоидина в микропорах. Адсорбция происходит в доступных мезо- и
макропорах. Значения энергии адсорбции сопоставимые с энергией водородной связи
подтверждает, что как у АУ АГ-ОВ-1, так и у «Пуролат-Стандарт» адсорбция
протекает за счет специфического взаимодействия на поверхности АУ.
Полученные результаты, свидетельствуют
принципиальной возможности использования активных углей (АУ) для адсорбционного
извлечения меланоидина.
Литература
1.
Мальцев, П. М.
Химико-технологический контроль производства солода и пива / П. М. Мальцев, Е.
И. Великая, М. В. Зазирная, П. В. Колотуша. – М.: Пищевая промышленность, 1976.
– 446 с.
2.
Селеменев, В. Ф.
пигменты пищевых производств (меланоидины) / В. Ф. Селемеев, О. Б. Рудаков, Г.
В. Славинская, Н. В. Дроздова. – М.: ДеЛи, 2008. – 246 с.
3.
Keller. Jorger. U. Gas adsorption equilibria: experimental methods and
adsorptive isotherms / Jorger. U. Keller/
- Springer US, 2005. - XIV, 422 с.